
【题目】关于乙炔分子中的共价键说法正确的是
A. sp杂化轨道形成σ键属于极性键,未杂化的2p轨道形成π键属于非极性键
B. C-H之间是sp-s形成σ键,与s-p σ键的对称性不同
C. (CN)2与乙炔都属于直线型分子,所以(CN)2分子中含有3个σ键和2个π键
D. 由于π键的键能比σ键的键能小,乙炔分子![]() 三键的键能小于C-C单键的键能的3倍,所以乙炔化学性质活泼易于发生加成反应
三键的键能小于C-C单键的键能的3倍,所以乙炔化学性质活泼易于发生加成反应
 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
【题目】某实验小组的同学在实验室利用下列装置进行实验。
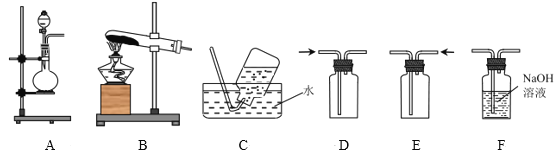
请回答下列问题:
(1)甲同学用A装置制备NO2气体,上述装置中可用于收集NO2气体的是___(填字母),A中发生反应的离子方程式为___。
(2)乙同学用图中的装置A进行铜与浓硫酸反应制取SO2气体,装置A中还缺少的仪器名称是___,该反应的化学方程式为___;实验所产生的SO2尾气选用装置___(填字母)来吸收。
(3)丙同学用装置B制取氨气,发生反应的化学方程式是___;为了检验集气瓶中氨气是否集满,可将湿润的红色石蕊试纸置于导管口,若___,则证明已收集满;若将一端蘸有浓盐酸的玻璃棒接近导管口,观察到的现象是___,该反应的化学方程式为___。
(4)丙同学在实验室中模拟氨的催化氧化反应,该反应中,当生成标准状况下11.2LNO时,被氧化的物质的质量是___g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组将下列装置如图连接,E、F、X、Y都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答下列问题:

(1)电源A极的名称是____,丁中____(填“X”或“Y”)极颜色会加深。
(2)欲用丙装置给铜镀银,H应该是____,电镀液的主要成分是____(填化学式)。
(3)如果收集乙装置中产生的气体,相同条件下两种气体的体积比是___。
(4)甲装置为使用过的铅蓄电池,充电后电极D应与用电器的____(填“正”或“负”)极连接,电极C上的电极反应式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A是最常用的食用油抗氧化剂,分子式为C10H12O5,可发生如下转化
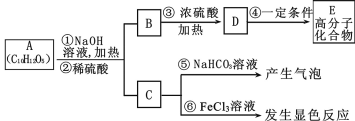
已知B的相对分子质量为60,分子中只含一个甲基。C的结构可表示为:
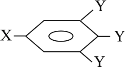 (其中:—X、—Y均为官能团)
(其中:—X、—Y均为官能团)
请回答下列问题:
(1)官能团-X的名称为____,反应③的类型为____;
(2)根据系统命名法,B的名称为____,高聚物E的链节为____;
(3)A的结构简式为____;
(4)反应⑤的化学方程式为____;
(5)C有多种同分异构体,其中符合下列要求的同分异构体共____种;
i.含有苯环 ii.能发生银镜反应 iii.不能发生水解反应
(6)从分子结构上看,A具有抗氧化作用的主要原因是____(填序号)。
a 含有苯环 b 含有羰基 c 含有酚羟基
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家利用H2-N2生物燃料电池,以固氮酶为正极催化剂、氢化酶为负极催化剂,在室温条件下即实现合成NH3的同时还获得电能,其工作原理如下图所示:
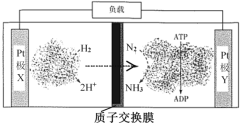
下列叙述不正确的是
A.该装置是将化学能转化为电能
B.正极反应:N2+6e-+6H+ = 2NH3
C.电池工作时H2在负极发生还原反应
D.电子沿X极板经导线向Y极板迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制备水合肼(N2H4·H2O)的反应原理是CO(NH2)2+ 2NaOH + NaClO=Na2CO3+N2H4·H2O+NaCl。已知CO(NH2)2沸点:133 ℃;水合肼是重要化工原料,沸点:118 ℃,易被氧化。请按要求回答下列制备水合肼实验的有关问题。
(1)制备 NaClO 溶液(实验装置如图所示)

锥形瓶中发生反应离子方程式是__________________________。
(2)制取水合肼(实验装置如右图所示,夹持装置已略)
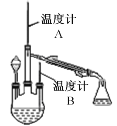
控制反应温度,再将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应后,加热蒸馏三颈烧瓶内的溶液,收集产品。
①分液漏斗中盛装的药品是NaOH溶液和_______________。
这样盛放的理由是防止___________________________________。
②本实验收集产品馏分时的关键条件是控制_______________________________。
(3)测定馏分中肼的含量。
①已知水合肼在一定条件下与I2反应生成N2,完成该反应原理的化学方程式:
____N2H4·H2O +____ I2 +6NaHCO3+H2SO4 = ____ N2↑+____ NaI +6CO2↑+Na2SO4 +7H2O
__________________________
②测定实验的步骤如下:
a.称取馏分 5.000 g,加水配制成1000 mL待测液溶液。
b.移取10.00 mL于锥形瓶中,加入10 mL水、稀硫酸、适量 NaHCO3固体(保证滴定过程中溶液的 pH 保持在 6.5左右)、2滴淀粉溶液,摇匀。
c.用0.2000 mol/L I2溶液滴定,至溶液呈现___________________________,记录消耗I2标准液的体积。
d._______________________________;然后处理数据。
③经数据处理,滴定消耗I2的标准溶液为 8.20 mL,馏分中水合肼(N2H4·H2O)的质量分数为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】改变0.1mol·L-1二元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数φ(X)随pH的变化如图所示。

下列叙述错误的是( )
A.pH=1.2时,c(H2A)=c(HA-)
B.lg[K2(H2A)]=-4.2
C.pH=2.7时,c(HA-)>c(H2A)=c(A2-)
D.pH=4.2时,c(HA-)=c(A2-)=c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X为一种常见酸的浓溶液,能使蔗糖粉末变黑。A与X反应的转化关系如图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是
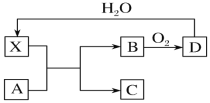
A.X使蔗糖变黑的现象主要体现了X的强氧化性
B.若A为铁,则足量A与X在室温下即可完全反应
C.工业上,B转化为D的反应条件为高温、常压、使用催化剂
D.若A为碳单质,则将C通入少量的澄清石灰水,一定可以观察到有白色沉淀产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为提升电池循环效率和稳定性,科学家近期利用三维多孔海绵状Zn(3DZn)可以高效沉积ZnO的特点,设计了采用强碱性电解质的3DZn—NiOOH二次电池,结构如下图所示。电池反应为Zn(s)+2NiOOH(s)+H2O(l)![]() ZnO(s)+2Ni(OH)2(s)。
ZnO(s)+2Ni(OH)2(s)。

A. 三维多孔海绵状Zn具有较高的表面积,所沉积的ZnO分散度高
B. 充电时阳极反应为Ni(OH)2(s)+OH(aq)e![]() NiOOH(s)+H2O(l)
NiOOH(s)+H2O(l)
C. 放电时负极反应为Zn(s)+2OH(aq)2e![]() ZnO(s)+H2O(l)
ZnO(s)+H2O(l)
D. 放电过程中OH通过隔膜从负极区移向正极区
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com