
【题目】已知CO2(g)+CH4(g)![]() 2CO(g)+2H2(g),达到平衡,若其它条件不变,将体积压缩至原来的1/2,达到新的平衡后,下列有关该体系的说法不正确的是( )
2CO(g)+2H2(g),达到平衡,若其它条件不变,将体积压缩至原来的1/2,达到新的平衡后,下列有关该体系的说法不正确的是( )
A.正、逆反应速率都加快 B.氢气的浓度与原平衡比减少
C.甲烷的物质的量增加 D.重新平衡时c(CO2) /c(CO)增大
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:
【题目】mX(g)+nY(g) ![]() qZ(g) △H<0, m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是
qZ(g) △H<0, m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是
A.通入稀有气体使压强增大,平衡将正向移动
B.X的正反应速率是Y的逆反应速率的m/n倍
C.降低温度,混合气体的平均相对分子质量变小
D.若平衡时X、Y的转化率相等,说明反应开始时X、Y的物质的量之比为n:m
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 溶解度大的化合物一定是强电解质
B. 胶体与溶液的本质区别是分散剂粒子大小的不同
C. 物质在发生化学反应的过程中,都伴随着能量的变化
D. 金属的冶炼必须在高温下进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一支50mL酸式滴定管其中盛有溶液,液面恰好在10mL刻度处,现把管内溶液全部流下排出,用量筒盛装,该溶液的体积应为
A. 10mL B. 40mL C. 大于40mL D. 小于40mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中发生反应:xA(g)+B(g)![]() 2C(g) △H<0,A、C的物质的量随时间变化的关系如右表所示。下列有关说法正确的是
2C(g) △H<0,A、C的物质的量随时间变化的关系如右表所示。下列有关说法正确的是

A. x=1
B. 反应开始2min内,用B表示的反应速率为0.05mol · L-l · min -1
C. 反应进行到lmin时,反应体系达到化学平衡状态
D. A的正反应速率等于C的逆反应速率时,反应体系达到化学平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CH4(g)+2O2(g)→CO2(g)+2H2O(g) ΔH=-Q1;
2H2(g)+O2(g)=2H2O(g) ΔH=-Q2;
H2O(g)=H2O(l) ΔH=-Q3
常温下,取体积比为4:1的甲烷和H2的混合气体112L(标准状况下),经完全燃烧后恢复到常温,则放出的热量为( )
A.4Q1+0.5Q2 B.4Q1+Q2+10Q3 C.4Q1+2Q2 D.4Q1+0.5Q2+9Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液X中可能含有下列离子中的若干种:Cl-、SO42-、SO32-、HCO3-、Na+、Mg2+、Fe3+,所含离子的物质的量浓度均相同。为了确定该溶液的组成,某同学取100mL上述溶液X,进行了如下实验:
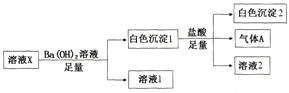
下列说法正确的是
A. 气体A可能是CO2或SO2
B. 溶液X中一定存在SO42-、HCO3-、Na+、Mg2+
C. 溶液X中一定不存在Fe3+和Mg2+,可能存在Na+
D. 分别在溶液1和溶液2中加入硝酸酸化的硝酸银溶液都能生成白色沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com