
����Ŀ��ij�¶��£�Ksp[Pd(OH)2]=1.0��10-30�������ʵ���Ũ����ͬ��NaOH��Na2S�Ļ����Һ�еμ�Pd(NO3)2��Һ����Pd(OH)2��PdS���ֳ�������Һ�������ӡ�������Ũ�ȹ�ϵ��ͼ��ʾ��ͼ�е�p(Pd)=-lgc(Pd2+)��p(B)=-lgc(OH-)��-lgc(S2-)������˵��������ǣ� ��

A. ���ߢ��ʾ����Pd2+��OH-Ũ�ȹ�ϵ������
B. ���¶��£�Ksp(PdS)=1.0��10 -58
C. �����¶�ʱ��b����ܻ���c���ƶ�
D. ���¶��£���d���Ӧ����Һ�м����Ӧ�����ӵ����Σ�d����b���ƶ�
���𰸡�C
��������
A. �����ߢ��ʾ����Pd2+��OH-Ũ�ȹ�ϵ����c��OH-��= c��Pd2+��=1.0��10-10mol/L��c��OH-��2��c��Pd2+��=��1.0��10-10mol/L��2��1.0��10-10mol/L=1.0��10-30=Ksp[Pd(OH)2]����A��ȷ��
B. ����Aѡ����������ߢ��ʾPdS���ܽ�ƽ�����ߣ����ﵽƽ��ʱ��c��S2-��= c��Pd2+��=1.0��10-29mol/L�����¶��£�Ksp(PdS)=1.0��10-29 mol/L��1.0��10 -29mol/L=1.0��10 -58����B��ȷ��
C. �����¶�ʱ���������ܽ�ƽ���������ƶ���c��S2-����c��Pd2+����������C����
D. ���¶��£���d���Ӧ����Һ�м������ƣ������ӵ�Ũ�����������ܽ�ƽ���������ƶ����γɳ����ķ���c��Pd2+�����С��d����b���ƶ�����D��ȷ��
��ѡC��


 ̽���빮�̺��Ͽ�ѧ����������ϵ�д�
̽���빮�̺��Ͽ�ѧ����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡ���沿��������þ��8.00g����250mL4.00mol��L-1��ϡ�����У���������Һ�еμ�δ֪Ũ�ȵ�NaOH��Һ������������������NaOH��Һ�������ϵ��ͼ��ʾ��
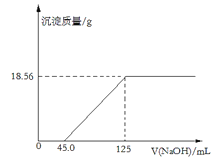
����㣺
��1��NaOH��Һ�����ʵ���Ũ��___mol��L-1��
��2����Ʒ��þԪ�ص�����___g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�������14��Ԫ�صĵ縺�ԣ�
Ԫ�� | �縺�� | Ԫ�� | �縺�� | Ԫ�� | �縺�� |
Al | 1.5 | B | 2.0 | Be | 1.5 |
C | 2.5 | Cl | 3.0 | F | 4.0 |
Li | 1.0 | Mg | 1.2 | N | 3.0 |
Na | 0.9 | O | 3.5 | P | 2.1 |
Cl | 2.5 | S | 1.8 |
(1)ͬһ�����У������ң�����Ԫ�صĵ縺��_________��ͬһ�����У����ϵ��£�Ԫ�صĵ縺��_________������Ԫ�صĵ縺����ԭ������������_________�仯��
(2)������Ԫ���У��縺������Ԫ����縺����С��Ԫ���γɵĻ���������____________������õ���ʽ��ʾ�û����___________________��
(3)��֪�����ɼ�Ԫ�ؼ�ĵ縺�Բ�ֵ����1.7ʱ��ͨ���γ����Ӽ������ɼ�Ԫ�ؼ�ĵ縺�Բ�ֵС��1.7ʱ��ͨ���γɹ��ۼ�����Mg3N2��BeCl2��AlCl3��SiC��Ϊ���ӻ��������_________��Ϊ���ۻ��������__________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪������(C2H5Br)����ɫҺ�壬�е�38.4�棬�ܶȱ�ˮ��������ˮ�������ڶ����л��ܼ�������������NaOH�Ҵ���Һ����ȥ��Ӧ�п��Թ۲쵽���������ɡ������������ͼ��ʾ��װ�ã���KMnO4������Һ�Ƿ���ɫ���������ɵ������Ƿ�����ϩ��

��ش��������⣺
(1)����a������Ϊ__________��
(2)ʵ��ǰӦ���װ��A�������ԡ��������£��ر�ֹˮ��c��������a������b�м�ˮ����______________________________����֤��װ��A��©����
(3)����b�з�����Ӧ�Ļ�ѧ����ʽΪ______________________________��
(4)��Ӧ��ʼһ��ʱ�����װ��B�ײ������˽϶����״Һ�壬���������״Һ����������ɶ�װ��A���θĽ���__________________________________________________
(5)װ��A�в���������ͨ��װ��C֮ǰҪ��ͨ��װ��B��װ��B������Ϊ__________________��
(6)������ϩ����KMnO4������Һ���ѡ�õ��Լ���__________����ʱ���Ƿ��б�Ҫ��������ͨ��װ��B��__________(����������������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����в�������������ԭ�����͵���ʵ�ǣ� ��
A���غ�ɫ��NO2��ѹ����ɫ�ȱ�����dz
B�����������������⻯��������ɵ�ƽ����ϵ��ѹ����ɫ����
C������ɫ����ˮ���պ���ɫ��dz
D���ϳɰ���ҵʹ�ø�ѹ����߰��IJ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������¶���ڿ����У��۲쵽��������
![]()
��ش��������⣺
��1����ɫ��ĩ�Ļ�ѧʽ��__________�����̢ڵĻ�ѧ����ʽ��_________��
��2������˵����ȷ����________��
A. ���̢�Ϊ�����仯
B. ���̢���̼�������տ����е�CO2��ˮ�����γ���̼������
C. ���̢ݷ����˷ֽⷴӦ
D. �����仯������ֻ��һ��������ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС��������ͼ��ʾװ���Ʊ�����NCl3����֪��NCl3����Cl2��NH4Cl��Һ�������¶��·�Ӧ���ɡ������£�NCl3Ϊ��ɫ��״Һ�壬�۵�Ϊ-40�棬�е�Ϊ71�棻���ױ�ը����Ȼ��ը��Ϊ95�档
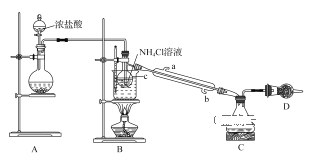
�ش��������⣺
��1��װ��A��Բ����ƿ����ʢ�ŵĹ�����___���ѧʽ����
��2��װ��B������C��������___��ʵ������и������ڷ�����Ӧ�Ļ�ѧ����ʽΪ___��
��3��װ��B���ձ���Ӧ����ˮԡ���ȵ��¶ȷ�ΧΪ____��
��4��װ��D����ʢ�ŵ��Լ�����Ϊ����ѡ���е�___������ĸ����
a����ʯ�� b��NaOH���� C����ʯ�� d����ˮCaCl2
��5���������Ͽ�֪�����pH<5��NH4Cl��ҺҲ���Ƶ�NCl3��������в���NCl3�ĵ缫Ϊ___��������������������������õ缫�ĵ缫��ӦʽΪ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ������Ũ�Ⱦ�Ϊ![]() �����ᡢ���ᡢ����������Һ,�ش��������⣺
�����ᡢ���ᡢ����������Һ,�ش��������⣺
��1����������Һ��![]() �ֱ�Ϊ
�ֱ�Ϊ![]() ,�����ǵĴ�С��ϵΪ_________________________________________��
,�����ǵĴ�С��ϵΪ_________________________________________��
��2�������������������ֱ��������![]() ��Һ��Ӧ,�����ɵ��ε����ʵ�������Ϊ
��Һ��Ӧ,�����ɵ��ε����ʵ�������Ϊ![]() �������ǵĴ�С��ϵΪ__________________________��
�������ǵĴ�С��ϵΪ__________________________��
��3���ֱ��������������к�һ������![]() ��Һ��������,����Ҫ�������ֱ�Ϊ
��Һ��������,����Ҫ�������ֱ�Ϊ![]() �����С��ϵΪ__________________________________��
�����С��ϵΪ__________________________________��
��4���ֱ���п��Ӧ,��ʼʱ��������������Ϊ![]() �����С��ϵΪ______________________��
�����С��ϵΪ______________________��
��������![]() ����ǿ�����,������ˮ�е�������������ӣ�ÿ������ֻ��һ���������һ����ظ�����
����ǿ�����,������ˮ�е�������������ӣ�ÿ������ֻ��һ���������һ����ظ�����
������ |
|
������ |
|
��֪:��![]() ��Һ��
��Һ��![]() ������7,
������7, ![]() ����Һ��ˮ�ĵ���̶���ͬ����
����Һ��ˮ�ĵ���̶���ͬ����![]() ��Һ��
��Һ��![]() ��Һ����ʱֻ���ɰ�ɫ����,
��Һ����ʱֻ���ɰ�ɫ����, ![]() ��Һ��
��Һ��![]() ��Һ����ʱֻ���ɴ̼�����ζ������,
��Һ����ʱֻ���ɴ̼�����ζ������, ![]() ��Һ��
��Һ��![]() ��Һ���ʱ������
��Һ���ʱ������
��1�� ![]() ��_________________________��
��_________________________��![]() ��_______________________���ѧʽ����
��_______________________���ѧʽ����
��2���![]() ��
��![]() ��Ӧ�����ӷ���ʽ_________________________________��
��Ӧ�����ӷ���ʽ_________________________________��
��3�� ![]() ʱ,
ʱ, ![]() ��Һ��
��Һ��![]() ,��
,��![]() ��Һ��
��Һ��![]() _________________________________________���ú���
_________________________________________���ú���![]() �Ĺ�ϵʽ��ʾ����
�Ĺ�ϵʽ��ʾ����
��4����������������ʵ���Ũ�ȵ�![]() ��Һ��
��Һ��![]() ��Һ���,��Ӧ����Һ�и�������Ũ���ɴ�С��˳����_________________________��
��Һ���,��Ӧ����Һ�и�������Ũ���ɴ�С��˳����_________________________��
��5����һ�������![]() ��
��![]() ��Һ��,����һ�������
��Һ��,����һ�������![]() ������,�����Һ��
������,�����Һ��![]() ,����Ӧ����Һ���������
,����Ӧ����Һ���������![]() ��Һ����������֮��,��
��Һ����������֮��,��![]() ��Һ��������������_______________��
��Һ��������������_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ������N2��H2����ʵ�ֺϳɰ����������ֿ��Խ�һ���Ʊ����ᣬ�ڹ�ҵ��һ��ɽ���������������ش������й����⣺
��1����֪N2(g)+O2(g)=2NO(g) ��H =+180.5kJ��mol��1��N2(g)+3H2(g)![]() 2NH3(g) ��H =��92.4kJ��mol��1��2H2(g)+O2(g)=2H2O(g) ��H =��483.6kJ��mol��1��д����������������ȫ����һ��������ˮ�������Ȼ�ѧ����ʽΪ___________��
2NH3(g) ��H =��92.4kJ��mol��1��2H2(g)+O2(g)=2H2O(g) ��H =��483.6kJ��mol��1��д����������������ȫ����һ��������ˮ�������Ȼ�ѧ����ʽΪ___________��
��2����һ��������ܱ������У��������»�ѧ��Ӧ��N2(g)+3H2(g)![]() 2NH3(g)���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
2NH3(g)���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
t/K | 298 | 398 | 498 | ...... |
K/(mol/L)2 | 4.1��106 | K1 | K2 | ...... |
����������⣺
�ٱȽ�K1��K2�Ĵ�С��K1______K2(�>������=����<��)��
���ں��º�ѹ���жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������______(�����)��
A��2v(H2)(��)=3v(NH3)(��) B��2v(N2) (��)=v(H2) (��)
C��������ѹǿ���ֲ��� D�����������ܶȱ��ֲ���
��3�����Ṥҵ��β��NO�������Ʊ�NH4NO3���乤��ԭ����ͼ��
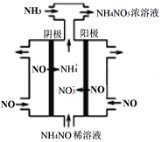
���������ĵ缫��ӦʽΪ___________��
�ڳ����£�1L pH=6��NH4NO3��Һ��c(NH3��H2O)+c(OH��)=________mol��L��1��
��4����ҵ���������صĻ�ѧ����ʽΪ��2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(l)����T�棬���Ϊ4L���ܱ������У�ͨ��6mol NH3��3mol CO2����Ӧ�ﵽƽ��ʱ��c(NH3)=0.5mol��L��1��c(CO2)=0.25mol��L��1������ʱ����T���ƽ��ʱ������ѹǿ���䣬��������ɱ�������г���3mol NH3�����ʱ��Ӧ��v��____ v��(�>����<����=��)���ٴ�ƽ���ƽ�ⳣ��Ϊ______��
CO(NH2)2(s)+H2O(l)����T�棬���Ϊ4L���ܱ������У�ͨ��6mol NH3��3mol CO2����Ӧ�ﵽƽ��ʱ��c(NH3)=0.5mol��L��1��c(CO2)=0.25mol��L��1������ʱ����T���ƽ��ʱ������ѹǿ���䣬��������ɱ�������г���3mol NH3�����ʱ��Ӧ��v��____ v��(�>����<����=��)���ٴ�ƽ���ƽ�ⳣ��Ϊ______��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com