
【题目】下列各组物质中,能用酸性高锰酸钾溶液鉴别的是
A. 乙烯、乙炔 B. 己烷、苯 C. 己烯、苯 D. 乙醇、乙醛
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
【题目】下列实验能达到目的的是( )
A.用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸
B.用NaOH溶液与FeCl3溶液制备Fe(OH)3胶体
C.用品红和盐酸检验Na2SO3和Na2CO3
D.将混有乙烯的SO2通入酸性KMnO4溶液中除去乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于固定体积的密闭容器中进行的气体反应可以说明A(g) + B(g)![]() C(g)+D(g)在恒温下已达到平衡的是
C(g)+D(g)在恒温下已达到平衡的是
A.反应容器的压强不随时间而变化
B.A气体和B气体的生成速率相等
C.A、B、C三种气体的生成速率相等
D.反应混合气体的密度不随时间而变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用电解法可将含有Fe、Zn、Ag、Pt等杂质的粗铜提纯,下列叙述正确的是( )
A.电解时以精铜作阳极
B.电解时阴极发生氧化反应
C.粗铜连接电源负极,其电极反应是Cu-2e-=Cu2+
D.电解后,电解槽底部会形成含少量Ag、Pt等金属的阳极泥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1000 mol/L NaOH溶液分别滴定20.00 mL 0.1000 mol/L盐酸和20.00 mL 0.1000 mol/L醋酸溶液,得到2条滴定曲线,如下图所示。若用HA表示酸,下列说法正确的是( )
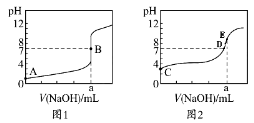
A.滴定盐酸的曲线是图2
B.达到B、D状态时,两溶液中离子浓度均为c(Na+)=c(A-)
C.达到B、E状态时,反应消耗的n(CH3COOH)>n(HCl)
D.当V(NaOH)=20.00 mL时,两混合溶液中各离子浓度由大到小的顺序均为c(Na+)>c(A-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SnSO4是一种重要的硫酸盐,在工业生产中有着广泛的应用。其制备路线如下:

已知:在酸性条件下,溶液中的Sn2+可被空气中的氧气氧化成Sn4+; SnCl2能水解生成碱式氯化亚锡[Sn(OH)Cl]。
(1)写出物质A的名称: 。
(2)SnCl2用盐酸而不用水溶解的原因是: 。
(3)锡粉的作用是除去酸溶时产生的少量Sn4+,请写出产生Sn4+的离子方程式: 。
(4)反应I生成的沉淀为SnO,写出该反应的化学方程式: 。
(5)实验室中“漂洗”沉淀的实验操作方法是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1451.6kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH=-566.0kJ/mol
(1)写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式_______________
(2)某小组根据甲醇燃烧的反应原理,设计如图所示的电池装置:
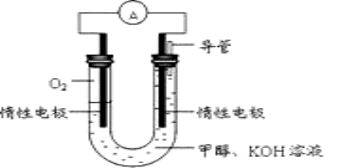
该电池正极的电极反应式____________________
工作一段时间后,测得溶液的pH______________(填增大、减小或不变),则该电池总反应的离子方程式__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解后,向混合溶液中滴加1mol·L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示。下列有关判断正确的是( )

A.AB段发生反应的离子方程式为Ba2++SO42-=BaSO4↓
B.BC段发生反应的离子方程式为H++OH-=H2O
C.D点表示的沉淀的化学式为Al(OH)3
D.E点时溶液中含有大量的AlO2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将甲酸和氢氧化钠溶液混合,所得溶液pH=7,则此溶液中( )
A. c(HCOO-)>c(Na+) B. c(HCOO-)<c(Na+)
C. c(HCOO-)=c(Na+) D. 无法确定c(HCOO-)与c(Na+)的关系
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com