
【题目】短周期主族元素![]() 的原子序数依次增大,W原子的最外层电子数等于Y原子最外层电子数的2倍;四种元素形成的一种化合物的结构如图所示,该化合物的阴离子中每个原子的最外层均满足8电子稳定结构,下列说法错误的是( )
的原子序数依次增大,W原子的最外层电子数等于Y原子最外层电子数的2倍;四种元素形成的一种化合物的结构如图所示,该化合物的阴离子中每个原子的最外层均满足8电子稳定结构,下列说法错误的是( )

A.原子半径:![]() B.W与Z形成晶体的基本单元为平面结构
B.W与Z形成晶体的基本单元为平面结构
C.X与Z在自然界中均不存在游离态D.W与Y形成的化合物可作耐火材料
【答案】B
【解析】
短周期主族元素W、X、Y、Z的原子序数依次增大,X、Y的简单离子为X+、Y3+,则X原子的最外层电子数是1、Y原子的最外层电子数是3,W原子的最外层电子数等于Y原子最外层电子数的2倍,则W为O、X为Na、Y为Al,由四种元素形成的一种化合物的结构图所示可知Z为+4价,且化合物中Z原子的最外层均满足8电子稳定结构,则Z为Si元素。
由分析知:W为O元素、X为Na元素、Y为Al元素、W为Si元素;
A.Na、Al、Si、S为同周期主族元素,核电荷数大,原子半径小,则原子半径Na>Al>Si>S,而O和S为同主族元素,S的原子半径大于O,则原子半径Na>Al>Si>O,故A正确;
B.O与Si组成的SiO2是原子晶体,是空间立体网状结构,故B错误;
C.Na是活泼金属,而Si是亲氧元素,则Na和Si在自然界均只有化合态,不存在游离态,故C正确;
D.Al2O3的熔点高,是高温耐火材料,故D正确;
故答案为B。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】(1)2012年伦敦奥运会火炬采用丙烷为燃料。丙烷热值较高,污染较小,是一种优良的燃料。试回答下列问题:

①如图是一定量丙烷完全燃烧生成CO2和1 mol H2O(l)过程中的能量变化图,请在图中的括号内填入“+”或“-”。
②写出表示丙烷燃烧热的热化学方程式:___________________________________。
③二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔。1 mol二甲醚完全燃烧生成CO2和液态水放出1 455 kJ热量。若1 mol丙烷和二甲醚的混合气体完全燃烧生成CO2和液态水共放出1 645 kJ热量,则混合气体中,丙烷和二甲醚的物质的量之比为________。
(2)盖斯定律认为:不管化学过程是一步完成或分几步完成,整个过程的总热效应相同。试运用盖斯定律回答下列问题:
①已知:H2O(g)=H2O(l) ΔH1=-Q1 kJ/mol C2H5OH(g)=C2H5OH(l) ΔH=-Q2 kJ/mol
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g) ΔH3=-Q3 kJ/mol
若使46 g液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为________kJ。
②碳(s)在氧气供应不充足时,生成CO同时还部分生成CO2,因此无法通过实验直接测得反应: C(s)+![]() O2(g)=CO(g)的ΔH。但可设计实验、利用盖斯定律计算出该反应的ΔH,计算时需要测得的实验数据有________。
O2(g)=CO(g)的ΔH。但可设计实验、利用盖斯定律计算出该反应的ΔH,计算时需要测得的实验数据有________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NA是阿伏加德罗常数的值,下列关于铜生锈反应2Cu+O2+H2O+CO2=Cu2(OH)2CO3的说法错误的是
A.消耗32gCu转移的电子数为NAB.1.8g H2O含有的质子数为NA
C.22g CO2的共用电子对数为NAD.标况下,11.2LO2和CO2混合气体中O原子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,1mol化学键断裂形成气态原子所需要的能量用![]() 表示。结合表中信息判断下列说法不正确的是( )
表示。结合表中信息判断下列说法不正确的是( )
共价键 | H-H | F-F | H-F | H-Cl | H-I |
E(kJ/mol) | 436 | 157 | 568 | 432 | 298 |
A. 432kJ/mol>E(H-Br)>298kJ/mol B. 表中最稳定的共价键是H-F键
C. H2(g)→2H(g) △H=+436kJ/mol D. H2(g)+F2(g)=2HF(g) △H=-25kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
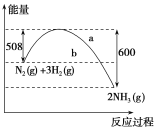
【题目】(1)如图是298K、101 kPa时,N2与H2反应过程中能量变化的曲线图。该反应的热化学方程式为____。
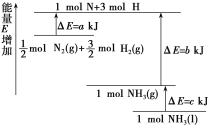
(2)化学反应N2+3H2![]() 2NH3的能量变化如图所示(假设该反应反应完全),试写出N2(g)和H2(g)反应生成NH3(l)的热化学方程式:____。
2NH3的能量变化如图所示(假设该反应反应完全),试写出N2(g)和H2(g)反应生成NH3(l)的热化学方程式:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用0.50mol·L-1 NaOH溶液和0.50mol·L-1硫酸溶液进行反应热的测定。
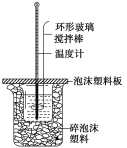
(1)写出该反应的热化学方程式[生成1 molH2O(l)时的反应热为-57.3 kJ·mol-1]:___。
(2)取50 mLNaOH溶液和30 mL 硫酸溶液进行实验,实验数据如表。
①请填写表中的空白:
温度 次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | ___ |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似认为0.50mol·L-1NaOH溶液和0.50mol·L-1硫酸溶液的密度都是1.0g·mL-1,中和后生成溶液的比热容c=4.18J/(g·℃)。则生成1 mol H2O(l)时的反应热ΔH=___(取小数点后一位)。
③上述实验数值结果与-57.3kJ·mol-1有偏差,产生偏差的原因不可能是(填字母)___。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅳ所示。
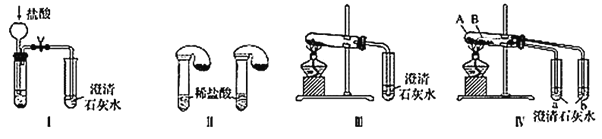
(1)只根据图Ⅰ、Ⅱ所示实验,能够达到实验目的的是________(填装置序号)。
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为__________;与实验Ⅲ相比,实验Ⅳ的优点是_____(填字母)。
A.Ⅳ比Ⅲ复杂
B.Ⅳ比Ⅲ安全
C.Ⅳ比Ⅲ操作简便
D.Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行
(3)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是________(填化学式),实验过程中的现象为__________。
(4)除了以上方法,请你再举出一例鉴别二者的方法:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的铁粉和硫粉的混合物共热,充分反应后冷却,再加入足量的稀硫酸,得到标准状况下的气体11.2 L,则原混合物可能的组成是(n代表物质的量)( )
A.n(Fe)<n(S),总质量等于44 g
B.n(Fe)>n(S),总质量等于44 g
C.n(Fe)=n(S),总质量小于44 g
D.n(Fe)>n(S),总质量小于44 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如右图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验不合理的是( )
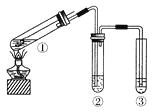
A. 上下移动①中铜丝可控制SO2的量
B. ②中选用品红溶液验证SO2的生成
C. ③中选用NaOH溶液吸收多余的SO2
D. 为确认CuSO4生成,向①中加水,观察颜色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com