
¡¾̀âÄ¿¡¿Ä³Đ£»¯Ñ§¿ÎÍâĐ¡×éΪÁ˼ø±đ̀¼ËáÄƺÍ̀¼ËáÇâÄÆÁ½ÖÖ°×É«¹̀̀壬ÓĂ²»Í¬µÄ·½·¨×öÁË̉ÔÏÂʵÑ飬Èçͼ¢ñ¡«¢ôËùʾ¡£
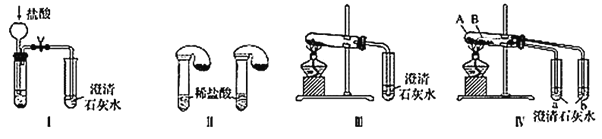
(1)Ö»¸ù¾Ưͼ¢ñ¡¢¢̣ËùʾʵÑ飬Äܹ»´ïµ½ÊµÑéÄ¿µÄµÄÊÇ________(̀î×°ÖĂĐ̣ºÅ)¡£
(2)ͼ¢ó¡¢¢ôËùʾʵÑé¾ùÄܼø±đƠâÁ½ÖÖÎïÖÊ£¬Æä·´Ó¦µÄ»¯Ñ§·½³̀ʽΪ__________£»ÓëʵÑé¢óÏà±È£¬ÊµÑé¢ôµÄÓŵăÊÇ_____(̀î×Öĸ)¡£
A.¢ô±È¢ó¸´ÔÓ
B.¢ô±È¢ó°²È«
C.¢ô±È¢ó²Ù×÷¼̣±ă
D.¢ô¿É̉Ô×öµ½ÓẲ»̀××°ÖĂͬʱ½øĐĐÁ½¸ö¶Ô±ÈʵÑ飬¶ø¢ó²»ĐĐ
(3)ÈôÓĂʵÑé¢ôÑéÖ¤̀¼ËáÄƺÍ̀¼ËáÇâÄƵÄÎȶ¨ĐÔ£¬ỘÊÔ¹ÜBÖĐ×°ÈëµÄ¹̀̀å×îºĂÊÇ________(̀ѧʽ)£¬ÊµÑé¹ư³̀ÖеÄÏÖÏóΪ__________¡£
(4)³ưÁË̉ÔÉÏ·½·¨£¬ÇëÄăÔپٳö̉»Àư¼ø±đ¶₫Ơߵķ½·¨£º__________¡£
¡¾´đ°¸¡¿¢̣ 2NaHCO3![]() Na2CO3£«H2O£«CO2¡ü£¬CO2£«Ca(OH)2=CaCO3¡ư£«H2O D NaHCO3 aÖĐ³ÎÇåʯ»̉Ë®±ä»ë×Ç£¬bÖĐ³ÎÇåʯ»̉Ë®²»±ä»ë×Ç °Ñ¶₫Ơß·Ö±đÅä³ÉÈÜ̉ººóµÎ¼ÓBaCl2ÊÔ¼Á£¬ÓĐ°×É«³ÁµíÉú³ÉµÄΪNa2CO3£¬Î̃ÏÖÏóµÄΪNaHCO3
Na2CO3£«H2O£«CO2¡ü£¬CO2£«Ca(OH)2=CaCO3¡ư£«H2O D NaHCO3 aÖĐ³ÎÇåʯ»̉Ë®±ä»ë×Ç£¬bÖĐ³ÎÇåʯ»̉Ë®²»±ä»ë×Ç °Ñ¶₫Ơß·Ö±đÅä³ÉÈÜ̉ººóµÎ¼ÓBaCl2ÊÔ¼Á£¬ÓĐ°×É«³ÁµíÉú³ÉµÄΪNa2CO3£¬Î̃ÏÖÏóµÄΪNaHCO3
¡¾½âÎö¡¿
(1)̀¼ËáÄÆ¡¢̀¼ËáÇâÄƾù¿É̉ÔÓëÑÎËá·´Ó¦²úÉú¶₫Ñơ»¯̀¼£¬µ«̀¼ËáÇâÄÆÓëÑÎËá·´Ó¦µÄËÙÂÊ´óÓÚ̀¼ËáÄÆ£»
(2) ̀¼ËáÄÆÖ±½Ó¼ÓÈȲ»·Ö½â£¬¶ø̀¼ËáÇâÄƼÓÈÈÉú³É̀¼ËáÄÆ¡¢¶₫Ñơ»¯̀¼Æø̀塢ˮ£»
(3)̀¼ËáÄÆÖ±½Ó¼ÓÈȲ»²úÉúÆø̀壬¶ø̀¼ËáÇâÄƲ»Ö±½Ó¼ÓÈȾͲúÉúÆø̀壬¸üÄÜ˵Ă÷̀¼ËáÇâÄƲ»Îȶ¨£»
(4)Na2CO3ÓëÂÈ»¯±µ·´Ó¦Éú³É̀¼Ëá±µ³Áµí¡¢NaHCO3ÓëÂÈ»¯±µ²»·´Ó¦¡£
(1)ͼ¢ñ²»ÄܴﵽʵÑéÄ¿µÄ£¬̣̉ΪÎ̃ÂÛ̀¼ËáÄÆ»¹ÊÇ̀¼ËáÇâÄƾù¿É̉ÔÓëÑÎËá·´Ó¦²úÉú¶₫Ñơ»¯̀¼£¬¶₫Ñơ»¯̀¼Æø̀åÓë³ÎÇåʯ»̉Ë®×÷Óñä»ë×Ç£¬¹Ê²»¿É̉Ô£»Í¼¢̣¿É̉Ô¼ø±đ£¬̣̉ΪµÈÖÊÁ¿µÄ̀¼ËáÄƺÍ̀¼ËáÇâÄÆÓë×ăÁ¿µÄÏ¡ÑÎËá·´Ó¦£¬Éú³ÉµÄ¶₫Ñơ»¯̀¼Æø̀åµÄÁ¿²»Í¬£¬¿É¸ù¾ƯÆøÇ̣Ạ̊Ơͳ̀¶ÈÀ´ÅĐ¶Ï¡£
(2)ͼ¢ó¡¢¢ôËùÉæ¼°µÄ»¯Ñ§·½³̀ʽΪ2NaHCO3![]() Na2CO3£«H2O£«CO2¡ü¡¢CO2£«Ca(OH)2=CaCO3¡ư£«H2O£¬ÊµÑé¢ôµÄÓŵăÊÇ¿Éͬʱ×ö¶Ô±ÈʵÑ飬¹ÊÑ¡D¡£
Na2CO3£«H2O£«CO2¡ü¡¢CO2£«Ca(OH)2=CaCO3¡ư£«H2O£¬ÊµÑé¢ôµÄÓŵăÊÇ¿Éͬʱ×ö¶Ô±ÈʵÑ飬¹ÊÑ¡D¡£
(3)̀¼ËáÄÆÖ±½Ó¼ÓÈȲ»²úÉúÆø̀壬¶ø̀¼ËáÇâÄƲ»Ö±½Ó¼ÓÈȾͲúÉúÆø̀壬¸üÄÜ˵Ă÷̀¼ËáÇâÄƲ»Îȶ¨£¬Ëù̉ÔÊÔ¹ÜBÖĐ×°ÈëµÄ¹̀̀å×îºĂÊÇ̀¼ËáÇâÄÆ£¬¹Û²́µ½µÄÏÖÏóΪaÖĐ³ÎÇåʯ»̉Ë®±ä»ë×Ç£¬bÖĐ³ÎÇåʯ»̉Ë®²»±ä»ë×Ç¡£
(4)¼ø±đNa2CO3ºÍNaHCO3»¹¿ÉÀûÓĂÆäÔÚÈÜ̉ºÖеçÀë³öµÄ̉ơÀë×ӵIJ»Í¬ĐÔÖÊÑ¡ÔñÊÔ¼Á£¬CO32¡ªÓëBa2£«»̣Ca2£«·´Ó¦Éú³É°×É«³Áµí£¬HCO3¡ªÓëBa2£«¡¢Ca2£«²»·´Ó¦£¬Ëù̉Ô¿É̉ÔÓĂÂÈ»¯±µÈÜ̉º¼ø±đNa2CO3ºÍNaHCO3¡£



| Ä꼶 | ¸ßÖĐ¿Î³̀ | Ä꼶 | ³ơÖĐ¿Î³̀ |
| ¸ß̉» | ¸ß̉»Ăâ·Ñ¿Î³̀ÍƼö£¡ | ³ở» | ³ở»Ăâ·Ñ¿Î³̀ÍƼö£¡ |
| ¸ß¶₫ | ¸ß¶₫Ăâ·Ñ¿Î³̀ÍƼö£¡ | ³ơ¶₫ | ³ơ¶₫Ăâ·Ñ¿Î³̀ÍƼö£¡ |
| ¸ßÈư | ¸ßÈưĂâ·Ñ¿Î³̀ÍƼö£¡ | ³ơÈư | ³ơÈưĂâ·Ñ¿Î³̀ÍƼö£¡ |
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
¡¾̀âÄ¿¡¿Ä³ÑĐ¾¿ĐÔÑ§Ï°Đ¡×éÀûÓĂH2C2O4ÈÜ̉ººÍËáĐÔKMnO4ÈÜ̉ºµÄ·´Ó¦̀½¾¿¡°Íâ½ç̀ơ¼₫µÄ¸Ä±ä¶Ô»¯Ñ§·´Ó¦ËÙÂʵÄÓ°Ḯ¡±£¬½øĐĐÁËÈçÏÂʵÑ飺
ʵÑéĐ̣ºÅ | ʵÑé ζÈ/K | ÓĐ¹ØÎïÖÊ | ÈÜ̉ºÑƠÉ«ÍÊÖÁÎ̃É«ËùĐèʱ¼ä/s | ||||
ËáĐÔKMnO4ÈÜ̉º | H2C2O4ÈÜ̉º | H2O | |||||
V/mL | c/mol¡¤L-1 | V/mL | c/mol¡¤L-1 | V/mL | |||
A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
£¨1£©Í¨¹ưʵÑéA¡¢B£¬¿É̀½¾¿³ö___(̀îÍⲿ̣̉ËØ)µÄ¸Ä±ä¶Ô»¯Ñ§·´Ó¦ËÙÂʵÄÓ°Ḯ£¬ÆäÖĐV1£½____¡¢T1£½____£»Í¨¹ưʵÑé___(̀îʵÑéĐ̣ºÅ)¿É̀½¾¿³öζȱ仯¶Ô»¯Ñ§·´Ó¦ËÙÂʵÄÓ°Ḯ£¬ÆäÖĐV2£½____¡£
£¨2£©Èôt1£¼8£¬ỘÓÉ´ËʵÑé¿É̉ÔµĂ³öµÄ½áÂÛÊÇ_____£»ºöÂÔÈÜ̉º̀å»ưµÄ±ä»¯£¬ÀûÓĂʵÑéBÖĐÊư¾Ư¼ÆËă£¬0¡«8sÄÚ£¬ÓĂKMnO4µÄŨ¶È±ä»¯±íʾµÄ·´Ó¦ËÙÂÊv(KMnO4)£½___¡£
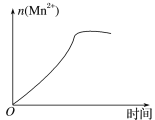
£¨3£©¸ĂĐ¡×éµÄ̉»Î»Í¬Ñ§Í¨¹ư²éÔÄ×ÊÁÏ·¢ÏÖ£¬ÉÏÊöʵÑé¹ư³̀ÖĐn(Mn2+)Ëæʱ¼äµÄ±ä»¯Çé¿öÈçͼËùʾ£¬²¢ÈÏΪỐ³ÉƠâÖֱ仯µÄỘ̉ÊÇ·´Ó¦̀åϵÖеÄijÖÖÁ£×Ó¶ÔKMnO4Óë²ƯËáÖ®¼äµÄ·´Ó¦ÓĐijÖÖ̀ØÊâ×÷ÓĂ£¬Ộ¸Ă×÷ÓĂÊÇ____£¬ÏàÓ¦µÄÁ£×Ó×î¿ÉÄÜÊÇ___(̀îÁ£×Ó·ûºÅ)¡£
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
¡¾̀âÄ¿¡¿̉ÑÖª£º¢Ù1mol¾§̀å¹èÖĐº¬ÓĐ2molSi¡ªSi¼ü¡£
¢ÚSi(s)£«O2(g)===SiO2(g) ¦¤H£¬Æä·´Ó¦¹ư³̀ÓëÄÜÁ¿±ä»¯ÈçͼËùʾ¡£
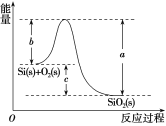
¢Û
»¯Ñ§¼ü | Si¡ªO | O=O | Si¡ªSi |
¶Ï¿ª1 mol¹²¼Û¼üËùĐèÄÜÁ¿/kJ | 460 | 500 | 176 |
ÏÂÁĐ˵·¨ÖĐƠưÈ·µÄÊÇ£¨ £©
A.¾§̀å¹è¹â·ü·¢µçÊǽ«»¯Ñ§ÄÜת»¯ÎªµçÄÜB.¶₫Ñơ»¯¹èÎȶ¨ĐÔĐ¡ÓÚ¹èµÄÎȶ¨ĐÔ
C.¦¤H£½£988kJ¡¤mol£1D.¦¤H£½(a£c)kJ¡¤mol£1
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
¡¾̀âÄ¿¡¿¶̀ÖÜÆÚÖ÷×åÔªËØ![]() µÄÔ×ÓĐ̣ÊửÀ´ÎÔö´ó£¬WÔ×ÓµÄ×îÍâ²ăµç×ÓÊưµÈÓÚYÔ×Ó×îÍâ²ăµç×ÓÊưµÄ2±¶£»ËÄÖÖÔªËØĐγɵÄ̉»ÖÖ»¯ºÏÎïµÄ½á¹¹ÈçͼËùʾ£¬¸Ă»¯ºÏÎïµÄ̉ơÀë×ÓÖĐĂ¿¸öÔ×ÓµÄ×îÍâ²ă¾ùÂú×ă8µç×ÓÎȶ¨½á¹¹£¬ÏÂÁĐ˵·¨´íÎóµÄÊÇ£¨ £©
µÄÔ×ÓĐ̣ÊửÀ´ÎÔö´ó£¬WÔ×ÓµÄ×îÍâ²ăµç×ÓÊưµÈÓÚYÔ×Ó×îÍâ²ăµç×ÓÊưµÄ2±¶£»ËÄÖÖÔªËØĐγɵÄ̉»ÖÖ»¯ºÏÎïµÄ½á¹¹ÈçͼËùʾ£¬¸Ă»¯ºÏÎïµÄ̉ơÀë×ÓÖĐĂ¿¸öÔ×ÓµÄ×îÍâ²ă¾ùÂú×ă8µç×ÓÎȶ¨½á¹¹£¬ÏÂÁĐ˵·¨´íÎóµÄÊÇ£¨ £©

A.Ô×Ӱ뾶£º![]() B.WÓëZĐγɾ§̀åµÄ»ù±¾µ¥ÔªÎªÆ½Ăæ½á¹¹
B.WÓëZĐγɾ§̀åµÄ»ù±¾µ¥ÔªÎªÆ½Ăæ½á¹¹
C.XÓëZÔÚ×ÔÈ»½çÖĐ¾ù²»´æÔÚÓÎÀë̀¬D.WÓëYĐγɵĻ¯ºÏÎï¿É×÷ÄÍ»đ²ÄÁÏ
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
¡¾̀âÄ¿¡¿ÈçͼÔÚ»¯Ñ§ÊµÑéÖĐÓжàÖÖÓĂ;£º
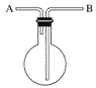
(1)ÏÖÓĂ´Ë×°ÖĂÊƠ¼¯°±Æø£¬Æø̀å´Ó_____¿ÚͨÈ룬ÈôÓĂ´Ë×°ÖĂÊƠ¼¯ÂÈÆø£¬Æø̀å´Ó____¿ÚͨÈë¡£
(2)ÏÖÓĐλͬѧ²ÉÓĂÅÅË®·¨ÊƠ¼¯°±Æø£¬Æä×°ÖĂÈçͼ£º
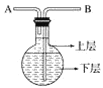
Æø̀å´Ó_______¿ÚͨÈ룬Éϲẳº̀åӦѡÔñ_____¡£
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
¡¾̀âÄ¿¡¿ËÄÂÈ»¯îÑÊÇÖÆÈ¡º£ĂàîѺÍÂÈ»¯·¨îÑ°×(¶₫Ñơ»¯îÑ)µÄÖ÷̉ªÔÁÏ£¬ÓĂÓÚÖÆỐÑƠÁϺÍîÑÓĐ»ú»¯ºÏÎï̉Ô¼°¹ú·ÀÉÏÓõÄÑ̀Ä»¼Á¡£Í¬Ê±̉²ÊÇÖÆÈ¡º½̀́º½¿Ơ¹¤̉µ²ÄÁÏ¡ª¡ªîѺϽđµÄÖØ̉ªÔÁÏ£¬ÓÉîÑ̀ú¿ó(Ö÷̉ª³É·ÖÊÇFeTiO3£¬º¬ÓĐÉÙÁ¿Fe2O3¡¢SiO2¡¢Al2O3µÈÔÓÖÊ)£¬ÖƱ¸TiCl4µÈ²úÆ·µÄ̉»ÖÖ¹¤̉ƠÁ÷³̀ÈçÏ£º

̉ÑÖª£º
¢ñ.¢ÙÖĐ¼ÓÈë̀úĐ¼ÖÁ½₫³ö̉ºÏÔ×ÏÉ«£¬´ËʱÈÜ̉ºÈÔ³ÊÇ¿ËáĐÔ¡£¸Ă¹ư³̀ÖĐÓĐÈçÏ·´Ó¦·¢Éú£º
2Fe3++Fe===3Fe2+¡¢2TiO2+(Î̃É«)+Fe+4H+===2Ti3+(×ÏÉ«)+Fe2++2H2O¡¢Ti3+(×ÏÉ«)+ Fe3++ H2O===2TiO2+(Î̃É«)+ Fe2++2H+£»
¢̣.ËÄÂÈ»¯îѵÄÈÛµă-25.0¡æ£¬·Đµă136.4¡æ£¬SiCl4µÄÈÛµă-68.8¡æ£¬·Đµă57.6¡æ¡£
»Ø´đÏÂÁĐÎỀ⣺
(1)ÓĂÑÎËáËá½₫ʱ£¬ÎªÊ¹Ëá½₫ËÙÂʼӿ́£¬¿É²ÉÈ¡µÄ´ëÊ©ÊÇ£º________________(ÖÁÉÙĐ´2̀ơ)£¬·¢ÉúÖ÷̉ª·´Ó¦µÄÀë×Ó·½³̀ʽΪ£º___________¡£
(2)·ÏÔüµÄ³É·ÖÊÇ_______¡£
(3)ÈçºÎ¼́Ñ鸻º¬TiO2+ÈÜ̉ºÖĐÊÇ·ñ»¹º¬̀úÔªËØ_____________¡£
(4)Èô½«ÖÆµĂµÄ¹̀̀åTiO2¡¤nH2OÓĂËáÇåÏ´³ưÈ¥ÆäÖеÄFe(OH)3ÔÓÖÊ£¬»¹¿ÉÖƵĂîÑ°×·Û¡£̉ÑÖª25¡æʱ£¬Ksp[Fe(OH)3]=4.0¡Á10-38£¬¸ĂζÈÏ·´Ó¦![]() µÄƽºâ³£ÊưK=____¡£
µÄƽºâ³£ÊưK=____¡£
(5)ÉÏÊö¹¤̉Ơ¾ßÓĐ³É±¾µÍ¡¢¿ÉÓõÍƷλ¿óÎïΪÔÁϵÈÓÅµă¡£̉À¾ƯẦÉ«»¯Ñ§ÀíÄ¸Ă¹¤̉ƠÁ÷³̀ÖĐ´æÔڵIJ»×ăÖ®´¦ÊÇ_______(Ö»̉ªÇóĐ´³ö̉»Ïî)¡£
(6)̉ª¾«Öƺ¬ÉÙÁ¿SiCl4ÔÓÖʵÄTiCl4£¬¿É²ÉÓõķ½·¨ÊÇ_______¡£
(7)ÓĂTiCl4Ë®½âÉú³ÉTiO2¡¤nH2O£¬¾¹ưÂË¡¢Ë®Ï´³ưÈ¥ÆäÖеÄCl¡¥£¬ÔÙºæ¸É¡¢±ºÉƠ³ưȥˮ·ÖµĂµ½·Û̀åTiO2£®Đ´³öTiCl4Ë®½âÉú³ÉTiO2¡¤nH2OµÄ»¯Ñ§·½³̀ʽ__________________¡£
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
¡¾̀âÄ¿¡¿Ï±íÖĐÁĐ³öÁË25 ¡æ¡¢101 kPaʱ̉»Đ©ÎïÖʵÄȼÉƠÈÈÊư¾Ư:
ÎïÖÊ | CH4(g) | CH3OCH3(g) | H2(g) | HC¡ÔCH(g) |
ȼÉƠÈÈ/(kJ¡¤mol-1) | 890.3 | 1 453.0 | 285.8 | 1 299.6 |
̉ÑÖª:¢Ù1 mol̉º̀¬Ë®±äΪÆø̀¬Ë®̉ªÎüÊƠ44.0 kJµÄÈÈÁ¿£»
¢Ú¼üÄÜ:C¡ªH¼ü¡¡413.4 kJ¡¤mol-1¡¢H¡ªH¼ü¡¡436.0 kJ¡¤mol-1¡£
ÏÂÁĐĐđÊö´íÎóµÄÊÇ
A. CH3OCH3(g)+3O2(g)£½2CO2(g)+3H2O(l)¡¡¦¤H=-1 453.0 kJ¡¤mol-1
B. C¡ÔC¼üµÄ¼üÄÜΪ786.0 kJ¡¤mol-1
C. 2CH4(g)+O2(g)£½CH3OCH3(g)+H2O(g)¡¡¦¤H=-283.6 kJ¡¤mol-1
D. H2O(g)£½H2O(l)¡¡¦¤H=-44.0 kJ¡¤mol-1
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
¡¾̀âÄ¿¡¿Éè![]() Ϊ°¢·ü¼ÓµÂẪ³£ÊưµÄÖµ¡£ÏÂÁĐĐđÊöƠưÈ·µÄÊÇ( )
Ϊ°¢·ü¼ÓµÂẪ³£ÊưµÄÖµ¡£ÏÂÁĐĐđÊöƠưÈ·µÄÊÇ( )
A.̉ÑÖª![]() £»
£»![]() ½«2NA¸öCOÓëNA¸öO2»́ºÏ³ä·Ö·´Ó¦·Å³öakJµÄÈÈÁ¿
½«2NA¸öCOÓëNA¸öO2»́ºÏ³ä·Ö·´Ó¦·Å³öakJµÄÈÈÁ¿
B.t¡æʱ£¬1LpH=6µÄ´¿Ë®ÖĐº¬OH¡¥ÊưΪ10-6NA
C.±ê×¼×´¿öÏ£¬2.24L¼×´¼ÖĐº¬ÓĐC-H¼üµÄÊưĿΪ0.3NA
D.1L0.1mol/LµÄÇâµâËáÖĐº¬µâ»¯Çâ·Ö×ÓÊưΪ0.1NA
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
¡¾̀âÄ¿¡¿Ä³Ñ§Ï°Đ¡×é̀½¾¿°±µÄ»¹ÔĐÔ¼°¼́Ñé²úÎïµÄĐÔÖÊ£¬°´ÏÂͼװÖĂ½øĐĐʵÑé(ͼÖĐ¼Đ³Ö×°ÖẲÑÂÔÈ¥)¡£½«B´¦µÄÈưÑơ»¯¶₫¸ơ¼ÓÈÈÖÁº́ÈÈ£¬ÔÙ¹ÄÈë¿ƠÆø£¬̉ÑÖª£ºÎ̃Ë®ÂÈ»¯¸Æ¿ÉÎüÊƠ°±ÆøºÍË®¡£»Ø´đÏÂÁĐÎỀ⣺
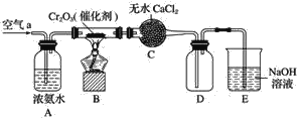
(1)BÖĐ·¢Éú·´Ó¦µÄ»¯Ñ§·½³̀ʽÊÇ________________________________¡£
(2)Ö¤Ă÷°±Æø·¢ÉúÁË´ß»¯Ñơ»¯µÄÏÖÏóÊÇ____________________________¡£
(3)Đ´³ö(2)ÖĐ·´Ó¦µÄ»¯Ñ§·½³̀ʽ______________________¡£
(4)×°ÖĂE×÷ÓĂÊÇ________________________________________¡£
²é¿´´đ°¸ºÍ½âÎö>>
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com