
【题目】氢气是未来最理想的能源.科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O ![]() 2H2↑+O2↑.制得的氢气可用于燃料电池.试回答下列问题:
2H2↑+O2↑.制得的氢气可用于燃料电池.试回答下列问题:
(1)分解海水时,实现了从光能转化为能.生成的氢气用于燃料电池时,实现了化学能转化为能.分解海水的反应属于反应(填“放热”或“吸热”).
(2)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,A、B两极上发生的电极反应分别为 A极:2H2+2O2﹣﹣4e﹣═2H2O,则A极是电池的极,电子从该极(填“流入”或“流出”).B极电极反应式 .
科目:高中化学 来源: 题型:
【题目】在反应H2S+H2SO4(浓)=S↓+SO2↑+2H2O中,若有32g硫生成则转移电子为( )
A.6 molB.2 molC.3 molD.4 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关Al与NaOH溶液反应的说法中,正确的是( )
A.铝是还原剂,其氧化产物是NaAlO2
B.NaOH是氧化剂,其还原产物是H2
C.Al是还原剂,H2O和NaOH都是氧化剂
D.水是氧化剂,铝被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
T | M层上有6个电子 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
Z | 元素最高正价是+7价 |
W | 其单质既能跟酸反应,又能跟碱反应,都产生H2 |
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是 .
(2)元素Y与氢元素形成一种离子YH4+ , 写出该微粒的化学式:(用元素符号表示).
(3)元素Z与元素T相比,非金属性较强的是(用元素符号表示),下列表述中能证明这一事实的是 . ①常温下Z的单质和T的单质状态不同
②Z的氢化物比T的氢化物稳定
③一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一.T、X、Y、Z四种元素的最高价氧化物对应的水化物中化学性质明显不同于其他三种的是(填化学式),理由是 . Z的最高价氧化物对应的水化物与W的最高价氧化物对应的水化物反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某硫酸工业废渣的主要成分为SiO2、MgO、Al2O3、Fe2O3等。回收废渣中金属元素的工艺流程如下:
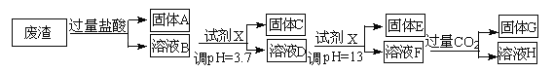
已知常温条件下:
①阳离子以氢氧化物形式开始沉淀和恰好完全沉淀(阳离子浓度等于10-5mol·L-1 )时的pH 如下表所
示。
阳离子 | Fe3+ | Al3+ | Mg2+ |
开始沉淀时的pH | 1.9 | 3.7 | 9.6 |
恰好完全沉淀时的pH | 3.2 | 5.2 | 11.0 |
②饱和氨水溶液中c(OH-)约为1×10-3mol·L-1。
请回答下列问题:
(1)固体C为_________(填化学式)。
(2)上述流程中两次使用试剂X,试剂X是_________(填“氨水”或“氢氧化钠”),其理由是_________________。
(3)溶液D→固体E的过程中需要控制溶液pH=13,如果pH过小,可能导致的后果是________________。
(4)写出溶液F→溶液H 的离子方程式:__________________。
(5)Ksp[Mg (OH )2]=_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】各物质之间的转化关系如图,部分生成物省略.C、D是由X、Y、Z中两种元素组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10.D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷线路板.请回答下列问题:
(1)G元素在周期表中的位置 , C的电子式 .
(2)比较Y与Z的原子半径大小>(填写元素符号).
(3)写出E和乙醛反应的化学反应方程式(有机物用结构简式表示);反应类型: .
(4)写出实验室制备G的离子反应方程式 .
(5)气体D与NaOH溶液反应可生成两种盐P和Q,在P中Na的质量分数为43%,其俗名为 .
(6)实验室中检验L溶液中的阳离子常选用溶液,现象是 .
(7)A中包含X、Y、Z元素,A的化学式为
(8)研究表明:气体D在一定条件下可被还原为晶莹透明的晶体N,其结构中原子的排列为正四面体,请写出N及其1种同素异形体的名称、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫有多种含氧酸,亚硫酸(H2SO3)、硫酸(H2SO4)、焦硫酸(H2SO4SO3)、硫代硫酸(H2S2O3)等等,在工业上有广泛的应用.它们对应的钠盐同样也是重要的化工产品.
(1)(一).硫代硫酸钠(Na2S2O3)可用做分析试剂及鞣革的还原剂,它受热、遇酸易分解.工业上常利用含硫废水生产Na2S2O35H2O,实验室可用如下装置(略去部分加持仪器)模拟生成过程.
烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq) (Ⅰ)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l) (Ⅱ)
S(s)+Na2SO3(aq) ![]() Na2S2O3(aq) (Ⅲ)
Na2S2O3(aq) (Ⅲ)
①烧瓶A中发生反应的离子方程式为: . 装置D的作用是 .
②装置B的作用之一是观察SO2的生成速率,其中的液体最好选择 .
a.蒸馏水 b.饱和Na2SO3溶液c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
③反应后期可用酒精灯适当加热烧瓶A,实验室用酒精灯加热时必须使用石棉网的仪器还有 .
a.烧杯 b.蒸发皿 c.试管 d.锥形瓶
④为了保证硫代硫酸钠的产量,实验中通入SO2不能过量,原因是 .
(2)(二)焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一.Na2S2O5溶于水即生成NaHSO3 . ①证明NaHSO3溶液中HSO3﹣的电离程度大于水解程度,可采用的实验方法是(填序号).
a.测定溶液的pH b.加入Ba(OH)2溶液c.加入盐酸d.加入品红溶液 e.用蓝色石蕊试纸检测
②葡萄酒常用Na2S2O5作抗氧化剂.测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:
葡萄酒样品100.00mL ![]() 馏分
馏分 ![]() 溶液出现蓝色且30s内不褪色
溶液出现蓝色且30s内不褪色
方程式为SO2+I2+2H2O=H2SO4+2HI)按上述方案实验,消耗标准I2溶液25.00mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为gL﹣1 . 上述实验过程中,若有部分HI被空气氧化,则测得结果(填“偏高”“偏低”或“不变”).其原因是(用化学方程式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识完成题目:
(1)下列物质含有离子键的是
A.H2
B.CO2
C.NH3
D.NaOH
(2)下列物质中含有共价键的离子化合物是
A.H2O
B.CaCl2
C.NH4Cl
D.HCl
(3)NaCl、NH3的电子式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活息息相关。下列说法错误的是
A.喝下汽水后常会打嗝,说明气体的溶解度随温度升高而减小
B.自行车钢架生锈主要是电化学腐蚀所致
C.可以通过灼烧的方法鉴别锦纶和蚕丝
D.凡是有食品添加剂的食物对人体健康均有害,不可食用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com