
【题目】用已准确称量过的氯化钠固体配制1.00 mol·L-1的氯化钠溶液0.5 L,要用到的仪器是( )
①500 mL容量瓶 ②试管 ③烧瓶 ④胶头滴管 ⑤烧杯
⑥玻璃棒 ⑦托盘天平 ⑧药匙
A.①④⑤⑥
B.①②④⑤
C.①④⑤⑥⑦⑧
D.全部
科目:高中化学 来源: 题型:
【题目】在一体积可变的密闭容器中,加入一定量的X、Y、Z,发生反 应mX(g) ![]() nY(g)+pZ(s) △H = Q kJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如表所示:
nY(g)+pZ(s) △H = Q kJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如表所示:
下列说法正确的是( )
气体体积/L c(Y)/molL-1 温度/℃ | 1 | 2 | 3 |
100 | 1.00 | 0.75 | 0.53 |
200 | 1.20 | 0.90 | 0.63 |
300 | 1.30 | 1.00 | 0.70 |
A.m>n+p
B.Q<0
C.温度不变,压强增大,Y的体积分数减少
D.体积不变,温度升高,平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)对于下列反应:2SO2+O2![]() 2SO3, 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么用SO2浓度变化来表示的化学反应速率为 ,用O2浓度变化来表示的反应速率为 。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)=0.5mol/(L·min),那么2min末SO2的浓度为 。
2SO3, 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么用SO2浓度变化来表示的化学反应速率为 ,用O2浓度变化来表示的反应速率为 。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)=0.5mol/(L·min),那么2min末SO2的浓度为 。
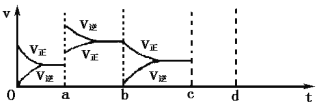
(2)下图左表示在密闭容器中反应:2SO2+O2![]() 2SO3 H<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,ab过程中改变的条件可能是 ;bc过程中改变的条件可能是 ;将增大压强时反应速率变化情况画在c—d处。
2SO3 H<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,ab过程中改变的条件可能是 ;bc过程中改变的条件可能是 ;将增大压强时反应速率变化情况画在c—d处。
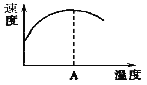
(3)酶是蛋白质,具有蛋白质的特性,酶能催化很多化学反应,上图右表示酶参加的反应中温度与反应速率的关系,解释曲线变化原因 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容密闭容器中,下列说法不能表明反应A(s)+2B(g)![]() C(g)+D(g)已达平衡的是( )
C(g)+D(g)已达平衡的是( )
A.B的物质的量浓度 B.混合气体的压强不变
C.混合气体的密度 D.混合气体的相对分子质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一固定容积的密闭容器中充入2molA和1molB,发生反应2A(g)+B(g)![]() xC(g),达到平衡后,C的体积分数为W%。若维持容器体积和温度不变,按0.6molA、0.3molB、1.4molC为起始物质,达到平衡后,C的体积分数也为W%,则x值为( )
xC(g),达到平衡后,C的体积分数为W%。若维持容器体积和温度不变,按0.6molA、0.3molB、1.4molC为起始物质,达到平衡后,C的体积分数也为W%,则x值为( )
A.1 B.2 C.3 D.2或3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是四位同学在学习“化学反应的速率和化学平衡”一章后,联系工业生产实际所发表的观点,你认为不正确的是
A.使用催化剂,可加快反应速率,目的是提高生产效率
B.使用冰箱保存食物,是利用了化学反应速率理论
C.化学反应速率理论是研究怎样提高原料转化率
D.化学平衡理论是研究怎样使用有限原料多出产品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化肥或农药的说法不正确的是( )
A.施用农药时要注意安全,以防中毒
B.化肥对提高农作物产量具有重要作用,应尽量多施用
C.复合肥料能同时供给作物几种养分,肥效高
D.长期施用硫酸铵、硫酸钾会使土壤酸化、板结
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列物质:CO2、N2、CaCl2、NH4Cl、NaOH、H2O2、Na2O2。
(1)属于共价化合物的有_______________,含有非极性键的离子化合物的是__________。
(2)N2、CO2的结构式分别为________________、_________________。
(3)分别写出NaOH、H2O2、Na2O2的电子式:_______________、_____________、______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下图所示两个装置的叙述中不正确的是
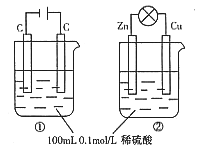
A.c(H+)浓度变化:①减小,②减小
B. 装置名称:①是电解池,②是原电池
C.离子移动方向:①中H+向阴极方向移动,②中H+向正极方向移动
D. 电极反应式:①中阳极:2H2O-4e-=4H++O2↑,②中负极中![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com