
【题目】固体粉末X中可能含有Cu、FeO、Fe2O3、NaHCO3、Na2CO3、Na2S2O3、NaAlO2中的若干种。某化学兴趣小组为确定该固体粉末的成分,现取X进行连续实验,实验过程及现象如下:
已知:HCO3-+AlO2-+H2O=Al(OH)3↓+CO32-下列说法正确的是( )
A. 气体乙和气体丙都为纯净物
B. 固体粉末X中一定含有FeO、Na2S2O3、NaAlO2 ,可能含有NaHCO3、Na2CO3
C. 溶液丁中的阳离子一定只含H+、Fe2+
D. 溶液甲中一定含有AlO2- ,可能含有CO32-
【答案】D
【解析】
固体X加水后,得到固体甲和溶液甲,固体甲中加入足量稀盐酸得到溶液丁,无固体剩余,由于 Cu不溶于稀盐酸,则有两种情况:①固体X中不含Cu ;②固体X中Fe2O3含量较多,溶于盐酸后生成Fe3+再与Cu 反应将其溶解。溶液丁加入酸性KMnO4溶液后,紫红色褪去,则溶液中一定含有Fe2+,可能含有Fe3+,故固体X中一定含有FeO,可能含有Fe2O3和Cu。溶液乙中含有过量的盐酸,加入过量(NH4)2CO3后会生成沉淀和气体,酸性条件下气体不可能是NH3,故气体丙是CO2,根据沉淀丙,推测是CO32-与H+结合生成 HCO3-, Al3+与HCO3-发生双水解,故溶液甲中含有AlO2- ,固体X中含有NaAlO2;由于AlO2-和 HCO3-在水溶液中就会发生反应,故固体X不含NaHCO3。溶液甲加入足量稀盐酸后,会生成沉淀和可使澄清石灰水气体变浑浊的气体(CO2或SO2),由于AlO2-与足量稀盐酸反应无沉淀生成,则溶液中必定含有S2O32-,可能含有CO32-,故固体X一定含有Na2S2O3,可能含有Na2CO3。
A项,气体乙可能是SO2气体,也可能CO2、SO2的混合气体,气体丙是CO2气体,故A项错误;
B项,由以上分析知固体粉末X中一定含有FeO、Na2S2O3、NaAlO2 ,可能含有 Na2CO3、Fe2O3,故B项错误;
C项,溶液丁中的阳离子一定含H+、Fe2+,可能含有Fe3+,故C项错误;
D项,由以上分析可知溶液甲中一定含有AlO2-,可能含有CO32-,故D项正确;
综上所述,本题选D。


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
【题目】世界上最旱发现并使用锌的是中国,明朝末年《天工开物》一书中有世界上最早的关于炼锌技术的记载。回答下列问題:
(1)基态Zn原子的核外电子所占据的最高能层符号为_____________,Zn2+基态核外电子排布式为_______________________。
(2)硫酸锌溶于过量的氨水可形成[Zn(NH3)4]SO4溶液。
①[Zn(NH3)4]SO4中阴离子的空间构型为 _____________(用文字描述);
②SO42-中,中心原子的轨道杂化类型为______________;
③写出一种与SO42-互为等电子体的分子的化学式_____________;
④NH3极易溶于水,除因为它们都是极性分子外,还因为_______________________。
(3)Zn与S所形成化合物晶体的晶胞如图所示。
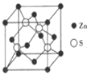
①该化合物的化学式为___________;
②已知该晶体的晶胞参数a=541 pm,其密度为___________g·cm-3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某离子晶体的晶胞示意图如下图所示,其摩尔质量为M g·mol-1,阿伏加德罗常数的值为NA,晶体的密度为d g·cm-3。

下列说法中正确的是
A. 晶体晶胞中阴、阳离子的个数都为1
B. 晶体中阴、阳离子的配位数都是4
C. 该晶胞可能是NaCl的晶胞
D. 该晶体中两个距离最近的阳离子的核间距为M/d cm
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于Na2O2的叙述不正确的是( )
A.1 mol Na2O2与足量CO2反应转移的电子为1 mol
B.将10 g H2和CO的混合气体充分燃烧,将生成物(H2O、CO2)通入足量的Na2O2固体中充分反应,固体增重为10 g
C.将Na2O2投入FeSO4溶液中生成红褐色沉淀
D.将等物质的量的NaHCO3和Na2O2混合后,在密闭容器中充分加热排除气体后剩余固体为Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于放热反应COCl2(g) ![]() CO(g) + Cl2(g)。当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是( )
CO(g) + Cl2(g)。当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是( )
A. ①②④B. ④⑥C. ②③⑤D. ③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将Na2O2逐渐加入到含有H+、Mg2+、Al3+、NH4+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入的Na2O2物质的量(mol)的关系如图所示,则原溶液中的Mg2+、Al3+、NH4+物质的量分别为

A. 2 mol、3 mol、6 mol B. 3 mol、2 mol、6mol
C. 2 mol、3 mol、4 mol D. 3 mol、2 mol、2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学用语的表示方法中错误的是
A. 次氯酸的电子式: ![]()
B. M2+离子核外有 a个电子,b个中子,M 原子符号为a+b+2a+2M
C. 用电子式表示MgCl2 的形成过程为 ![]()
D. Na+的结构示意图:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】解释下列事实的方程式不正确的是
A. 纯碱溶液遇酚酞变红:CO32-+H2O![]() HCO3-+OH-
HCO3-+OH-
B. 以石墨为电极电解MgCl2溶液:2Cl-+2H2O ![]() Cl2↑+H2↑+20H-
Cl2↑+H2↑+20H-
C. 纯碱溶液处理锅炉中的水垢:CaSO4(s)+CO32-(aq)![]() CaCO3(s)+SO42-(aq)
CaCO3(s)+SO42-(aq)
D. 在Fe(NO3)2溶液中加稀硫酸有气体产生:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com