
【题目】实验室以一种工业废渣(主要成分为MgCO3、Mg2SiO4和少量Fe、Al的氧化物)为原料制备MgCO3·3H2O。实验过程如如:
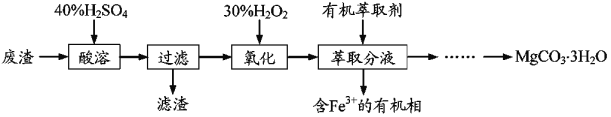
(1)酸溶过程中主要反应的热化学方程式为
MgCO3(s)+2H+(aq)=Mg2+(aq)+CO2(g)+H2O(l) ΔH=-50.4kJ·mol–1
Mg2SiO4(s)+4H+(aq)=2Mg2+(aq)+H2SiO3(s)+H2O(l) ΔH=-225.4kJ·mol–1
酸溶需加热的目的是__;所加H2SO4不宜过量太多的原因是__。
(2)加入H2O2氧化时发生发应的离子方程式为__。
(3)用如图所示的实验装置进行萃取分液,以除去溶液中的Fe3+。
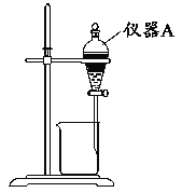
①实验装置图中仪器A的名称为__。
②为使Fe3+尽可能多地从水相转移至有机相,采取的操作:向装有水溶液的仪器A中加入一定量的有机萃取剂,__、静置、分液,并重复多次。
(4)请补充完整由萃取后得到的水溶液制备MgCO3·3H2O的实验方案:边搅拌边向溶液中滴加氨水,___,过滤、用水洗涤固体2~3次,在50℃下干燥,得到MgCO3·3H2O。
【答案】加快酸溶速率 避免制备MgCO3时消耗更多的碱 H2O2+2Fe2++2H+=2Fe3++2H2O 分液漏斗 充分振荡 至5.0<pH<8.5,过滤,边搅拌边向滤液中滴加Na2CO3溶液至有大量沉淀生成,静置,向上层清液中滴加Na2CO3溶液,若无沉淀生成
【解析】
工业废渣(主要成分为MgCO3、Mg2SiO4和少量Fe、Al的氧化物)加入硫酸反应生成硫酸镁、硅酸、硫酸亚铁、硫酸铝等,过滤,向滤液中加入双氧水,主要目的是氧化亚铁离子为后续除杂,加入有机萃取剂萃取分液,有机相中含有铁离子,分液后溶液中先加氨水除铝离子,过滤,滤液中加入碳酸钠溶液得到碳酸镁沉淀。
(1)酸溶需加热的目的是加快酸溶速率,酸溶时生成硫酸镁,经过一系列反应最终变为MgCO3·3H2O,H2SO4过多,再后续反应过程中会需要大量碱来中和过量的硫酸,因此所加H2SO4不宜过量太多的原因是避免制备MgCO3时消耗更多的碱;故答案为:加快酸溶速率;避免制备MgCO3时消耗更多的碱。
(2)加入H2O2氧化时主要发生亚铁离子被双氧水氧化生成铁离子,发生发应的离子方程式为H2O2+2Fe2++2H+=2Fe3++2H2O;故答案为:H2O2+2Fe2++2H+=2Fe3++2H2O。
(3)①实验装置图中仪器A的名称为分液漏斗;故答案为:分液漏斗。
②为使Fe3+尽可能多地从水相转移至有机相,一般采取少量多次萃取,为充分萃取需要充分振荡;故答案为:充分振荡。
(4)萃取后得到的水溶液,边搅拌边向溶液中滴加氨水,滴加到一定pH值后,生成氢氧化铝沉淀,过滤,边搅拌边向滤液中滴加Na2CO3溶液至有大量沉淀生成碳酸镁,静置,向上层清液中滴加Na2CO3溶液,若无沉淀生成,过滤、用水洗涤固体2~3次,在50℃下干燥,得到MgCO3·3H2O;故答案为:至5.0<pH<8.5,过滤,边搅拌边向滤液中滴加Na2CO3溶液至有大量沉淀生成,静置,向上层清液中滴加Na2CO3溶液,若无沉淀生成。


科目:高中化学 来源: 题型:
【题目】配制500mL 0.100 mol·Lˉ1的NaCl溶液,部分实验操作示意图如下:
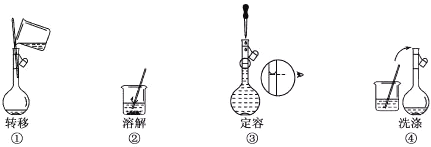
下列说法正确的是
A. 实验中需用的仪器有:天平、250mL容量瓶、烧杯、玻璃棒、胶头滴管等
B. 上述实验操作步骤的正确顺序为①②④③
C. 容量瓶需要用自来水、蒸馏水洗涤,干燥后才可用
D. 定容时,仰视容量瓶的刻度线,使配得的NaCl溶液浓度偏低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应能用离子方程式2H+ + CO32-=CO2↑ + H2O表示的是
A.HCl溶液与MgCO3反应
B.CH3COOH与K2CO3溶液反应
C.HNO3溶液与NaHCO3溶液反应
D.H2SO4溶液与(NH4)2CO3溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雌二醇的结构简式如图,下列说法不正确的是
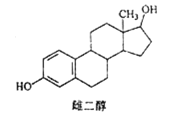
A. 能与 Na、NaOH溶液、Na2CO3溶液反应
B. 能发生加成反应、取代反应、消去反应
C. 该分子中所有碳原子不可能在同一个平面内
D. 可与 FeC13溶液发生显色反应,但不能发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)3.01×1023个NH4+含有质子的物质的量是______mol,含有电子的物质的量是______mol。
(2)200mL 2mol/L的Al2(SO4)3 溶液中SO42-的物质的量浓度为_________。
(3)标准状况下36g H2和O2组成的混合气体的体积是67.2L 。求这种混合气体中H2和O2的体积比为____________。
(4)同温同压下,质量比为17:48的NH3和CH4两种气体,密度之比为_________。
(5)已知1.505×1023个A气体分子质量为31g ,则A气体的摩尔质量是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2O5是一种新型硝化剂,在一定温度下可发生如下反应:2N2O5(g)![]() 4NO2(g) + O2(g) △H >0。T1温度时,向密闭容器中通入N2O5气体,部分实验数据见下表:
4NO2(g) + O2(g) △H >0。T1温度时,向密闭容器中通入N2O5气体,部分实验数据见下表:
时间/s | 0 | 500 | 1000 | 1500 |
c(N2O5)/(mol·L-1) | 5.00 | 3.52 | 2.50 | 2.50 |
下列说法正确的是
A.500 s内NO2的生成速率为2.96×10-3mol·L-1·s-1
B.T1温度下该反应平衡时N2O5的转化率为29.6%
C.达到平衡后,其他条件不变,将容器的体积压缩到原来的1/2,则c(N2O5)﹤5.00mol/L
D.T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1>K2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W 均为常见短周期非金属元素,常温下,其最简单氢化物水溶液(浓度均为0.01 mol/L)的 pH 和原子半径的关系如图所示。其中 X 为氧元素。下列有关说法正确的是
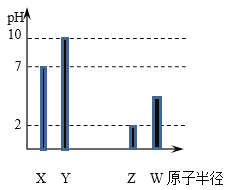
A.Y 是钠元素
B.图中 Y 的氢化物不能与X 的氢化物反应
C.Z 的最高价氧化物对应水化物的化学式为 HClO4
D.W 的最高价氧化物对应水化物是弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】萜类化合物广泛存在于动植物体内,关于下列萜类化合物的说法正确的是( )
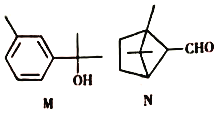
A. M和N互为同分异构体
B. M分子中所有碳原子均处于同一平面上
C. N与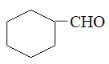 属于同系物
属于同系物
D. M和N均能使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
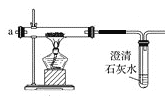
【题目】某研究性学习小组类比镁在二氧化碳中的燃烧反应,认为钠和二氧化碳也可以发生反应,他们对钠在CO2气体中燃烧进行了下列实验:
(1)若用下图装置制备CO2,则发生装置中反应的离子方程式为_________。
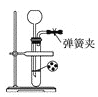
(2)将制得的CO2净化、干燥后由a口缓缓通入下图装置,待装置中的空气排净后点燃酒精灯,观察到玻璃直管中的钠燃烧,火焰为黄色。待冷却后,管壁附有黑色颗粒和白色物质。
①能说明装置中空气已经排净的现象是_________。
②若未排尽空气就开始加热,则可能发生的化学反应方程式主要为_________。
(3)若钠着火,可以选用的灭火物质是_________。
A.水 B.泡沫灭火剂 C.干沙土 D.二氧化碳
(4)该小组同学对管壁的白色物质的成分进行讨论并提出假设:
Ⅰ.白色物质可能是Na2O; Ⅱ.白色物质可能是Na2CO3; Ⅲ.白色物质还可能是_________。
(5)为确定该白色物质的成分,该小组进行了如下实验:
实验步骤 | 实验现象 |
①取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加过量的CaCl2溶液 | 出现白色沉淀 |
②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
①通过对上述实验的分析,你认为上述三个假设中,___成立(填序号)。
②由实验得出:钠在CO2中燃烧的化学方程式为_____;每生成1mol氧化产物,转移的电子数为____。
(6)在实验(2)中还可能产生另一种尾气,该气体为________;处理该尾气的方法为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com