
����Ŀ������������Ԫ��X��Y��Z��W��ԭ������������������Ԫ���γɵĵ�������Ϊm��n��p��q��r��t��u����ЩԪ����ɵĶ�Ԫ���������uΪ�γ��������Ҫ����֮һ��25��ʱ��0.01mol��L-1��v��Һ�У�c��OH-��/c��H+��=1.0��1010���������ʵ�ת����ϵ��ͼ��ʾ������˵����ȷ����
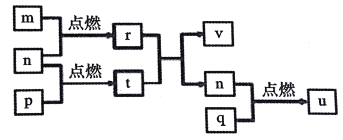
A. ԭ�Ӱ뾶�Ĵ�С��W>Z>Y>X
B. Z�ֱ���Y��W��ɵĻ������л�ѧ�����Ϳ�����ͬ
C. v������ˮ�ĵ����u�ܴٽ�ˮ�ĵ���
D. ճ��q���Թܿ��þƾ�ϴ��
���𰸡�B
������������������Ԫ��X��Y��Z��W��ԭ������������������Ԫ���γɵĵ�������Ϊm��n��p��q��r��t��u����ЩԪ����ɵĶ�Ԫ���������uΪ�γ��������Ҫ����֮һ����u��SO2������W��S��Y��O����n��������25��ʱ��0.01mol��L-1��v��Һ�У�c��OH-��/c��H+��=1.0��1010��������������Ũ����0.01mol/L������v���������ƣ���X��H��Z��Na��m��������r��H2O��p��Na��t�ǹ������ƣ�A. ͬ������������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶��������ԭ�Ӱ뾶�Ĵ�С��Z>W>Y>X��A������B. Na�ֱ���O��S������ɻ�����Na2O2��Na2S2����ѧ��������ͬ��B��ȷ��C.�������ƺ�SO2��ˮ��Һ��������ˮ�ĵ��룬C����D. ճ��S���Թܿ���CS2ϴ�ӣ�S���ھƾ���D����ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͬ��ͬѹ�£���ͬ�����CO2��NO�������壬���ߵ����ʵ����ı�Ϊ_________���ܶ�֮��Ϊ___________��������֮��Ϊ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�����һ��ԭ��ء��Իش���������(���ݹ��ʺ���)��

(1)�������ҺΪϡ����ʱ������________ (��������������������a�⣬���������b��)��
a��������������Mg�缫�Ϸ����ķ�ӦΪ______________��Al�缫�Ϸ����ķ�ӦΪ________________________________________________________________________��
(2)�������ҺΪNaOH��Һʱ������________ (��������������������a�⣬���������b��)��
a������������Al�缫�Ϸ����ķ�ӦΪ________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����֪����2Fe��s��+O2��g��=2 FeO��s����H1=��544.0kJmol��1��
��4Al��s��+3O2��g���T2Al2O3��s����H2=��3351.4kJmol��1��
Al��FeO�������ȷ�Ӧ���Ȼ�ѧ����ʽ��
��2����Ӧ�����������Ϊ��̬��ij���淴Ӧ�ڲ�ͬ�����µķ�Ӧ���̷ֱ�ΪA��B����ͼ��ʾ��
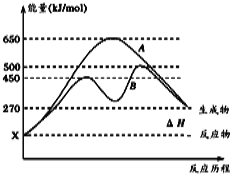
�پ�ͼ�жϸ÷�Ӧ�� ��������š����ȷ�Ӧ������Ӧ�ﵽƽ��������������䣬�����¶ȣ��淴Ӧ���ʽ� �����������С�����䡱����
������B���̱����˷�Ӧ���õ�����Ϊ ������ĸ����
A�������¶� B������Ӧ���Ũ��
C�������¶� D��ʹ�ô���
��3����֪�Ȼ�ѧ����ʽ��2H2��g��+O2��g��=2H2O��g����H=��483.6kJmol��1���÷�Ӧ�Ļ��Ϊ334.4kJmol��1�������淴Ӧ�Ļ��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������������ȷ������ ��
A��1 L 0.1 mol��L-1��CuCl2��Һ�к�Cu2+Ϊ0.1NA
B����״���£�22.4 L CCl4��CCl4����ΪNA
C��1mol H3O+��������Ϊ10 NA
D��1molNa2O��Na2O2������к������ӵ�����ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з���ʽ��д��ȷ����
����NaAlO2��Һ��ͨ�������CO2��2AlO2-+3H2O+CO2=2Al��OH��3��+CO32-
��������KMnO4��Һ�еμ�����H2C2O4��Һ��ԭ��Һ��ɫ��ȥ��2MnO4-+5H2C2O4=2Mn2-+10CO2��+2H2O+6OH-
��̼��ĵ��뷽��ʽ��H2CO3![]() 2H++CO32-
2H++CO32-
��NaClO��Һ��CIO-��ˮ�⣺CIO-+H2O=HClO+OH-
�����������£���H2O2��I-����ΪI2��H2O2+2I-+2H+=I2+2H2O
����NaHSO4��Һ�еμ�Ba��OH��2��Һ����Һ�����ԣ�H++SO42-+Ba2++OH-=BaSO4��+H2O
A. 1�� B. 2�� C. 3�� D. 4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ����һ����CO2�������״�ȼ�ϵķ�����CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g); ��H=-49.0kJ/mol��ij�¶��£���6molCO2��8molH2����2L���ܱ������У����H2�����ʵ�����ʱ��仯��ͼʵ����ʾ��ʵ�ߣ���ͼ������a��1,6����ʾ����1minʱH2�����ʵ�����6mol��
CH3OH(g)+H2O(g); ��H=-49.0kJ/mol��ij�¶��£���6molCO2��8molH2����2L���ܱ������У����H2�����ʵ�����ʱ��仯��ͼʵ����ʾ��ʵ�ߣ���ͼ������a��1,6����ʾ����1minʱH2�����ʵ�����6mol��
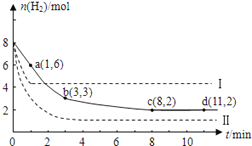
��1����һ������H2��ƽ����Ӧ������________��ʽ��������¶��µĻ�ѧƽ�ⳣ��K=______
��2������ʱ���ƽ����Ӧ����������_______
A.0-1min B.1-3min C.3-8min D.8-11min
��3�����ı�ijһʵ�������ٽ�������ʵ����H2�����ʵ�����ʱ��仯��ͼ��������ʾ������I��Ӧ��ʵ�������ı���__________�����ߢ��Ӧ��ʵ�������ı����_____________��
��4������d��ʱ����ϵ�ڳ���2molCO2��2molH2O����ʱV��_____V�������ڣ�С�ڣ����ڣ�
��5����֪��
��CO(g)+1/2O2(g)=CO2(g); ��H1=-283.0kJ/mol
��H2(g)+1/2O2(g)=H2O(g); ��H2=-241.8kJ/mol
��CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g); ��H3=-192.2kJ/mol
�ڹ�ҵ�ϳ���CO��H2�ϳɼ״����÷�Ӧ���ȷ���ʽΪ_____________
��6����ͼ�Ǽ״�ȼ�ϵ��ԭ��ʾ��ͼ���ش��������⣺��ظ����ĵ缫��Ӧ�ǣ�__________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(CeO2)��һ����Ҫ��ϡ�������ƽ�������ʾ�����������в��������ķϲ�����ĩ����SiO2��Fe2O3��CeO2��FeO�����ʣ���ij�������Դ˷�ĩΪԭ�ϣ�������¹������̶���Դ���л��գ��õ�������CeO2��������茶��塣
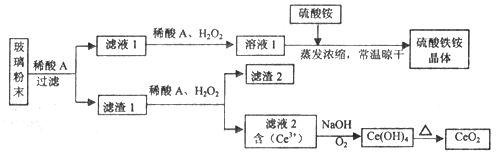
��֪��CeO2������ϡ���ᣬҲ������NaOH��Һ��
(1)ϡ��A�ķ���ʽ��_____________________��
(2)��Һ1�м���H2O2��Һ��Ŀ����__________________��
(3)���ʵ��֤����Һ1�к���Fe2+_____________________��
(4)��֪Fe2+��Һ���Ժ�������ˮ��FeO(OH)��Ӧ����Fe3O4,��д�÷�Ӧ�����ӷ���ʽ____________��
(5)����Һ2����Ce(OH)4�����ӷ���ʽ__________________��
(6)������茶���[Fe2(SO4)3��2(NH4)2SO4��3H2O]�㷺����ˮ�ľ���������������ȥ�����Է�ˮ�е�������ʱЧ�ʽ�������ԭ����___________________��
(7)ȡ���������еõ���Ce(OH)4��Ʒ0.531 g���������ܽ����Ũ��Ϊ0.l000mol��L-1FeSO 4����Һ�ζ����յ�ʱ���汻��ԭΪCe3+ )������25.00 mL����Һ���ò�Ʒ��Ce(OH)4�����÷���Ϊ_______(���������λ��Ч����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ֻ������ͷ�Ӧ��һ������������ԭ��Ӧ���ǣ� ��
A.���ֽⷴӦ
B.�ֽⷴӦ
C.���Ϸ�Ӧ
D.�û���Ӧ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com