
����Ŀ����1����֪����2Fe��s��+O2��g��=2 FeO��s����H1=��544.0kJmol��1��
��4Al��s��+3O2��g���T2Al2O3��s����H2=��3351.4kJmol��1��
Al��FeO�������ȷ�Ӧ���Ȼ�ѧ����ʽ��
��2����Ӧ�����������Ϊ��̬��ij���淴Ӧ�ڲ�ͬ�����µķ�Ӧ���̷ֱ�ΪA��B����ͼ��ʾ��
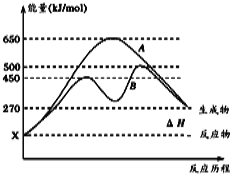
�پ�ͼ�жϸ÷�Ӧ�� ��������š����ȷ�Ӧ������Ӧ�ﵽƽ��������������䣬�����¶ȣ��淴Ӧ���ʽ� �����������С�����䡱����
������B���̱����˷�Ӧ���õ�����Ϊ ������ĸ����
A�������¶� B������Ӧ���Ũ��
C�������¶� D��ʹ�ô���
��3����֪�Ȼ�ѧ����ʽ��2H2��g��+O2��g��=2H2O��g����H=��483.6kJmol��1���÷�Ӧ�Ļ��Ϊ334.4kJmol��1�������淴Ӧ�Ļ��Ϊ ��
���𰸡���1��2Al��s��+3FeO��s���TAl2O3��s��+3Fe��s����H=��859.7 kJmol��1
��2����������������D����3��818.0 kJmol��1
��������
�����������1����֪����2Fe��s��+O2��g��=2 FeO��s����H1=��544.0kJmol��1����4Al��s��+3O2��g���T2Al2O3��s����H2=��3351.4kJmol��1�����ݸ�˹���ɣ�����-����3����2��2Al��s��+3FeO��s���TAl2O3��s��+3Fe��s����H=��859.7 kJmol��1��
��2���پ�ͼ�ж���Ӧ����е�������������������ͣ��÷�Ӧ�����ȷ�Ӧ������Ӧ�ﵽƽ��������������䣬�����¶ȣ������淴Ӧ���ʽ�������������B���������˷�Ӧ�Ļ�ܣ��˷�Ӧ���õ�����Ϊʹ�ô�����ѡD��
��3����ѧ��Ӧ���ʱ��������Ӧ�Ļ�ܼ�ȥ�淴Ӧ�Ļ�ܡ����淴Ӧ�Ļ��Ϊx������483.6kJmol��1=334.4kJmol��1-x�����x=818.0 kJmol��1��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ������ȥ��Ӧ����
A. �Ҵ���Ũ���Ṳ�ȵ�140�� B. �Ҵ��������ᣨHBr����Ӧ
C. �Ҵ���������Ӧ������ȩ D. �Ҵ���Ũ���Ṳ����170��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��FeCl3 ���о�ˮ���ã�����ʴ�豸�����ۺ��Ȼ�����һ�����͵���������������ˮ��FeCl3 ��Ч���Ҹ�ʴ��С��(��֪25����Ksp[Fe(OH)3]=4.0��10��38��lg2=0.3)
��ش��������⣺
(1)FeCl3��ˮ��ԭ���� ��(�����ӷ���ʽ��ʾ)��Fe3��ˮ�����ɵ�Fe(OH)3��������������ˮ�е��������ʣ������´˷�Ӧ��ƽ�ⳣ��Ϊ (��д��ֵ)��
(2)��FeCl3 ��Һ��NaHCO3 ��Һ��ϣ������ӷ���ʽΪ ��
(3)25��ʱpH=3����Һ�У�c(Fe3��)= molL��1��
(4)FeCl3 ����Һ�з�����ˮ�⣺
Fe3����H2O![]() Fe(OH)2����H�� K1
Fe(OH)2����H�� K1
Fe(OH)2����H2O![]() Fe(OH)2����H�� K2
Fe(OH)2����H�� K2
Fe(OH)����H2O![]() Fe(OH)3��H�� K3
Fe(OH)3��H�� K3
����ˮ�ⷴӦ��ƽ�ⳣ��K1��K2��K3�ɴ�С��˳���� ��
ͨ����������������ˮ�����ۺϣ����ɾۺ������������ӷ���ʽΪ��xFe3����yH2O![]() Fex��yH������ʹƽ�������ƶ��ɲ��õķ�����(�����) ��
Fex��yH������ʹƽ�������ƶ��ɲ��õķ�����(�����) ��
a.���� b.��ˮϡ�� c.����NH4Cl d.����NaHCO3
(5) FeCl3��Һ�ɸ�ʴӡˢ��·�壬�䷴ӦΪCu ��2FeCl3 =CuCl2��2FeCl2 Ҫ���˷�Ӧ�����ԭ����н��У���������ӦʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(H3PO2)ΪһԪ�ᣬ���н�ǿ�Ļ�ԭ�ԡ�������NaH2PO2Ϊԭ�ϣ�ͨ�����ҵ��������Ʊ�������ԭ����ͼ��ʾ�����ö��Ե缫��ab,cd,ef��Ϊֻ���������ӣ��������ӣ�ͨ�������ӽ���Ĥ���ֱ��Ϊ��Ĥ������Ĥ��������˵�������������

A. �����ҷ�ӦΪ��2H2O-4e-=O2��+4H+
B. ab,ef��Ϊ��Ĥ��cdΪ��Ĥ
C. ����ϡH2SO4��ΪH3PO2����ȥabĤ����Ʒ���ܻ������ʵ�ԭ���ǣ�H3PO2�������ŵ������������H3PO4
D. ͨ����Ʒ���е�H+������ԭ����Ǩ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ��ˮ�г�����һ������Cr2O72����CrO42�������ǻ�����༰��̬ϵͳ�����ܴ���˺���������д������÷��Ĺ�������ΪCrO42��![]() Cr2O72��
Cr2O72��![]() Cr3+
Cr3+![]() Cr(OH)3�� ���е���������ƽ�⣺2CrO42������ɫ��+2H+
Cr(OH)3�� ���е���������ƽ�⣺2CrO42������ɫ��+2H+![]() Cr2O72������ɫ��+H2O
Cr2O72������ɫ��+H2O
��1����ƽ����ϵ��pH=2������Һ�� ɫ��
��2����˵����������Ӧ��ƽ��״̬���� ����ѡ���ţ�
a��Cr2O72����CrO42����Ũ����ͬ b��v��(Cr2O72��)=2v��(CrO42��)
c����Һ����ɫ���� d����Һ��pHֵ����
��3��д����������Cr2O72��ת��ΪCr3+�����ӷ���ʽ�� ��
��4����Cr2(SO4)3��Һ�У��μ�NaOH����pH=4.6ʱ����ʼ����Cr(OH)3����������pH�����ߣ��������࣬����pH��13ʱ��������ʧ����������ɫ��[Cr��OH��4]�����ӣ���ƽ���ϵ���£�H++[Cr(OH)4]��������ɫ��![]() Cr��OH��3��s������ɫ��+H2O
Cr��OH��3��s������ɫ��+H2O ![]() Cr3+����ɫ��+H2O +3OH��������0.05mol��L��1��Cr2(SO4)3��Һ50mL�У���������0.6mol��L��1��NaOH��Һ����ַ�Ӧ����Һ�пɹ۲쵽������Ϊ ��
Cr3+����ɫ��+H2O +3OH��������0.05mol��L��1��Cr2(SO4)3��Һ50mL�У���������0.6mol��L��1��NaOH��Һ����ַ�Ӧ����Һ�пɹ۲쵽������Ϊ ��
��5����Na[Cr��OH��4]��Na2Cr2O7��Ϻ����Һ�м���H2SO4�ữ����Ԫ���� ��ʽ���ڣ���д���ӷ��ţ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ�����ר�Һ�°�ĸ����Ĵ����������գ��������̿ɼ�Ҫ��ʾ���£�
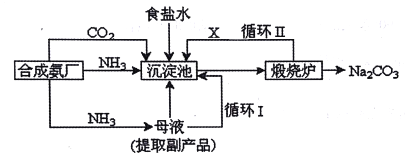
��1���������з����Ļ�ѧ��Ӧ����ʽ��______��
��2������������X���ʵķ���ʽ______��
��3��̼������뱥��ʳ��ˮ��Ӧ��������̼�����ƾ����ԭ����___��ѡ����ĸ����
A.̼������������ˮ
B.̼�����������ֽ�
C.̼�����Ƶ��ܽ����Խ�С����������Һ�����Ƚᾧ����
��4��ij̽���С����������Ƽ�ԭ�������Ʊ�̼�����ƣ�ͬѧ�ǰ�������Ƶķ�������ʵ�顣��һλͬѧ����������̼����ͨ�뺬���ı���ʳ��ˮ���Ʊ�̼�����ƣ�ʵ��װ������ͼ��ʾ��ͼ�мг֡��̶��õ�����δ��������

��ش�
�ټ��з�����Ӧ�����ӷ���ʽ��________��
����װ���е��Լ���___________��
��ʵ����������NaHCO3����IJ�����________���������������ƣ���
�ڶ�λͬѧ����ͼ����װ�ý���ʵ�飨����װ��δ��������
��Ϊ��߶�����̼�ڴ˷�ӦҺ�б����յij̶ȣ�ʵ��ʱ�����ȴ�a��ͨ��___���壬�ٴ�b��ͨ��_____ ���塣
��װ��c�е��Լ�Ϊ_______��ѡ����ĸ����
A.��ʯ�� B.Ũ���� C.��ˮ�Ȼ���
��5��������д��һ��ʵ������ȡ����̼�����Ƶķ��������ü�Ҫ�����ֺ���صĻ�ѧ��Ӧ����ʽ����������________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ��X��Y��Z��W��ԭ������������������Ԫ���γɵĵ�������Ϊm��n��p��q��r��t��u����ЩԪ����ɵĶ�Ԫ���������uΪ�γ��������Ҫ����֮һ��25��ʱ��0.01mol��L-1��v��Һ�У�c��OH-��/c��H+��=1.0��1010���������ʵ�ת����ϵ��ͼ��ʾ������˵����ȷ����
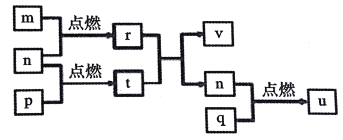
A. ԭ�Ӱ뾶�Ĵ�С��W>Z>Y>X
B. Z�ֱ���Y��W��ɵĻ������л�ѧ�����Ϳ�����ͬ
C. v������ˮ�ĵ����u�ܴٽ�ˮ�ĵ���
D. ճ��q���Թܿ��þƾ�ϴ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������أ��ֲ�Ӧ�ÿ���������ʹ���������������Ľṹ���Ա�ʾΪ��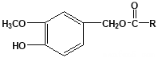 (RΪ����)������һ���������������J�ĺϳ�·�����£�
(RΪ����)������һ���������������J�ĺϳ�·�����£�
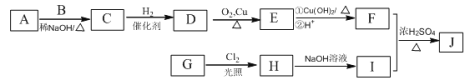
��֪��
��A��B��EΪͬϵ�����B����Է�������Ϊ44��A��B�˴Ź���������ʾ�����������������ȷֱ�Ϊ9��1��3��1��
�ڻ�����J�ķ���ʽΪC15H22O4��
��
�ش��������⣺
��1��G������������� �� ��
��2����C����D�ķ�Ӧ����Ϊ ��D�Ļ�ѧ����Ϊ ��
��3���ٵĻ�ѧ����ʽΪ ��
��4��J�Ľṹ��ʽΪ ��
��5��G��ͬ���칹���У������ϵ�һ�ȴ���ֻ��һ�ֵĹ��� ��(���������칹)���˴Ź���������ʾ2������ (д�ṹ��ʽ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��Ϊ��̽��̼�����ϡ���ᷴӦ�����е����ʱ仯����VmLϡ�����м���������̼��ƣ��ռ���Ӧ�ų���CO2����������ѻ���Ϊ��״���µ���ֵ����ʵ���¼���£��ۼ�ֵ����
ʱ�䣨min�� | 1 | 2 | 3 | 4 | 5 |
CO2�����mL�� | 50 | 120 | 232 | 290 | 310 |
��1��0��1 min��1��2 min��2��3 min��3��4 min��4��5 min���ʱ����У�_________��Ӧ������졣
��2��������Һ������䣬4��5minʱ����������Ũ�ȱ仯����ʾ�ĸ÷�Ӧ����Ϊ____________________________��
��3��Ϊ�˽���������ѧ��Ӧ�ķ�Ӧ���ʣ�����Һ�м����������ʣ�����Ϊ���е���
_______________�����ţ���
a������ˮ b��Ũ���� c��NaCl���� d��NaCl��Һ
��4���������������⣬����Ϊ�����Բ�ȡ��Щ��ʩ�����ͻ�ѧ��Ӧ���ʣ�����д������_______________________________________________________________________��
________________________________________________________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com