
【题目】在强酸性溶液中能大量共存的离子是( )
A.S2﹣ B.AlO2﹣ C.HCO3﹣ D.NH4+
科目:高中化学 来源: 题型:
【题目】下列用来表示物质变化的化学方程式中,正确的是
A.粗铜精炼时,与电源正极相连的是纯铜,阳极反应式为Cu﹣2e﹣═Cu2+
B.氢氧燃料电池的负极反应式:O2+2H2O+4e﹣═4OH﹣
C.用惰性电极电解饱和食盐水时,阳极的电极反应式为2Cl﹣﹣2e﹣═Cl2↑
D.钢铁发生电化学腐蚀的正极反应式:Fe﹣2e﹣═Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是重要化工原料,其产量是一个国家石油化工水平的标志。通过石油裂解可以获得乙烯,再以乙烯为原料还可以合成很多的化工产品。已知乙烯能发生以下转化:
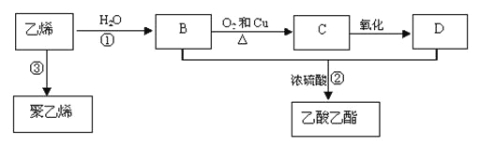
(1)乙烯的结构简式为 。
(2)反应①的反应类型是 ,D中含官能团名称为 。
(3)写出以下反应的化学方程式:[x① ;② ;③ 。
(4)乙烯大量用来生产环氧乙烷,生产工艺主要有两种:
工艺一:![]()
工艺二:![]()
根据绿色化学的原则,理想的生产工艺是原子经济性好的反应,在实际生产中,应采用___________(填“工艺一”或“工艺二”)更环保、更经济。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】数十年来,化学工作者对碳的氧化物做了广泛深入的研究并取得了一些重要成果。在高温高压下CO具有极高的化学活性,能与多种单质或化合物反应。
(1)工业上常采用水蒸气喷到灼热的炭层上实现煤的气化(制得CO、H2),该反应的化学方程式是 。
(2)上述煤气化过程中需向炭层交替喷入空气和水蒸气,喷入空气的目的是 ;反应生成的气体在加热、催化剂作用条件下可合成液体燃料甲醇,该反应的化学方程式为 。
(3)一定条件下,CO与H2可合成甲烷,反应方程式为:CO(g)+3H2(g)![]() CH4(g)+H2O (g)该条件下,该反应能够自发进行的原因是 。
CH4(g)+H2O (g)该条件下,该反应能够自发进行的原因是 。
(4)CO—空气燃料电池中使用的电解质是搀杂了Y2O3的ZrO2晶体,它在高温下能传导O2-。该电池正极的电极反应式为 。
(5)工业上可通过甲醇羰基化法制取甲酸甲酯,反应方程式为:
CH3OH(g)+CO(g)![]() HCOOCH3(g) ΔH =-29.1 kJ·mol-1
HCOOCH3(g) ΔH =-29.1 kJ·mol-1
科研人员对该反应进行了研究,部分研究结果如下:
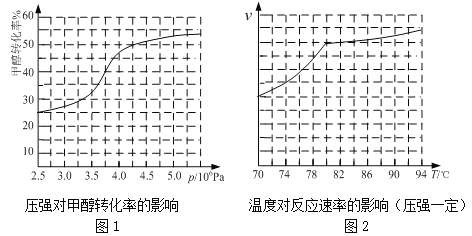
①根据反应体系的压强对甲醇转化率的影响并综合考虑生产成本因素,工业制取甲酸甲酯应选择的压强为 。
a.3.5×106Pa b.4.0×106Pa c.5.0×106Pa
②实际工业生产中采用的温度是 ,其理由是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如图。下列叙述正确的是( )
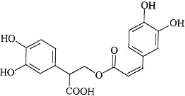
A.迷迭香酸属于芳香烃
B.1mol迷迭香酸最多能和9mol氢气发生加成反应
C.迷迭香酸可以发生水解反应、取代反应和酯化反应
 D.1mol迷迭香酸最多能和含5mol NaOH的水溶液完全反应
D.1mol迷迭香酸最多能和含5mol NaOH的水溶液完全反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.钠、钾着火时,不能用泡沫灭火器灭火
B.氧化铝是冶炼金属铝的原料,也是较好的耐火材料
C.石英是制造光导纤维的原料,也是常用的半导体材料
D.在汽车尾气系统中装催化转化器,可降低尾气中CO、NOx等的排放量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某+2价离子的电子排布式为1s22s22p43s23p43d10,该元素在周期表中所属的族是( )
A. ⅡA B. ⅡB C. ⅤⅡ D. ⅠB
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硅藻土为载体的五氧化二钒(V2O5)是接触法生产硫酸的催化剂。从废钒催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
以下是一种废钒催化剂回收工艺路线:
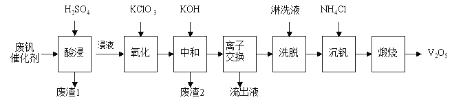
回答下列问题:
(1)“酸浸”时V2O5转化为VO2+,反应的离子方程式为___________,同时V2O4转成VO2+。“废渣1”的主要成分是__________________。
(2)“氧化”中欲使3 mol的VO2+变为VO2+,则需要氧化剂KClO3至少为____________mol。
(3)“中和”作用之一是使钒以V4O124-形式存在于溶液中。“废渣2”中含有_____________。
(4)“离子交换”和“洗脱”可简单表示为:4ROH+![]()
![]() R4V4O12+4OH(以ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈___________性(填“酸”“碱”“中”)。
R4V4O12+4OH(以ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈___________性(填“酸”“碱”“中”)。
(5)“流出液”中阳离子最多的是________。
(6)“沉钒”得到偏钒酸铵(NH4VO3)沉淀,写出“煅烧”中发生反应的化学方程式____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com