
【题目】某兴趣小组设计如图所示的装置进行原电池原理的探究。下列叙述错误的是

A.a和b不连接时,锌片上有气体生成,该装置不能形成原电池
B.a和b用导线连接时锌片为负极,发生的反应式为:Zn-2e-=Zn2+
C.a和b用导线连接时,电子由Zn经导线流向Cu,再经稀硫酸流回Zn
D.无论a和b是否连接,稀硫酸均参与反应
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】钛的化合物如TiO2、Ti(NO3)4、TiCl4、Ti(BH4)2等均有着广泛用途。
(1)写出Ti的基态原子的外围电子排布式_____。
(2)TiCl4熔点是﹣25℃,沸点136.4℃,可溶于苯或CCl4,该晶体属于_____晶体;BH4﹣中B原子的杂化类型为_____。
(3)在 TiO2催化作用下,可将CN﹣氧化成CNO﹣,进而得到N2。与CNO﹣互为等电子体的分子化学式为(只写一种)________。
(4)Ti3+可以形成两种不同的配合物:[Ti(H2O)6]Cl3(紫色),[TiCl(H2O)5]Cl2H2O(绿色)。绿色晶体中配体是_______。

(5)TiO2难溶于水和稀酸,但能溶于浓硫酸,析出含有钛酰离子的晶体,钛酰离子常成为链状聚合形式的阳离子,其结构形式如图1,化学式为______。
(6)金属钛内部原子的堆积方式是面心立方堆积方式,如图2。若该晶胞的密度为ρgcm﹣3,阿伏加德罗常数为NA,则该晶胞的边长为___cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酰苯胺是一种白色有光泽片状结晶或白色结晶粉末,是磺胺类药物的原料, 可用作止痛剂、退热剂、防腐剂和染料中间体,乙酰苯胺的制备原理为:![]() +CH3COOH
+CH3COOH![]() +H2O,有关物质的性质如下表:
+H2O,有关物质的性质如下表:
名称 | 式量 | 性状 | 密度/g·cm-3 | 沸点/℃ | 溶解度 | |
苯胺 | 93 | 无色油状液体,易氧化 | 1.02 | 184.4 | 微溶于水 | 易溶于乙醇、乙醚 |
乙酸 | 60 | 无色液体 | 1.05 | 118.1 | 易溶于水 | 易溶于乙醇、乙醚 |
乙酰苯胺 | 135 | 白色晶体 | 1.22 | 304 | 微溶于冷水,溶于热水 | 易溶于乙醇、乙醚 |
注:刺形分馏柱的作用相当于二次蒸馏,用于沸点差别不太大的混合物的分离。
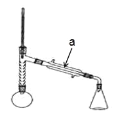
实验步骤:
步骤 1:在圆底烧瓶中加入无水苯胺 9.2 mL,冰醋酸 17.4 mL,锌粉 0.1 g,安装仪器, 加入沸石,调节加热温度,使分馏柱顶温度控制在 105℃ 左右,反应约 60~80 min,反应 生成的水及少量醋酸被蒸出。
步骤 2:在搅拌下,趁热将烧瓶中的物料以细流状倒入盛 100 mL 冰水的烧杯中,剧烈搅拌,并冷却,结晶,抽滤、洗涤、干燥,得到乙酰苯胺粗品。
步 骤 3:将此粗乙酰苯胺进行重结晶,晾干,称重,计算产率。
(1)仪器 a 的名称____________________;
(2)步骤 1 加热可用______________(填“水浴”或“油浴”);
(3)制备过程中加入粒的作用:___________________;
(4)从化学平衡的角度分析,控制分馏柱上端的温度在 105℃左右的原因_______________________;
(5)乙酰苯胺粗品因含杂质而显色,欲用重结晶进行提纯,步骤如下:粗产品溶于沸水中配 成饱和溶液→再加入少量蒸馏水→加入活性炭脱色→加热煮沸→趁热过滤→________________→过 滤→洗涤→干燥;
(6)该实验最终得到纯品 10.8g,则乙酰苯胺的产率是______________;
(7)如果重结晶过程中,加入活性炭过多,会造成产率下降,其可能原因为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对有关事实分析不正确的是
选项 | 事实描述 | 相关知识分析 |
A | 谚语“正月打雷麦谷堆”、“雷雨肥庄稼” | 自然固氮:N2+2O2 |
B | 成语“滴水石穿” | 包含CaCO3+CO2+H2O=Ca(HCO3)2 |
C | 《木草经集注》记载“强烧之,紫青烟起,云是真硝石也。” | “硝石”为KNO3,钾元素的焰色反应为紫色 |
D | 野外之鬼磷,其火色青,其状如炬,或聚或散,俗称鬼火,实乃诸血之磷光也。 | “磷光”是指磷化氢(PH3)自燃,将化学能转化为光能 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下面的信息,下列叙述正确的是( )
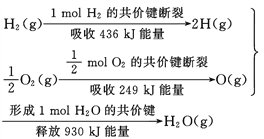
A. 2 mol H2(g)跟 1 mol O2(g)反应生成 2 mol H2O(g)吸收能量为490 kJ
B. 化学反应中能量变化的大小与反应物的质量多少无关
C. 1 mol H2(g) 跟0.5mol O2(g) 反应生成 1 mol H2O(l)释放能量为245 kJ
D. 2molH2O (g)的能量比2 mol H2(g)与1 mol O2(g)的能量之和低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(I)某温度时,在2 L的容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。请通过计算回答下列问题。
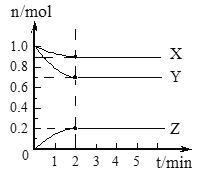
(1)列式计算反应开始至2 min,Y的平均反应速率___________。
(2)分析有关数据,写出X、Y、Z的反应方程式___________。
(3)由图中看出:________分钟后,A、B、C各物质的物质的量不再随时间而变化,说明在这个条件下,该反应已达到了________________状态。
(II)将纯锌片和纯铜片按如图所示方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:
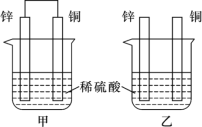
①下列说法正确的是____________(填字母代号)。
A.甲、乙均为化学能转变为电能的装置
B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲____乙(填“>”、“<“或“=”)。
③请写出图中构成原电池的装置正极的电极反应式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学平衡常数K的数值大小是衡量化学反应进行程度的标志,下列反应的平衡常数数值如下:
2NO(g) N2(g)+ O2(g) K1=1×1030
2H2(g)+ O2(g) 2H2O(g) K2=2×1081
2CO2(g) 2CO(g)+ O2(g) K3=4×10﹣92
以下说法正确的是( )
A. NO分解产生O2的反应的平衡常数表达式K1=c(N2)c(O2)/c(NO)
B. 水分解产生O2,此时平衡常数的数值约为5×10﹣80
C. NO、H2O、CO2三种化合物分解放出O2的倾向由大到小的顺序为NO>H2O>CO2
D. 以上说法都不正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有500 mL 1 mol·L-1的H2SO4溶液,下列操作及结论正确的是
A.取出50mL该溶液,其中c(SO![]() )=0.1 mol·L-1
)=0.1 mol·L-1
B.取出50mL该溶液,加入足量的BaCl2溶液,完全反应,可得11.65gBaSO4沉淀
C.取出100mL该溶液,加入足量的锌粒,充分反应,所得气体的体积为2.24L
D.取出50mL该溶液,加蒸馏水配制成100 mL溶液,c(H+)=2mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com