
【题目】将一定量的硫酸钡放入水中,有关的叙述正确的是( )
A.硫酸钡不溶于水,硫酸钡固体质量不会改变
B.最终会得到BaSO4的极稀的饱和溶液
C.因为![]() 很容易发生,所以不存在BaSO4(s)
很容易发生,所以不存在BaSO4(s)![]() Ba2+(aq)+SO42-(aq)的过程
Ba2+(aq)+SO42-(aq)的过程
D.因为BaSO4难溶于水,所以改变外界条件也不会改变BaSO4的溶解性
 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:高中化学 来源: 题型:
【题目】广东省有着丰富的海洋资源。海水提取食盐和Br2以后的盐卤可以用来制备纯净的MgCl2或MgO。盐卤中含有Mg2+、Cl-,还含有少量Na+、Fe2+、Fe3+和CO(NH2)2等.制备流程如图所示:
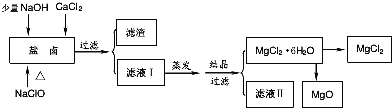
(1)滤渣的成分是____________(填化学式);滤液Ⅱ中所含的主要杂质离子是________(写离子符号)。
(2)用NaClO除去尿素CO(NH2)2时,生成物除盐外,都是能参与大气循环的物质,则该反应的化学方程式为_____________________;
(3)用MgCl26H2O制备无水MgCl2过程中,所需要的化学试剂是___________________;
(4)海水制溴过程中吸收潮湿空气中的Br2是利用SO2气体,SO2吸收Br2的离子方程式是_______________;SO2气体可来源于硫酸工业的尾气,同时,SO2尾气也可用氨水吸收,作为制备化肥的原料,SO2气体用氨水吸收得到的产物可能是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学气敏传感器可用于监制环境中 NH3 的含量,其工作原理示意图如图所示,下列说法不正确的是( )
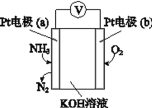
A.电池工作一段时间后pH将变大
B.反应消耗的NH3与O2的物质的量之比为4:3
C.负极的电极反应式为2NH36e6OHN26H2O
D.电流方向:电极b→导线→电极a→电解质溶液→电极b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表所示为元素周期表的一部分,参照元素①~⑩在表中的位置,请回答下列问题:

(1)写出①和④两种元素原子按1:1组成的常见化合物的电子式______。
(2)用电子式表示⑥和⑨形成化合物的过程:______。
(3)③、⑧、⑩的最高价氧化物对应水化物的酸性由强到弱的顺序为 ______(用化学式表示)。
(4)已知周期表中存在对角相似规则,如②与⑦在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑥的氢氧化物反应的化学方程式 ______。
(5)⑤、⑥、⑩的离子半径由大到小的顺序为 ______(用离子符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为 2L 的密闭容器中进行如下反应:A g + 2Bg ![]() 3Cg + nDg ,开始时 A 为 4mol,B 为 6mol,5min 末时测得 C 的物质的量为 3mol,D 的化学反应速率vD = 0.2mol L1 min1 ,请回答:
3Cg + nDg ,开始时 A 为 4mol,B 为 6mol,5min 末时测得 C 的物质的量为 3mol,D 的化学反应速率vD = 0.2mol L1 min1 ,请回答:
(1)5min 末A 的物质的量浓度为_____,
(2)前 5min 内用B 表示的化学反应速率 v(B)为_____,
(3)前 5min 内A 的转化率为_____,
(4)化学方程式中 n 的值为_____,
(5)此反应在四种不同情况下的反应速率分别为:
① v A = 5mol L1 min1 ② v B = 6mol L1 min1
③ v C = 4.5mol L1 min1 ④ v D = 8mol L1 min1
其中反应速率最快的是_____(填编号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是引起“温室效应”的主要物质,节能减排,高效利用化石能源,控制
是引起“温室效应”的主要物质,节能减排,高效利用化石能源,控制![]() 排放,探索
排放,探索![]() 的循环利用是保护环境,促进经济科持续发展的重要举措.
的循环利用是保护环境,促进经济科持续发展的重要举措.
(1)在一定温度下,向2L固定容积的密闭容器中通入2mol![]() ,3mol
,3mol![]() ,发生反应为:
,发生反应为:![]() ,测得
,测得![]() 和
和![]() 的浓度随时间变化如图1所示.
的浓度随时间变化如图1所示.
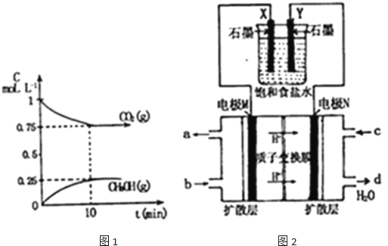
①能说明该反应已达到平衡状态的是 ______
A.![]() 体积分数在混合气体中保持不变
体积分数在混合气体中保持不变
B.单位时间内有![]()
![]() 断裂,同时有
断裂,同时有![]()
![]() 键生成
键生成
C.混合气体的密度不随时间变化
D.当体系中![]() :
:![]() :l,且保持不变
:l,且保持不变
②下列措施能使![]() 增大的是 ______
增大的是 ______
A.升高温度 ![]() 恒温恒容充入
恒温恒容充入![]()
![]() 使
使![]() 变成
变成![]()
D.恒温恒容下,再充入2mol![]() ,3mol
,3mol![]()
③计算该温度下此反应的平衡常数![]() ______ ;若使
______ ;若使![]() 应采取的措施是 ______
应采取的措施是 ______
A.增大压强![]() 恒压加入一定量
恒压加入一定量![]() C.恒容通入
C.恒容通入![]() D.降低温度
D.降低温度![]() 升高温度
升高温度
(2)如图2所示:用某甲醇燃料电池作电源电解饱和食盐水.
①写出电极N发生的反应式: ______
②若食盐水体积为300Ml,电解过程溶液体积变化忽略不计,常温下测得![]() 时,理论上消耗甲醇质量为 ______
时,理论上消耗甲醇质量为 ______ ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组比值为1∶2的是( )
A.0.1mol·L-1与0.2mol·L-1 CH3COOH溶液,c(H+)之比
B.0.1mol·L-1 Na2CO3溶液,![]()
![]() c(Na+)之比
c(Na+)之比
C.pH=10的Ba(OH)2溶液与氨水,溶质的物质的量浓度之比
D.pH=3的H2SO4与CH3COOH溶液,![]()
![]() c(CH3COO-)之比
c(CH3COO-)之比
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】膳食纤维具有突出的保健功能,近年来受到人们的普遍关注,被世界卫生组织称为人体的“第七营养素”。木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构简式如图所示。下列有关芥子醇的说法正确的是( )

A.芥子醇的分子式是C11H12O4
B.芥子醇能发生水解反应
C.芥子醇分子中所有原子不可能在同一平面
D.1 mol芥子醇能与足量溴水反应消耗3 mol Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种化合物,均含有某种常见元素,它们的转化关系如下图所示,其中A为澄清溶液,C为难溶于水的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)。请回答下列问题:

(1)写出化学式:A__________C__________
(2)写出下列反应的离子方程式:
A→B:________________________________。
B→D:________________________________。
C→E:________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com