

 ��
��

 ����Ϣʹ�Ľṹ��ʽΪ
����Ϣʹ�Ľṹ��ʽΪ


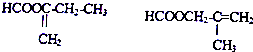
���� B��HCN��Ӧ����CH3C��OH��CNCH3����B�Ľṹ��ʽΪCH3COCH3��A����������Ӧ���ɱ�ͪ�ͱ��ӣ���A�Ľṹ��ʽΪ ��D����������ͼ��ʾ��Է�������Ϊ100��10gD�����ʵ���=$\frac{10g}{100g/mol}$=0.1mol�����ɶ�����̼�����ʵ���=$\frac{22.0g}{44g/mol}$=0.5mol������ˮ�����ʵ���=$\frac{7.2g}{18g/mol}$=0.4mol��
��D����������ͼ��ʾ��Է�������Ϊ100��10gD�����ʵ���=$\frac{10g}{100g/mol}$=0.1mol�����ɶ�����̼�����ʵ���=$\frac{22.0g}{44g/mol}$=0.5mol������ˮ�����ʵ���=$\frac{7.2g}{18g/mol}$=0.4mol��
��D�����к���5��Cԭ�ӡ�8��Hԭ�ӣ�D����Է�������Ϊ100����D�л�����Oԭ�ӣ�Oԭ�Ӹ���=$\frac{100-12��5-1��8}{16}$=2������D�ķ���ʽΪC5H8O2���䲻���Ͷ�=$\frac{5��2+2-8}{2}$=3��D�ܷ����Ӿ۷�Ӧ˵������̼̼˫��������������������CH3C��OH��CNCH3�ͼ״�����������Ӧ��ͬʱ����������ȥ��Ӧ����D�Ľṹ��ʽΪCH2=C��CH3��COOCH3��D�����Ӿ۷�Ӧ����E����E�Ľṹ��ʽΪ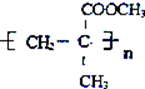 ��
��
���������Ϣ֪��CH2=C��CH3��COOH��SOCl��Ӧ����G��G�Ľṹ��ʽΪCH2=C��CH3��COCl��H�����Ӿ۷�Ӧ���ɺ�����Ϣʹ�߷���ҩ���H�Ľṹ��ʽΪ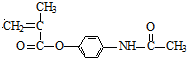 ��G������Ϣʹ��Ӧ����H��������Ϣʹ�ṹ��ʽΪ
��G������Ϣʹ��Ӧ����H��������Ϣʹ�ṹ��ʽΪ ���ٽ����Ŀ�������
���ٽ����Ŀ�������
��� �⣺B��HCN��Ӧ����CH3C��OH��CNCH3����B�Ľṹ��ʽΪCH3COCH3��A����������Ӧ���ɱ�ͪ�ͱ��ӣ���A�Ľṹ��ʽΪ ��D����������ͼ��ʾ��Է�������Ϊ100��10gD�����ʵ���=$\frac{10g}{100g/mol}$=0.1mol�����ɶ�����̼�����ʵ���=$\frac{22.0g}{44g/mol}$=0.5mol������ˮ�����ʵ���=$\frac{7.2g}{18g/mol}$=0.4mol��
��D����������ͼ��ʾ��Է�������Ϊ100��10gD�����ʵ���=$\frac{10g}{100g/mol}$=0.1mol�����ɶ�����̼�����ʵ���=$\frac{22.0g}{44g/mol}$=0.5mol������ˮ�����ʵ���=$\frac{7.2g}{18g/mol}$=0.4mol��
��D�����к���5��Cԭ�ӡ�8��Hԭ�ӣ�D����Է�������Ϊ100����D�л�����Oԭ�ӣ�Oԭ�Ӹ���=$\frac{100-12��5-1��8}{16}$=2������D�ķ���ʽΪC5H8O2���䲻���Ͷ�=$\frac{5��2+2-8}{2}$=3��D�ܷ����Ӿ۷�Ӧ˵������̼̼˫��������������������CH3C��OH��CNCH3�ͼ״�����������Ӧ��ͬʱ����������ȥ��Ӧ����D�Ľṹ��ʽΪCH2=C��CH3��COOCH3��D�����Ӿ۷�Ӧ����E����E�Ľṹ��ʽΪ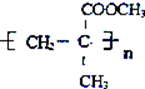 ��
��
���������Ϣ֪��CH2=C��CH3��COOH��SOCl��Ӧ����G��G�Ľṹ��ʽΪCH2=C��CH3��COCl��H�����Ӿ۷�Ӧ���ɺ�����Ϣʹ�߷���ҩ���H�Ľṹ��ʽΪ ��G������Ϣʹ��Ӧ����H��������Ϣʹ�ṹ��ʽΪ
��G������Ϣʹ��Ӧ����H��������Ϣʹ�ṹ��ʽΪ ��
��
��1��ͨ�����Ϸ���֪��A�Ľṹ��ʽΪ ������Ϣʹ�ṹ��ʽΪ
������Ϣʹ�ṹ��ʽΪ ��
��
�ʴ�Ϊ�� ��
�� ��
��
��2��ͨ�����Ϸ���֪���÷�ӦΪ�ӳɷ�Ӧ���ʴ�Ϊ���ӳɣ�
��3��C6H6OΪ���ӣ���ɱ���������ʴ�Ϊ��ɱ��������
��4��ͨ�����Ϸ���֪��D�Ľṹ��ʽΪCH2=C��CH3��COOCH3��D�й�����Ϊ̼̼˫����������D�����ӳɷ�Ӧ����E����Ӧ����ʽΪ ��
��
�ʴ�Ϊ��̼̼˫���������� ��
��
��5��������Ϣʹ�߷���ҩ������������������Һ����ȡ����Ӧ����Ӧ����ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��6��D�Ľṹ��ʽΪCH2=C��CH3��COOCH3��D��ͬ���칹�������������������D������ͬ������˵������������̼̼˫�������ܷ����۾���Ӧ��˵�����м���������H�˴Ź������������ֲ�ͬ��������ԭ�ӱ����ֱ�Ϊ1��2��2��3��˵���÷����к���4�����͵�Hԭ�ӣ�����������D��ͬ���칹����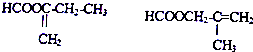 ���ʴ�Ϊ��
���ʴ�Ϊ��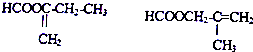 ��
��
���� ���⿼���л����ƶϣ����ؿ���ѧ�������������ƶ���������CH3C��OH��CNCH3Ϊͻ�ƿڲ��������ϵķ����Ƶ���֪�������л���Ĺ����ż��ܹ������ķ�Ӧ��ע���������Ϣ��������ѵ���ͬ���칹��������жϣ���Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 36gþ�������ĵ�������ȫȼ�չ�ת�Ƶĵ�����Ϊ3NA | |
| B�� | �����£�21.0g��ϩ�Ͷ�ϩ�Ļ�������к��е�C-H���ۼ���ĿΪ3NA | |
| C�� | ��״���£�44.8 L NO��22.4 LO2��Ϻ������з�������Ϊ3NA | |
| D�� | 1 molNa2O��Na2O2�����������������������3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | һ��������Ba2+��NH4+���ܴ��� | B�� | CO32-һ������ | ||
| C�� | Na+һ������ | D�� | һ��������Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ϸ�Ӧ | B�� | �û���Ӧ | C�� | ������ԭ��Ӧ | D�� | ���ֽⷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
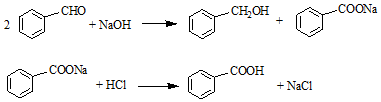
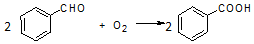
| ���� | ������ | ��״ | ����ܶ� ��g•cm-3�� | �е� ���棩 | �ܽ�� | ||
| ˮ | ���� | ||||||
| ����ȩ | 106 | ��ɫҺ�� | 1.04 | 179 | �� | ���� | |
| ������ | 122 | ��ɫ���� | 1.27 | 249 | 0.21g | 66g | |
| ���״� | 108 | ��ɫҺ�� | 1.04 | 205 | �� | ���� | |
| ���� | 74 | ��ɫҺ�壮 | 0.71 | 35 | ���� | -- | |
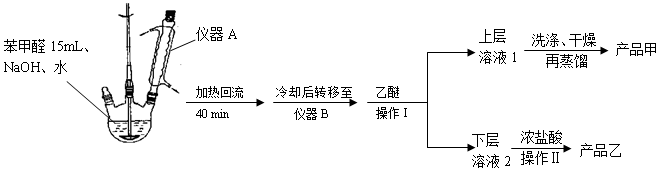
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

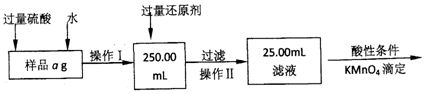
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
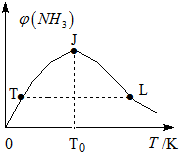 ������������Դ����Ҫ����ԭ�ϣ�
������������Դ����Ҫ����ԭ�ϣ�| ������� | ��ʼʱ�����ʵ����ʵ���/mol | ƽ��ʱ��Ӧ�е������仯 | ||
| H2 | N2 | NH3 | ||
| �� | 3n | n | 0 | �ų�����a kJ |
| �� | 3n | 2n | 0 | �ų�����b kJ |
| �� | 6n | 2n | 0 | �ų�����c kJ |
| ʱ��/min | 0 | 5 | 10 | 15 | 20 | 25 | �� |
| NH3/mol | 2 | 1.0 | 0.5 | 0.25 | 0.24 | 0.24 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
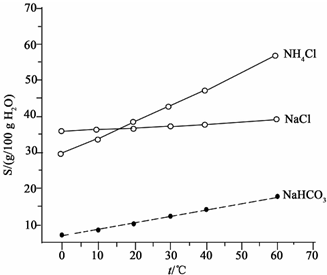
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | x=0.6a 2Fe2++Cl2=2Fe3++2Cl- | |
| B�� | x=a 2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl- | |
| C�� | x=0.4a 2Br-+Cl2=Br2+2Cl- | |
| D�� | x=2a 2Fe2++6Br-+4Cl2=3Br2+2Fe3++8Cl- |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com