
【题目】下列关于如图所示原电池的说法正确的是
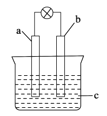
A.当a为Cu,b为含有碳杂质的 Al,c 为稀硫酸时,b 极上观察不到气泡产生
B.当a为石墨,b为 Fe,c为浓硫酸时,不能产生连续的稳定电流
C.当a为Mg,b为 Al,c为NaOH 溶液时,根据现象可推知 Al 的活动性强Mg的
D.当a为石墨,b为 Cu,c为FeCl3 溶液时,a、b之间没有电流通过
科目:高中化学 来源: 题型:
【题目】有以下物质:①石墨;②氯化氢气体;③酒精;④氨水;⑤二氧化碳;⑥碳酸氢钠固体;⑦氯化铁溶液;⑧纯醋酸;⑨氧化钠固体;⑩铝。
(1)属于非电解质的是______________;属于强电解质的是__________;属于弱电解质的是___________。(用序号填空)
(2)写出物质⑥溶于水溶液显碱性的原因_______(用离子方程式和简要文字说明作答)
(3)写出物质⑥和⑧在水中反应的离子方程式:_____________。
(4)配制溶液⑦时通常将⑦先溶于___________,然后再加水稀释,通过增加溶液中_______的浓度以防止其发生水解。
(5)浓度、体积相同的②和⑧的溶液,加入相同形状且足量的Zn粒,反应速率快的是___(用序号填空);pH值、体积相同的②和⑧的溶液时,产生气体的量多的是________。(用序号填空)
查看答案和解析>>
科目:高中化学 来源: 题型:
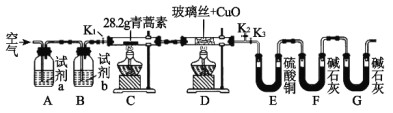
【题目】青蒿素是一种高效的抗疟药,某研究性学习小组的同学通过查阅资料获得如下信息:青蒿素是由碳、氢、氧三种元素所组成的,熔点为156~157℃,他们设计了如下装置来测量青蒿素的分子组成,回答下列问题:
装置 | 实验前/g | 实验后/g |
E | 22.6 | 42.4 |
F | 80.2 | 146.2 |
(1)试剂加入后首先要进行的操作是_____________,其目的是____________,实验中需要对开关K1、K2、K3进行操作,首次对开关K1、K2、K3进行操作的方法是________,适当时间后再关闭相应的开关,为提高实验的准确性,在C处停止加热后还应进行的操作是____________。
(2)试剂a、b分别是________________________________________,点燃C、D处酒精灯的先后顺序是___________________________,使用装置D的目的是___________。
(3)E中使用硫酸铜相对于使用CaCl2的好处(不考虑吸收效果的差异性)是_____。
(4)充分反应后获得的有关数据如上表(假设生成的气体全部被吸收):则测得青蒿素的最简式是_________________________。
(5)若要求出青蒿素的分子式,还需要通过实验测量出一个数据,请你指出该数据是什么,测量出该数据的方法是(只考虑理论上的可能性):___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知高能锂电池的总反应式为:2Li+FeS=Fe+Li2S[LiPF6SO(CH3)2为电解质],用该电池为电源进行如图的电解实验,电解一段时间测得甲池产生标准状况下H24.48L。下列有关叙述不正确的是
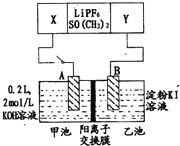
A.从隔膜中通过的离子数目为0.4NA
B.若电解过程体积变化忽略不计,则电解后甲池中溶液浓度为4mol/L
C.A电极为阳极
D.电源正极反应式为:FeS+2Li++2e-=Fe+Li2S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H是合成抗炎药洛索洛芬钠的关键中间体,它的一种合成路线如下:

回答下列问题:
(1)A的名称是____,H中官能团名称是____;
(2)反应①的反应条件为____;
(3)反应⑥的化学方程式为________;反应类型为____。
(4)反应⑦除生成H外,还生成了另一种有机产物的结构简式为____。
(5)符合下列条件的G的同分异构体有____种。
I.能发生银镜反应 Ⅱ.苯环上一氯取代物只有一种 Ⅲ.核磁共振氢谱有4组峰
(6)仿照H的合成路线,设计一种由B合成![]() 的合成路线___。
的合成路线___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LiOH是制备锂离子电池的材料,可由电解法制备。工业上利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。下列说法正确的是
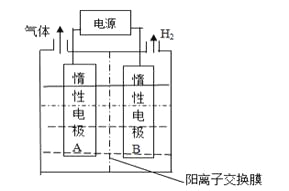
A.B极区电解液为LiOH溶液
B.电极每产生22.4L气体,电路中转移2mole-
C.电解过程中Li+迁移入B电极区、OH-迁移入A电极区
D.电解池中总反应方程式为:2HCl![]() 2H2↑+Cl2↑
2H2↑+Cl2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学校实验室从化学试剂商店买回的盐酸试剂上的标签如图所示。下列说法正确的是

A.从试剂瓶中取出100 mL该盐酸,在空气中久置,溶液质量将增大
B.1 mol Fe与足量该酸反应产生22.4 L氢气
C.配制250 mL 6 mol · L-1稀盐酸需取该浓盐酸100 mL
D.该溶液溶质的物质的量浓度约为12 mol · L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项操作中发生“先产生沉淀,然后沉淀又溶解”现象的是
①向澄清石灰水中逐渐通入CO2至过量 ②向NaAlO2溶液中逐渐通入CO2至过量
③向AlCl3溶液中逐滴加入NaOH至过量 ④向硅酸钠溶液中逐滴加入盐酸至过量
⑤向Fe(OH)3胶体中逐滴加入稀盐酸至过量 ⑥向Ca(ClO)2溶液中逐渐通入CO2至过量
A.①③B.①②⑤C.①③⑤⑥D.①②⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种。①加入铝片,产生无色无味的气体;②加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是( )
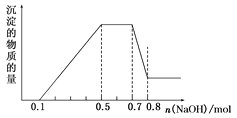
A.溶液中一定不含CO32-,可能含有SO42-和NO3-
B.在滴加NaOH溶液物质的量为0.5~0.7mol时,发生离子反应为Al3++4OH-=AlO2-+2H2O
C.溶液中的阳离子只有H+、Mg2+、Al3+
D.n(H+)∶n(NH4+)∶n(Mg2+)=2∶4∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com