
【题目】利用如图装置,完成很多电化学实验.下列有关此装置的叙述中,正确的是
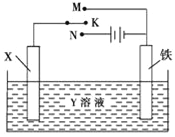
A. 若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阴极保护法
B. 若X为碳棒,Y为NaCl溶液,开关K置于N处,可加快铁的腐蚀
C. 若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动
D. 若X为铜棒,Y为硫酸铜溶液,开关K置于N处,可用于铁表面镀铜,溶液中铜离子浓度将减小
【答案】C
【解析】当开关置于M处时,此装置为原电池,锌比铁活泼,所以锌是负极,铁是正极,负极锌溶解失去电子,电子通过外电路传到正极保护了铁,这种铁的防护方法在电化学上称为牺牲阳极的阴极保护法。所以A不正确。
当开关置于N处时,此装置为电解池,碳电极连接电源正极作阳极,铁电极作阴极被保护起来,此法称为外接电流的阴极保护法,B不正确。
当开关置于M处时,此装置为原电池,铁比铜活泼,铁作负极失去电子,电子经外电路流向正极铜,溶液中铜离子在正极表面得到电子被还原为铜附着在铜表面,所以铜棒质量增加,C正确。
当开关置于N处时,此装置为电镀池,阳极铜失电子变为铜离子进入溶液,溶液中铜离子在阴极表面得到电子被还原为铜镀到铁棒表面,因为阴阳两极得失电子守恒,所以溶液中铜离子浓度保持不变,D错了。


科目:高中化学 来源: 题型:
【题目】(1)下列微粒中,只有氧化性的是_____________ (用字母填写,下同),既有氧化性又有还原性的是___________________。
A. Cl2 B. S2— C. H+ D. Na E. FeCl2
(2)在4HCl(浓)+MnO2 ![]() MnCl2+Cl2↑+2H2O反应中
MnCl2+Cl2↑+2H2O反应中
①氧化剂是________,氧化产物是________;
②被氧化与未被氧化的HCl的质量之比为_______,若有7.3gHCl被氧化,转移电子的物质的量为________;。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.25℃,两种酸的电离平衡常数如右表。
Ka1 | Ka2 | |
H2SO3 | 1.3×10-2 | 6.3×10-8 |
H2CO3 | 4.2×10-7 | 5.6×10-11 |
(1)0.10 mol·L-1Na2SO3溶液中离子浓度由大到小的顺序为____________
(2)H2SO3溶液和NaHCO3溶液反应的主要离子方程式为________________
Ⅱ.某化学小组设计下列实验测定硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液的标定浓度:
步骤1:取20.00mL0.015mol/LK2Cr2O7标准液于250mL锥形瓶中,加入20mL稀硫酸和5mL浓磷酸,用硫酸亚铁铵溶液滴定,接近终点时加入2滴R溶液作指示剂,继续滴定至终点,消耗的体积为10.10mL.
步骤2:重复操作1实验,接近终点时加入4滴R溶液,消耗的体积为10.20mL。
已知:①6Fe2+ +Cr2O72-+14H+=6Fe3+ +2Cr3+ +7H2O,其中Cr3+为绿色
②R溶液的变色原理:R(氧化型,紫红色) ![]() Q(还原性,无色)
Q(还原性,无色)
(3)该实验中需要用到的主要玻璃仪器有锥形瓶、胶头滴管、___________、______________
(4)如何判断滴定达到终点:_______________________________
(5)步骤2的主要作用是________________
(6)硫酸亚铁铵溶液的标定浓度是___________mol/L(保留三位有效数字)
(7)若滴定前锥形瓶中有水,对测定结果的影响是______(填“偏大”、“偏小”或“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测定硫酸铜晶体中结晶水含量的实验中,错误的操作是
A. 要进行恒重操作
B. 在空气中冷却后再称量
C. 加热后不能趁热称量
D. 在加热硫酸铜晶体时,要慢慢加热至晶体全部变成白色粉末
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组用如图所示装置模拟工业上生产无水FeCl2的过程。
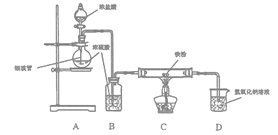
下列说法中正确的是
A. 先点燃C处酒精灯,再打开分液漏斗的活塞
B. 本实验中浓H2SO4体现出吸水性和强氧化性
C. 利用该装置制备FeCl2的原理可表示为:Fe+2HCl![]() FeCl2+H2
FeCl2+H2
D. 装置D适合处理该实验的所有尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸的反应为:S+2KNO3+3C![]() K2S+N2↑+3CO2↑,下列说法中正确的是 ( )
K2S+N2↑+3CO2↑,下列说法中正确的是 ( )
A. 该反应中的还原剂为KNO3
B. 该反应中C被还原
C. 若消耗32g S,该反应转移电子数为2 NA
D. 若生成标准状况下气体22.4L,则有0.75 mol物质被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,反应后固体质量减轻的是( ) ①氨气通过灼热的CuO粉末
②二氧化碳通过Na2O2粉末
③水蒸气通过灼热的Fe粉
④Zn投入CuSO4溶液.
A.①②
B.①④
C.②③
D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含有0.078molFeCl2的溶液中通入0.009molCl2,再向其中加入含0.01molX2O72-的酸性溶液,使溶液中的Fe2+恰好完全被氧化,且X2O72-被还原为Xn+,则n值为( )
A.2B.3C.4D.5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com