
【题目】在体积可变的密闭容器中发生反应:CO(g) + H2O(g) CO 2 (g) + H2O(g)(正反应为放热反应),改变下列条件,不能使ν正 增大的是
A. 升高温度B. 恒容充He
C. 缩小容器体积D. 恒容时充入更多的H2O(g)
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行实验,有关现象和解释均正确的是( )
选项 | 足量 | 甲中试剂 | 乙中试剂 | 现象 | 解释 |
A | CO2 | Na2SiO3 | BaCl2 | 甲浑浊、乙澄清 | 酸性:HCl>H2CO3>H2SiO3 |
B | Cl2 | 紫色石蕊 | Fe(SCN)2 | 开始均变红 | Cl2溶于水显酸性 |
C | SO2 | 品红溶液 | KMnO4 | 均褪色 | SO2具有漂白性 |
D | NH3 | AgNO3 | AlCl3 | 现象相同 | NH3H2O电离出OH﹣ |

A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体混合物可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的一种或几种组成,现对该混合物做如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积): 
下列说法正确的是( )
A.固体混合物中一定含有Al,但质量不可确定
B.固体混合物中可能含有MgCl2和AlCl3
C.固体混合物中一定含有MgCl2和FeCl2
D.固体混合物中一定含有(NH4)2SO4、MgCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有浓度为0.1molL﹣1的盐酸、硫酸、醋酸三种溶液,试回答:
(1)三种溶液中c(H+) 依次为a molL﹣1 , b molL﹣1 , c molL﹣1 , 其大小顺序为 .
(2)等体积的以上三种酸分别与过量的NaOH 溶液反应,生成的盐的物质的量依次为n 1mol,n2 mol,n3 mol,它们的大小关系为
(3)中和一定量NaOH溶液生成正盐时,需上述三种酸的体积依次是V1L、V2L、V3L,其大小关系为
(4)与锌反应时产生氢(气)的速率分别为v1、v2、v3 , 其大小关系为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在酸性介质中,往MnSO4溶液里滴加(NH4)2S2O8(过二硫酸铵)溶液会发生如下反应:Mn2++S2O82﹣+H2O→MnO4﹣+SO42﹣+H+ , 下列说法不正确的是( )
A.可以利用该反应检验Mn2+
B.氧气性比较:S2O82﹣>MnO4﹣
C.该反应中酸性介质可以为盐酸
D.若有0.1mol氧化产物生成,则转移电子0.5mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ag2CrO4在水中的沉淀溶解平衡曲线如图所示,t℃时,反应Ag2CrO4(s)+2Cl﹣(aq)=2AgCl(s)+CrO42﹣(aq)的K=2.5×107 , 下列说法正确的是( )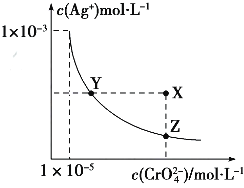
A.t℃时,Ag2CrO4的Ksp为1×10﹣12
B.t℃时,向饱和Ag2CrO4溶液中加入K2CrO4溶液,再次平衡时c2(Ag+)×c(CrO42﹣)>Ksp
C.t℃时,Ksp(AgCl)=1.56×10﹣10
D.t℃时,用0.01molL﹣1 AgNO3溶液滴定20mL 0.01molL﹣1KCl和0.01mol K2CrO4的混合溶液,CrO42﹣先沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在18.6g Fe和Zn合金中加入200mL某浓度的稀硫酸恰好完全反应,生成0.3mol H2 . 则原合金中有mol Fe,稀硫酸的物质的量浓度为 mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】晶体硅是信息科学和能源科学中的一种重要材料,可用于制芯片和太阳能电池等.以下是工业上制取纯硅的一种方法. 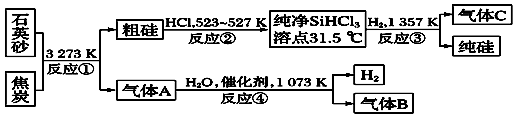
请回答下列问题(各元素用相应的元素符号表示):
(1)在上述生产过程中,属于置换反应的有(填反应代号).
(2)写出反应③的化学方程式 .
(3)化合物W的用途很广,通常可用作建筑工业和造纸工业的黏合剂,可作肥皂的填充剂,是天然水的软化剂.将石英砂和纯碱按一定比例混合加热至1 373~1 623K反应,生成化合物W,其化学方程式是
(4)A、B、C三种气体在“节能减排”中作为减排目标的一种气体是(填化学式);分别通入W溶液中能得到白色沉淀的气体是(填化学式).
(5)工业上合成氨的原料H2的制法是先把焦炭与水蒸气反应生成水煤气,再提纯水煤气得到纯净的H2 , 提纯水煤气得到纯净的H2的化学方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com