
��10 �֣���֪����ͭ��ˮ��ˮ������л�ԭ�ԡ�ʵ�����Ʊ�����ͭ�����Cu(HCOO)2��4H2O�ݵ��������£�

�ش��������⣺
��1����ĥʱӦ�ý�����ԭ�Ϸ��ڣ����������ƣ� �У��Ʊ� Cu2(OH)2CO3ʱ��Ҫ�õ�70�桫80�����ˮ�ܽ�С�մ�͵����Ļ�����Ŀ���� ��
��2��д����С�մ����Ʊ� Cu2(OH)2CO3�����ӷ���ʽ ��ʵ�ʲ����е�С�մ��뵨�� �����ʵ���֮�ȴ��� 2��1��ԭ���� ��
��3������a �������� ��
��4��֤��Cu2(OH)2CO3�����Ѿ�ϴ�Ӹɾ���ʵ�鷽���� ��
��5��ʵ��������ˮ�Ҵ�ϴ�Ӳ����Ŀ���� ��
��1�����塢 �ӿ췴Ӧ���ʣ���ֹNaHCO3�ֽ� ��2��2Cu2+ + 4HCO3���� Cu2(OH)2CO3 +3CO2��+H2O
NaHCO3���ֽ⡢����NaHCO3����ά�ּ��� ��3������ ��4��ȡ�������һ��ϴ��Һ���Թ��У�����BaCL2��Һ��������������˵��ϴ�Ӹɾ���5�����ټ���ͭ����ʧ
��������
�����������1����ĥʱӦ�ý�����������������ĥ���Ʊ� Cu2(OH)2CO3ʱ��Ҫ�õ�70�桫80�����ˮ���ʵ�����¶ȿ��Լӿ췴Ӧ���ʣ����¶Ȳ���̫�ߣ�NaHCO3���ֽҪ��ֹNaHCO3�ֽ⡣��2���������е���ϢС�մ�͵����Ƿ�Ӧ���Cu2(OH)2CO3��CO2���ɣ���Ӧ�����ӷ���ʽΪ��2Cu2+ + 4HCO3����Cu2(OH)2CO3 +3CO2��+H2O��NaHCO3Ҫ������ΪNaHCO3�ֽ⣬������ʧ����ӦҪ�ڼ�����Һ�н��У�����NaHCO3����ά�ּ��ԡ���3������a�Ƿ��뾧�����Һ�������ǹ��ˡ���4�����ݷ�ӦԪ���غ㿴��Cu2(OH)2CO3��������Na2SO4���ʣ���֤������ϴ�Ӹɾ����Լ���ϴ��Һ���Ƿ���SO42- ���ɣ�ʵ�鷽���ǣ�ȡ�������һ��ϴ��Һ���Թ��У�����BaCl2��Һ��������������˵��ϴ�Ӹɾ�����5������ͭ���Ҵ����ܽ�ȱ���ˮ��ҪС��ʵ��������ˮ�Ҵ�ϴ�ӿ��Լ��ټ���ͭ����ʧ��
���㣺����������Ļ������ⷽ�������ӷ���ʽ����д�����ʷ��뷽����
��������� ����1�����ʵķ��롢���Ӻ��ᴿ ����2�����ʵļ���ͼ��� ��������

 ȫ�ܲ��һ���þ�ϵ�д�
ȫ�ܲ��һ���þ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�걱����ʯ��ɽ��������ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���л�ѧ������ȷ����
A��CO2�Ľṹʽ��O=C=O
B�������Ǻ͵��۵�ʵ��ʽ��Ϊ��CH2O
C��N2H4�ĵ���ʽ��
D���۱�ϩ�Ľṹ��ʽ��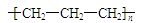
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ��ׯ�и�����ѧ�ڿ�ѧ������Ծ����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���ڼס���װ�õ�������������ȷ����

A���׳���ͨ����ļ��Ǹ�������Һ��Na+��Pt�缫�ƶ�
B��C�缫�ĵ缫��ӦΪ��O2+4e-+4H+==2H2O
C���ҳ��е��ܷ�ӦΪ��Cu+H2SO4 H2
H2 +CuSO4
+CuSO4
D����Ӧ�����У��ס���װ������Һ��pH����С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ�����и�����һ��ģ�⿼�������ۺϻ�ѧ�Ծ��������棩 ���ͣ������
ѡ��(12��)����ѧ�����л���ѧ������

�ش��������⣺
��1��A������Ϊ________��
��2��B��C�ķ�Ӧ����Ϊ________��E��F�ķ�Ӧ����Ϊ________��
��3��D�Ľṹ��ʽΪ________��
��4��������������G��ͬ���칹����________�֣����к˴Ź�������Ϊ5����Ϊ__________��д�ṹ��ʽ����
����ʹ FeCl3��Һ����ɫ��
�ڱ�����ֻ��2��ȡ������
��lmol�������Ƕ������3molNaOH��
��5��G��H�Ļ�ѧ����ʽΪ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ�����и�����һ��ģ�⿼�������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��������װ�÷ֱ�������ʵ�飬�ܴﵽʵ��Ŀ�ĵ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���㽭ʡ�����и�����ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij��Һ�п��ܺ���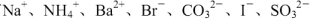 ��ij��ȤС��Ϊȷ������Һ����ɣ�����������ʵ�飺ȡ�����μ�������ˮ�������ݲ�������Һ�ʳ�ɫ�����ɫ��Һ�м�BaCl2��Һ����۾������Ա仯������˵����ȷ����
��ij��ȤС��Ϊȷ������Һ����ɣ�����������ʵ�飺ȡ�����μ�������ˮ�������ݲ�������Һ�ʳ�ɫ�����ɫ��Һ�м�BaCl2��Һ����۾������Ա仯������˵����ȷ����
A����Һ��һ������Na+��I����CO32��
B����Һ��һ�������ڵ�ֻ��I����SO32��
C��ֻ���ٽ���һ��ʵ�飬�Ϳ���ȫȷ����Һ�����
D����Һ��һ������Br����CO32�������ٴ���Na+��NH4+�е�һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���㽭ʡ�����и�����ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ȷ����
A������NO2����ˮ��Ӧ�������ᣬ�� NO2����������������
B��ij����ֻ��N��H ����Ԫ�أ�������֮��Ϊ14�U3���������һ��Ϊ������
C���������Ȼ��������Ϻ����ɵ�NH4Cl�����ӻ������˸÷�ӦΪ���ӷ�Ӧ
D��Na2O ����ˮ������Һ�ܵ��磬�ݴ˿��ж� Na2O���ڵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ��̨�и�����ѧ��һģ��ϲ��������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£���20.00mL0.1000mol��L��1(NH4)2SO4��Һ����μ���0.2000mol��L��1NaOH��Һʱ����Һ��pH������NaOH��Һ����Ĺ�ϵ����ͼ��ʾ��������NH3��H2O�ķֽ⣩������˵������ȷ����

A����a��ʾ��Һ�У�c(NH4+)��c(SO42��)��c(H+)��c(OH��)
B����b��ʾ��Һ�У�c(NH4+)��c(Na��)��c(H��)��c(OH��)
C����c��ʾ��Һ�У�c(NH4+)+c(H+)+ c(Na��)��c(OH��)+2c(SO42��)
D����d��ʾ��Һ�У�c(NH4+)+c(NH3��H2O)= 0.1000mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��㶫ʡ��ɽ�и�����ѧ�ڵڶ���ģ�⿼�������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪��Fe2O3 (s)�� C(s)=
C(s)=  CO2(g)��2Fe(s) ��H=234.1kJ��mol��1
CO2(g)��2Fe(s) ��H=234.1kJ��mol��1
C(s)��O2(g)=CO2(g) ��H=��393.5kJ��mol��1 ��2Fe(s)�� O2(g ) = Fe2O3(s) �ġ�H��
O2(g ) = Fe2O3(s) �ġ�H��
A����824.4kJ��mol��1 B����627.6kJ��mol��1
C����744.7kJ��mol��1 D����169.4kJ��mol��1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com