
选做(12分)【化学——有机化学基础】

回答下列问题:
(1)A的名称为________。
(2)B→C的反应条件为________,E→F的反应类型为________。
(3)D的结构简式为________。
(4)符合下列条件G的同分异构体有________种,其中核磁共振氢谱为5组峰的为__________(写结构简式)。
①能使 FeCl3溶液显紫色;
②苯环上只有2个取代基;
③lmol该物质是多可消耗3molNaOH。
(5)G→H的化学方程式为________。
(1)2-甲基-1-丙烯
(2)NaOH水溶液、加热;取代反应
(3)(CH3)2CHCHO 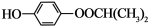
(4)6;
(5)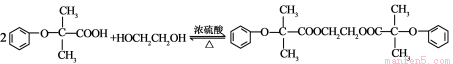 +2H2O
+2H2O
【解析】
试题分析:由已知条件I可知,烃A为烯烃,逆推:H是G与乙二醇发生酯化反应得到的产物,那么H水解可得G;G是F与苯酚钠反应得到的,那么在F的结构中既有-Br,又有-COOH;F是E在Br2和红磷的条件下反应得到的,由已知条件II可知此处发生了取代反应,那么E为含四个碳原子的羧酸;E是D氧化得到的,则D为醛,且结构式为(CH3)2CHCHO;还原后得到醇,即为C,烯烃A与HBr和过氧化物发生反马氏加成,故B为卤代烃,水解后得到醇,所以可知A为2-甲基-1-丙烯,B→C的反应为卤代烃的水解反应,条件为NaOH水溶液、加热;E→F为取代反应;符合条件①能使FeCl3溶液显紫色,说明结构中含有酚羟基;②苯环上只有2个取代基;③lmol该物质是多可消耗3molNaOH,说明结构中要有-OOCCH(CH3)2或-OOCCH2CH2CH3结构,含有这两种结构的有机物均有邻、间、对的结构,所以G的同分异构体有6种,其中核磁共振氢谱为5组峰的为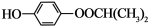 ;G→H为酯化反应,反应方程式为
;G→H为酯化反应,反应方程式为
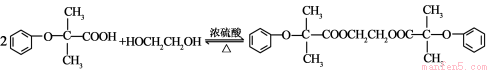 +2H2O。
+2H2O。
考点:有机化合物的性质、结构、同分异构体
考点分析: 考点1:有机化学知识综合应用 试题属性

 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源:2014-2015学年北京市石景山区高三上学期期末考试化学试卷(解析版) 题型:选择题
利用下图装置进行实验(必要时可加热),不能得出相应结论的是
溶液① | 固体② | 溶液③ | 实验结论 |
| |
A | 稀硫酸 | Na2CO3 | Na2SiO3 | 非金属性:C>Si | |
B | 浓盐酸 | MnO2 | Na2S | 氧化性:Cl2>S | |
C | 盐酸 | CaCO3 | C6H5ONa | 酸性:碳酸>苯酚 | |
D | 稀硫酸 | Na2CO3 | CaCl2 | CO2不与氯化钙反应 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市海淀区高三年级3月适应性训练理综化学试卷(解析版) 题型:选择题
已知反应:2NO2(红棕色) N2O4(无色)△H<0。将一定量的NO2充入注射器中后封口,下图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是
N2O4(无色)△H<0。将一定量的NO2充入注射器中后封口,下图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是


A.b点的操作是压缩注射器
B.c点与a点相比,c(NO2)增大,c(N2O4)减小
C.若不忽略体系温度变化,且没有能量损失,则T(b)>T(c)
D.d 点:v(正)>v(逆)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省枣庄市高三下学期开学初检测试卷理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的数值,下列说法正确的是
A.10gNH3含有4NA个电子
B.0.1mol铁和0.1mol铜分别与0.1 mol氯气完全反应,转移的电子数均为0.2NA
C.标准状况下,22.4 L H2O中分子数为NA 个
D.1L 0.1 mol·L-1Na2CO3 溶液中含有 0.1NA个CO32-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省文登市高三第二次统考理科综合化学试卷(解析版) 题型:选择题
等质量的氯气与下列足量物质反应,转移的电子数最少的是
A.冷的NaOH溶液 B.SO2的水溶液
C.FeCl2溶液 D.铜
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省菏泽市高三第一次模拟考试理科综合化学试卷(解析版) 题型:选择题
原子结构决定元素的性质,下列说法中,正确的是
A.Na、Al、Cl的原子半径依次减小,Na+、Al3+、Cl-的离子半径也依次减小
B.在第VIA族元素的氢化物(H2R)中,热稳定性最强的其沸点也最高
C.第2周期元素的最高正化合价都等于其原子的最外层电子数
D.非金属元素的非金属性越强,其氧化物对应水化物的酸性也一定越强
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省宁波市高三上学期期末考试化学试卷(解析版) 题型:填空题
(10 分)已知甲酸铜遇水易水解而具有还原性。实验室制备甲酸铜晶体[Cu(HCOO)2·4H2O]的流程如下:

回答下列问题:
(1)研磨时应该将固体原料放在(填仪器名称) 中;制备 Cu2(OH)2CO3时需要用到70℃~80℃的热水溶解小苏打和胆矾的混合物,其目的是 。
(2)写出用小苏打、胆矾制备 Cu2(OH)2CO3的离子方程式 ;实际操作中的小苏打与胆矾 的物质的量之比大于 2∶1,原因是 。
(3)操作a 的名称是 。
(4)证明Cu2(OH)2CO3沉淀已经洗涤干净的实验方法是 。
(5)实验中用无水乙醇洗涤产物的目的是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省宁波市高三上学期期末考试化学试卷(解析版) 题型:选择题
美日三位科学家曾因对“有机物合成过程中钯催化交叉偶联”的研究获诺贝尔化学奖。评审委员会认定这项研究成果可以大大提升合成复杂化学物质的可能性。钯的化合物氯化钯可用来检测有毒气体CO,发生反应的化学方程式为:CO+PdCl2+H2O=CO2+Pd↓+2HC1。对该反应的下列说法正确的是
A.CO作氧化剂,具有氧化性
B.HCl是还原产物
C.反应中H2O 提供了氧原子,因此 H2O 是氧化剂
D.生成22.4 L CO2(标准状况)时,转移的电子数为2 mo1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省稳派教育高三一轮复习质量检测理科综合化学试卷(解析版) 题型:选择题
已知常温下CH3COOH的电离平衡常数为Ka ,常温下,向20mL 0.1 mol·L-1CH3COOH溶液中逐滴加入0.1 mol·L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。下列说法中正确的是

A. a点表示的溶液中由水电离出的H+浓度为1.0×10-3mol·L-1
B. b点表示的溶液c(CH3COO-)< c(Na+)
C. b、d点表示的溶液中 相等
相等
D. c点表示CH3COOH和NaOH恰好反应完全
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com