
【题目】社会在飞速发展,环境问题也备受关注,如何减少污染,寻求清洁能源是现代学者研究的方向。
Ⅰ、为了模拟汽车尾气在催化转化器内的工作情况
(1)控制条件,让反应在恒容密闭容器中进行如下反应:2NO(g)+2CO(g) ![]() N2(g)+2CO2(g),用传感器测得不同时间NO和CO的浓度如下表:
N2(g)+2CO2(g),用传感器测得不同时间NO和CO的浓度如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)(10-4mol/L) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
c(CO)(10-3mol/L) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
前2s内的平均反应速率v(N2)=_______
(2)用氨气催化氧化还原法脱硝(NOx)
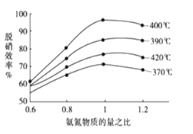
①根据下图 (纵坐标是脱硝效率、横坐标为氨氮物质的量之比),判断提高脱硝效率的最佳条件是:___。
②已知: N2(g)+O2(g)=2NO(g)△H=+akJ/mol
N2(g)+3H2(g) ![]() 2NH3(g)△H=-bk/mol
2NH3(g)△H=-bk/mol
2H2(g)+O2(g)=2H2O(g)△H=-ckJ/mol其中a、b、c均为大于0。
则放热反应:4NO(g)+4NH3(g)+O2(g) ![]() 4N2(g)+6H2O(g)△H=________。
4N2(g)+6H2O(g)△H=________。
Ⅱ、甲醇是一种很好的燃料
(1)在压强为0.1MPa条件下,a mol CO与3a mol H2的混合气体在催化剂作用下能自发反应生成甲醇:CO(g)+2H2(g)CH3OH(l) △H<0 。为了寻找合成甲醇的适宜温度和压强,某同学设计了三组实验,部分实验条件已经填在了下面的实验设计表中.
实验编号 | T(℃) | n(CO)/n(H2) | P(MPa) |
① | 180 | 2:3 | 0.1 |
② | n | 2:3 | 5 |
③ | 350 | m | 5 |
表中剩余的实验数据:n=________,m=________.
(2)CH3OH燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。下列说法正确的是______________(填序号)。
①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗6.4 g CH3OH转移1.2 mol电子
④负极反应式为CH3OH+8OH--6e-=CO32-+6H2O
【答案】1.875×10-4mol·L-1·s-1 400℃,氨氮物质的量之比为1 -(2a-2b+3c)kJ/mol或(2b-2a-3c)kJ/mol 180 2:3 ②③④
【解析】
I(1)v=![]() c/
c/![]() t;
t;
(2)①根据图像可知,脱硝效率最高时,效果最佳;
②根据盖斯定律,进行计算即可;
II(1)参数对比时,只改变一个量,其余量相同;
(2)甲醇燃料电池,甲醇为负极,氧气为正极,电解质溶液为碱性,有机物中的碳生成碳酸根离子;
I(1)
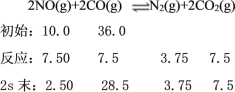
v(N2)=3.75![]() 10-4/2 mol·L-1·s-1=1.875×10-4mol·L-1·s-1;
10-4/2 mol·L-1·s-1=1.875×10-4mol·L-1·s-1;
(2)①根据图像可知,温度在400℃时,氨氮物质的量之比为1:1时脱硝效率为95%作用,效果最佳;
②根据盖斯定律,①N2(g)+O2(g)=2NO(g)△H=+akJ/mol,②N2(g)+3H2(g) ![]() 2NH3(g)△H=-bk/mol,③2H2(g)+O2(g)=2H2O(g)△H=-ckJ/mol,③
2NH3(g)△H=-bk/mol,③2H2(g)+O2(g)=2H2O(g)△H=-ckJ/mol,③![]() 3-②
3-②![]() 2-①
2-①![]() 2,可得到4NO(g)+4NH3(g)+O2(g)
2,可得到4NO(g)+4NH3(g)+O2(g) ![]() 4N2(g)+6H2O(g),则△H=-(2a-2b+3c)kJ/mol或(2b-2a-3c)kJ/mol;
4N2(g)+6H2O(g),则△H=-(2a-2b+3c)kJ/mol或(2b-2a-3c)kJ/mol;
II(1)探究不同温度或压强下合成甲醇的适宜条件时,参考数据具有可比性,则温度或压强不同时,其余条件相同,故n=180℃,m=2:3;
(2)①电池放电时通入空气的电极得电子,化合价降低为正极,①错误;
②电池放电时,电解质溶液中的氢氧根离子与生成的二氧化碳反应生成碳酸根离子,碱性逐渐减弱,②正确;
③电池放电时每消耗6.4 g CH3OH即反应0.2mol,碳的化合价由-2变为+4,转移1.2 mol电子,③正确;
④负极反应式为CH3OH+8OH--6e-===CO32-+6H2O,④正确。


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]化合物J是制备降血脂药贝利贝特的中间体,制备J的一种合成路线设计如下:
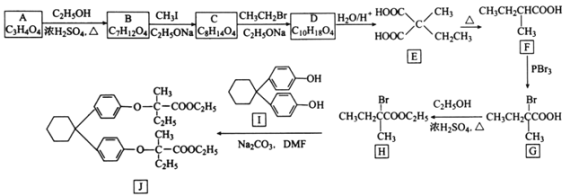
回答下列问题:
(1)A的化学名称是________________。
(2)G生成H的反应类型是________________;J的分子式为________________。
(3)C的结构简式为________________________。
(4)化合物I可由芳香化合物C6H6O和环状化合物C6H10O在醋酸和盐酸催化下制备得到,该反应的化学方程式为________________________________________。
(5)R与E互为同分异构体且与E具有相同的官能团种类和数目,则R的结构有________种。其中对应的核磁共振氢谱图中有四组峰,且峰面积比为4:3:2:1的结构简式为________。
(6)苯氧乙酸乙酯(![]() )是一种农药,设计由苯酚和乙醇为起始原料制备苯氧乙酸乙酯的合成路线:________________(无机试剂任选)。
)是一种农药,设计由苯酚和乙醇为起始原料制备苯氧乙酸乙酯的合成路线:________________(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关铝及其铝的化合物用途错误的是
A.明矾可用作净水剂
B.Al2O3可用于制作耐火材料
C.Al(OH)3可用于治疗胃酸过多
D.铝制餐具可用于长时间存放酸性、碱性或咸的食物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图的转化关系判断下列说法正确的是(反应条件已略去)
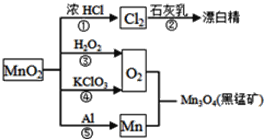
A. 反应⑤说明该条件下铝的还原性强于锰
B. 反应①②③④⑤均属于氧化反应和离子反应
C. 相同条件下生成等量的O2,反应③和④转移的电子数之比为1∶1
D. 反应①中氧化剂与还原剂的物质的量之比为1∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以淀粉为主要原料合成一种有果香味的物质C和化合物D的合成路线如下图所示。
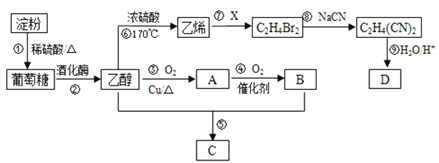
已知:![]()
请回答下列问题:
(1)A的结构简式为____________________,B分子中的官能团名称为__________________。
(2)反应⑦的化学方程式为___________________________,反应⑧的类型为______________。
(3)反应⑤的化学方程式为_____________________________。
(4)已知D的相对分子量为118,有酸性且只含有一种官能团,其中碳、氢两元素的质量分数分别为40.68%、5.08%,其余为氧元素,则D的结构简式为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】催化加氢可生成2-甲基戊烷的是
A. CH2=CHC(CH3)2CH2CH3 B. CH2=CHCH(CH3)C≡CH
C. (CH3)2C=C(CH3)2 D. (CH3)2CHCH2C≡CH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com