
【题目】学生为探究苯与溴发生反应的原理,用如图所示装置进行了实验。根据相关知识回答下列问题:

(1)实验开始时,关闭K2,开启K1和分液漏斗活塞,滴加苯和液溴的混合液,反应开始。过一会儿,在装置Ⅲ中可能观察到的现象是______________________________________。
(2)整套实验装置中能防止倒吸的装置有___________________________(填装置序号)。
(3)写出装置Ⅱ中发生反应的化学方程式:_____________________________________。
(4)本实验能不能用溴水代替液溴?___________________________________________。
(5)采用冷凝装置,其作用是_________________________________________________。
(6)Ⅲ装置中小试管内苯的作用是_____________________________________________。
【答案】小试管中有气泡,液体变棕黄色,有白雾出现,广口瓶内溶液中有浅黄色沉淀生成 III和IV; 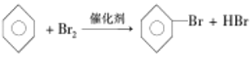 不能 防止溴和苯挥发,减少苯和液溴的损失,提高原料利用率 除去HBr中的Br2,防止干扰HBr的检验
不能 防止溴和苯挥发,减少苯和液溴的损失,提高原料利用率 除去HBr中的Br2,防止干扰HBr的检验
【解析】
(1)根据从冷凝管出来的气体为溴化氢,溴化氢不溶于苯,溴化氢遇空气中水蒸气形成酸雾,溴化氢能与硝酸银反应生成溴化银沉淀;
(2)根据装置III和IV中的导管没有与溶液接触,能防倒吸;
(3)根据溴与铁反应生成溴化铁,苯和液溴在溴化铁的催化作用下生成溴苯和溴化氢;
(4)液溴与苯反应,实际起催化作用的是溴化铁,如果用溴水代替,生成的溴化铁发生水解,起不到催化作用;
(5)溴和苯沸点低,易挥发;
(6)根据取代反应和加成反应的区别在于是否产生溴化氢。
(1)因从冷凝管出来的气体为溴蒸汽和溴化氢,溴化氢不溶于苯,溴化氢遇空气中水蒸气形成酸雾,溴化氢能与硝酸银反应生成溴化银沉淀,故现象是:小试管中有气泡,液体变棕黄色;有白雾出现;广口瓶内溶液中有浅黄色沉淀生成;
(2)装置III试管里苯与导管导管口接触,不会减小装置内的气体压强,所以可以防止发生倒吸;IV烧杯中,倒立的干燥管容积大,发生倒吸后,水上升到干燥管中,使烧杯中液面下降,上升的液体有在重力作用下回流到烧杯中,所以可以防止发生倒吸;
(3)溴与铁反应生成溴化铁:2Fe+3Br2 ═2FeBr3,苯和液溴在溴化铁的催化作用下生成溴苯和溴化氢:C6H6+Br2![]() C6H5Br+HBr;
C6H5Br+HBr;
(4)液溴与苯反应,实际起催化作用的是溴化铁,如果用溴水代替,生成的溴化铁发生水解,起不到催化作用,无法制取溴苯;
(5)苯与溴都容易挥发,所以需要采用冷凝装置,防止溴和苯挥发,减少苯和液溴的损失,提高原料利用率;
(6)如果发生取代反应会产生溴化氢,如果发生加成反应不会产生溴化氢。但挥发出的溴会干扰实验,而溴易溶于苯,溴化氢不溶于苯,小试管中的苯能除去HBr中的Br2,防止干扰HBr的检验。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】用示意图或图示的方法能够直观形象地将化学知识传授给学生,下列示意图或图示正确的是( )
A.砷原子的结构示意图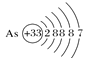 B.BF4—的结构式
B.BF4—的结构式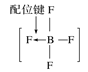
C.HF分子间的氢键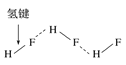 D.丙氨酸的手性异构
D.丙氨酸的手性异构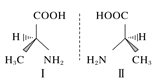
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组设计了如图甲所示的数字化实验装置,研究常温下,向1L0.1mol/LH2A溶液中逐滴加入等浓度NaOH溶液时的pH变化情况,并绘制出溶液中含A元素的粒子的物质的量分数与溶液pH的关系如图乙所示,则下列说法中正确的是( )


A.pH=4.0时,图中n(HA-)约为0.0091mol
B.0.1mol/LNaHA溶液中存在c(A2-)+c(HA-)+c(H2A)=0.1mol/L
C.该实验应将左边的酸式滴定管换成右边碱式滴定管并加酚酞作指示剂
D.常温下,等物质的量浓度的NaHA与Na2A溶液等体积混合后溶液pH=3.0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸铵是一种常见的强氧化剂,常用作火箭发射的推进剂。根据下列信息回答问题:
已知:①高氯酸铵受热分解为N2、Cl2、O2和H2O;②Mg3N2易水解;③Cu与N2在酒精灯加热条件下不反应。
(1)写出高氯酸铵受热分解的化学反应方程式: _____________,Mg3N2的电子式为________。
(2)现有23.5g NH4ClO4分解,用下列装置设计实验,验证其分解产物并计算分解率。(注:①装置中空气已除尽;②装置可重复使用;③B~F装置中的试剂均过量且能与相应物质反应完全。)
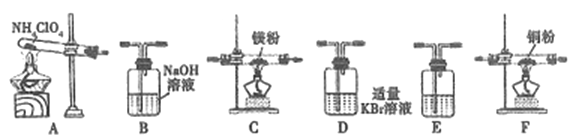
①用E装置质量的增加来验证生成的气体产物之一,则E中盛放的试剂是:_______。
②请按气流由左至右的方向连接装置:A →E→D →B→______→_____→_______→E (选择B~F装置,并用B~F字母填空)。
③证明产物中有Cl2的实验现象:________。
④反应结束后,若C装置质量增加了2.38g,则NH4ClO4的分解率是:________%。
(3)样品中NH4ClO4的含量(杂质中不含NH4+)还可用蒸馏法测定(如图所示,加热和夹持装置已略去),实验步骤如下:

步骤1:组装仪器,检查气密性;准确称取样品a g(不超过0.5g)于蒸馏烧瓶中,加入约150mL水溶解。
步骤2:准确量取40.00mL 约0.1mol/L H2SO4于锥形瓶中。
步骤3:向蒸馏烧瓶中加入20mL 3mol/L NaOH溶液;加热蒸馏使NH3全部挥发。
步骤4:用新煮沸过的水冲洗冷凝装置2~3次,洗涤液并入锥形瓶中。
步骤5:向锥形瓶中加2~3滴甲基橙,用c mol/L NaOH标准溶液滴定至终点,消耗NaOH标准溶液V1 mL。
步骤6:重复实验2~3次。
回答下列问题:
①步骤2中,准确量取40.00ml H2SO4 溶液的玻璃仪器是: __________。
②为获得样品中NH4ClO4的含量,还需补充的实验是:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯的叙述正确的是( )
A.苯的分子式为C6H6,它不能使酸性KMnO4溶液褪色,属于饱和烃
B.从苯的凯库勒式(![]() )看,苯分子中含有碳碳双键,应属于烯烃
)看,苯分子中含有碳碳双键,应属于烯烃
C.在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应
D.苯分子为平面正六边形结构,6个碳原子之间的价键完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E 为原子序数依次增大的短周期元素。A、C处于同一主族,C、D、E 处于同一周期,E 原子的最外层电子数是 A、B、C原子最外层电子数之和。A、B 组成的常见气体 X 能使湿润的红色石蕊试纸变蓝;D 的单质既能与C元素最高价氧化物的水化物的溶液反应生成盐,也能与A、E 形成的化合物的水溶液反应生成盐。下列说法正确的是( )
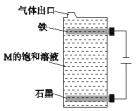
A.原子半径的大小顺序:C>D>E>A>B
B.C、E组成的化合物M 用右图装置进行电解能得到大量的 E 单质
C.元素B、E的最高价氧化物对应的水化物的酸性:B>E
D.C元素的氧化物中阴、阳离子数目之比为1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积一定的密闭容器中,置入一定量的NO(g)和足量C(s),发生反应C(s)+2NO(g) ![]() CO2(g)+N2(g),平衡状态时NO(g)的物质的量浓度[NO]与温度T的关系如图所示。则下列说法中正确的是( )
CO2(g)+N2(g),平衡状态时NO(g)的物质的量浓度[NO]与温度T的关系如图所示。则下列说法中正确的是( )

A. 该反应的ΔH>0
B. 若该反应在T1、T2时的平衡常数分别为K1、K2,则K1<K2
C. 在T2时,若反应体系处于状态D,则此时一定有v正<v逆
D. 在T3时,若混合气体的密度不再变化,则可以判断反应达到平衡状态C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种新型非氯高效消毒剂,微溶于KOH溶液,热稳定性差。实验室制备高铁酸钾的原理为3Cl2+2Fe(OH)3+10KOH==2K2FeO4+6KCl++8H2O。下列实验设计不能达到实验目的的是
A.用图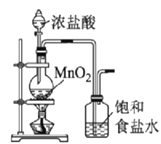 所示装置制备并净化氯气
所示装置制备并净化氯气
B.用图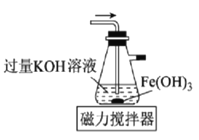 所示装置制备高铁酸钾
所示装置制备高铁酸钾
C.用图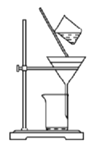 所示装置分离出高铁酸钾粗品
所示装置分离出高铁酸钾粗品
D.用图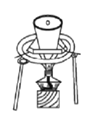 所示装置干燥高铁酸钾
所示装置干燥高铁酸钾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水合肼(N2H4·H2O)可用作抗氧剂等,工业上常用尿素[CO(NH2)2]和 NaClO溶液反应制备水合肼。
已知:Ⅰ.N2H4·H2O 的结构如图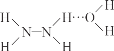 (…表示氢键)。
(…表示氢键)。
Ⅱ.N2H4·H2O 沸点 118 ℃,具有强还原性。
(1)将 Cl2 通入过量 NaOH 溶液中制备 NaClO,得到溶液 X,离子方程式是__。
(2)制备水合肼:将溶液 X 滴入尿素水溶液中,控制一定温度,装置如图 a(夹持及控温装置已略)。充分反应后,A 中的溶液经蒸馏获得水合肼粗品后,剩余溶液再进一步处理还可获得副产品 NaCl 和Na2CO3·10H2O。

①A 中反应的化学方程式是__。
②冷凝管的作用是__。
③若滴加 NaClO 溶液的速度较快时,水合肼的产率会下降,原因是__。
④NaCl 和 Na2CO3 的溶解度曲线如图 b。由蒸馏后的剩余溶液获得 NaCl 粗品的操作是__。
(3)水合肼在溶液中可发生类似 NH3·H2O 的电离,呈弱碱性;其分子中与 N 原子相连的 H 原子易发生取代反应。
①水合肼和盐酸按物质的量之比 1∶1 反应的离子方程式是__。
②碳酰肼(CH6N4O)是目前去除锅炉水中氧气的最先进材料,由水合肼与 DEC( ![]() )发生取代反应制得。碳酰肼的结构简式是__。
)发生取代反应制得。碳酰肼的结构简式是__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com