
【题目】下图是元素周期表的一部分,A、B、C、D、E、X 是元素周期表给出元素组成的常见单质或化合物。已知 A、B、C、D、E、X 存在如图所示转化关系(部分生成物和反应条件略去)。

(1)若 E 为氧化物,则 A 与水反应的方程式为____ ___,该反应中氧化剂和还原剂物质的量之比为__________ 。
①当 X 为碱性盐溶液,C 分子中有 22 个电子时,D 是__________(写化学式)。
②当 X 为金属单质时,X 与足量 B 的稀溶液反应生成 C 的离子方程式为________ __,写出检验生成物 C 的阳离子所用试剂的电子式__________。
(2)若 E 为单质气体,D 为白色沉淀,A 可能是________(写化学式), X是_______(写化学式)。
【答案】(1)3NO2+H2O = 2HNO3+NO 1 : 2 ① NaHCO3
②Fe+4H++NO3-= Fe3++NO↑+2H2O![]() (2)Na、Na2O2、NaH ;AlCl3或Al(NO3)3
(2)Na、Na2O2、NaH ;AlCl3或Al(NO3)3
【解析】试题分析:根据元素在周期表中的位置可判断元素的种类,①为H元素,②为Na元素,③为Al元素,④为C元素,⑤为N元素,⑥为O元素,⑦为Cl元素。
(1)若E为氧化物,根据转化关系以及元素种类可知,A为NO2,B为硝酸,NO2与水反应生成硝酸和一氧化氮,反应的方程式为3NO2+H2O = 2HNO3+NO,该反应中氧化剂是NO2,还原剂是NO2,N元素的化合价由+4价降低到+2价,发生还原反应,有+4价升高到+5价,发生氧化反应,则氧化剂与化合价的物质的量之比为1:2。
①X 为碱性盐溶液,C 分子中有 22 个电子,则C为CO2,X为碳酸钠,硝酸与碳酸钠反应生成二氧化碳,碳酸钠与CO2反应生成碳酸氢钠,则D 是NaHCO3。
②X为金属单质时,由转化图可知,应为Fe与稀硝酸反应生成硝酸铁,X与B的稀溶液反应生成C的离子方程式为Fe+4H++NO3-= Fe3++NO↑+2H2O;检验Fe3+的试剂是KSCN溶液,KSCN的电子式为![]() 。
。
(2)根据转化关系以及元素种类,若E为单质气体,则E为氢气或氧气,A为Na或Na2O2、NaH等,B为NaOH,D为白色沉淀,D为Al(OH)3,由![]() ,可以推知X为铝盐,C为偏铝酸盐,所以X是 AlCl3或 Al(NO3)3。
,可以推知X为铝盐,C为偏铝酸盐,所以X是 AlCl3或 Al(NO3)3。


 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:
【题目】下列说法没有科学性错误的是 ( )
A. “白雪牌”漂白粉可令所有有色物质黯然失“色”,没有最白,只有更白
B. CO有毒,生有煤炉的居室,可放置数盆清水,这样可有效地吸收CO,防止煤气中毒
C. 氯化钙具有吸水性和潮解性,夏日里用它的水溶液喷洒柏油路,可有效地保护路面
D. 氯元素有毒,禁止放入口中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合理应用和处理氮的化合物,在生产生活中有重要意义。
(1)氧化—还原法消除氮氧化物的转化如下:![]()
①反应Ⅰ为:NO+O3=NO2+O2,生成11.2 L O2(标准状况)时,转移电子的物质的量是 mol。
②反应Ⅱ中,当n(NO2)∶n[CO(NH2)2]=3∶2时,反应的化学方程式是_____。
(2)硝化法是一种古老的生产硫酸的方法,同时实现了氮氧化物的循环转化,主要反应为:NO2(g)+SO2(g)![]() SO3(g)+NO(g) △H=-41.8 kJ·mol-1
SO3(g)+NO(g) △H=-41.8 kJ·mol-1
已知:2SO2(g)+O2(g)![]() 2SO3(g) △H=-196.6 kJ·mol-1,写出NO和O2反应生成NO2的热化学方程式 。
2SO3(g) △H=-196.6 kJ·mol-1,写出NO和O2反应生成NO2的热化学方程式 。
(3)尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料。
①以尿素为原料一定条件下发生反应:CO(NH2)2 (s) + H2O(l)![]() 2 NH3(g)+CO2(g) △H = +133.6 kJ/mol。该反应的化学平衡常数的表达式K= 。关于该反应的下列说法正确的是 (填序号)。
2 NH3(g)+CO2(g) △H = +133.6 kJ/mol。该反应的化学平衡常数的表达式K= 。关于该反应的下列说法正确的是 (填序号)。
a.从反应开始到平衡时容器中混合气体的平均相对分子质量保持不变
b.在平衡体系中增加水的用量可使该反应的平衡常数增大
c.降低温度使尿素的转化率增大
②密闭容器中以等物质的量的NH3和CO2为原料,在120 ℃、催化剂作用下反应生成尿素:CO2(g) +2NH3(g)![]() CO (NH2)2 (s) +H2O(g),混合气体中NH3的物质的量百分含量[(NH3)]随时间变化关系如图所示。则a点的正反应速率V(正)(CO2) b点的逆反应速率V(逆)(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是 。
CO (NH2)2 (s) +H2O(g),混合气体中NH3的物质的量百分含量[(NH3)]随时间变化关系如图所示。则a点的正反应速率V(正)(CO2) b点的逆反应速率V(逆)(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是 。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素R有如下反应:RO3-+5R-+6H+=3R2+3H2O,下列说法正确的是
A.元素R位于周期表中第ⅦA族
B.RO3-中的R只能被还原
C.R2在常温常压下一定是气体
D.每反应消耗1 mol RO3-,转移电子的物质的量为5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电子工业中,常用氯化铁溶液作为印刷电路铜板蚀刻液。请按要求回答下列问题:
(1)若向氯化铁溶液中加入一定量的澄清石灰水,调节溶液pH,可得红褐色沉淀,该反应的离子方程式为:______________________________________,该过程中调节溶液的pH为5,则c(Fe3+)为:____________mol·L-1。(己知:Ksp[Fe(OH)3]= 4.0×10-38)
(2)某探究小组设计如下线路处理废液和资源回收:
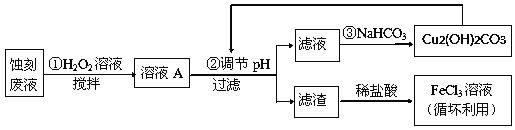
①用足量FeCl3溶液蚀刻铜板后的废液中含有的金属阳离子有:_______________。
②FeCl3蚀刻液中通常加入一定量的盐酸,其中加入盐酸的目的是:_________________。
③步骤①中加入H2O2溶液的目的是:______________________________________。
④已知:生成氢氧化物沉淀的pH
Cu(OH)2 | Fe(OH)2 | Fe(OH)3 | |
开始沉淀时 | 4.7 | 7.0 | 1.9 |
沉淀完全时 | 6.7 | 9.0 | 3.2 |
根据表中数据推测调节pH的范围是:________________。
⑤写出步骤②中生成CO2的离子方程式:__________(已知Cu2(OH)2CO3难溶于水)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸氯(C1NO)是有机合成中的重要试剂。可由NO与Cl2在通常条件下反应得到,化学方程式为2NO(g)+C12(g)![]() 2C1NO(g),
2C1NO(g),
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酸氯,涉及如下反应:
① 2NO2(g)+NaC1(s)![]() NaNO3(s)+ClNO(g) K1
NaNO3(s)+ClNO(g) K1
② 4NO2(g)+2NaC1(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g) K2
2NaNO3(s)+2NO(g)+Cl2(g) K2
③ 2NO(g)+C12(g)![]() 2C1NO(g) K3
2C1NO(g) K3
则K1,K2,K3之间的关系为K3=______________。
(2)已知几种化学键的键能数据如下表(亚硝酸氯的结构为Cl-N=O):

则2NO(g)+C12(g)![]() 2C1NO(g)反应的△H和a的关系为△H=________kJ/mol。
2C1NO(g)反应的△H和a的关系为△H=________kJ/mol。
(3)在1L的恒容密闭容器中充入2molNO(g)和1molC12(g),在不同温度下测得c(C1NO)与时间的关系如图A:

① 由图A可判断T1 ________T2,该反应的△H________0 (填“>”“<”或“=”)。
② 反应开始到10min时NO的平均反应速率v(NO)=____________mol/(L·min)。
③ T2时该反应的平衡常数K=____________。
(4) 一定条件下在恒温恒容的密闭容器中按一定比例充入NO(g)和Cl2(g),平衡时ClNO的体积分数随n(NO)/n(C12)的变化图象如图B,则A、B、C三状态中,NO的转化率最大的是________点。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知溶液中:还原性HSO3―>I―,氧化性IO3―>I2>>SO32―。向含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如下图所示,下列说法正确的是

A.a点反应的还原剂是NaHSO3,被氧化的元素是碘元素
B.b点反应的离子方程式是:3HSO3-+IO3-+3OH-=3SO42-+I-+3H2O
C.c点到d点的反应中共转移0.6mol电子
D.往200ml 1mol/LKIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式是:
5HSO3-+2IO3-=I2+5SO42-+3H++H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的固体废渣中主要含Cu和CuO,还含有少量Cu2O和SiO2等。利用该固体废渣制取Cu (NO3)2的部分工艺流程如图所示:

(1)Cu2O与稀硝酸反应的离子方程式为 。
(2)酸溶时,反应温度不宜超过70℃,其主要原因是 ,若保持反应温度为70℃,欲加快反应速率可采取的措施为 (写出一种即可)。
(3)过滤后所得废渣的主要成分的化学式为 。
(4) Cu(NO3)2晶体受热易分解成CuO,同时产生NO2和O2,该反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素的同位素![]() ,它的氯化物XCl21.11g溶于水配成溶液后,加入1mol/L的AgNO3溶液20mL恰好完全反应。若这种同位素原子核内有20个中子,求:
,它的氯化物XCl21.11g溶于水配成溶液后,加入1mol/L的AgNO3溶液20mL恰好完全反应。若这种同位素原子核内有20个中子,求:
(1)Z值和A值。
(2)X元素在周期表中的位置。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com