
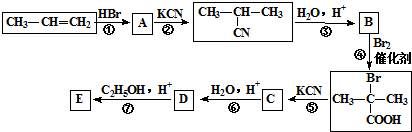
| H2O/H+ |
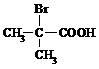 与足量NaOH溶液反应的化学方程式为
与足量NaOH溶液反应的化学方程式为 ,故A为
,故A为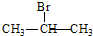 ,由信息R-CN水解得到RCOOH,可知B为
,由信息R-CN水解得到RCOOH,可知B为 ,B发生取代反应生成
,B发生取代反应生成 ,
, 与KCN发生取代反应生成C为
与KCN发生取代反应生成C为 ,C水解生成D为
,C水解生成D为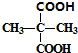 ,
,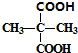 与足量的乙醇发生酯化反应生成E,则E为
与足量的乙醇发生酯化反应生成E,则E为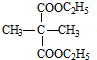 ,据此解答.
,据此解答. ,故A为
,故A为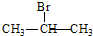 ,由信息R-CN水解得到RCOOH,可知B为
,由信息R-CN水解得到RCOOH,可知B为 ,B发生取代反应生成
,B发生取代反应生成 ,
, 与KCN发生取代反应生成C为
与KCN发生取代反应生成C为 ,C水解生成D为
,C水解生成D为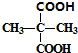 ,
,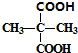 与足量的乙醇发生酯化反应生成E,则E为
与足量的乙醇发生酯化反应生成E,则E为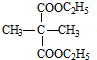 ,
,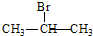 ,反应①是丙烯与HBr发生加成反应生成
,反应①是丙烯与HBr发生加成反应生成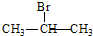 ,
,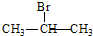 ,加成反应;
,加成反应;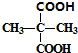 与足量的乙醇发生酯化反应生成
与足量的乙醇发生酯化反应生成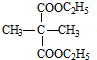 ,反应化学方程式为:
,反应化学方程式为: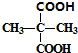 +2C2H5OH
+2C2H5OH| 浓硫酸 |
| △ |
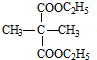 +2H2O,
+2H2O,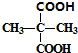 +2C2H5OH
+2C2H5OH| 浓硫酸 |
| △ |
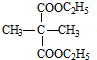 +2H2O;
+2H2O;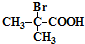 与足量NaOH乙醇溶液反应,发生卤代烃的水解溶液与羧酸的中和反应,反应方程式为:
与足量NaOH乙醇溶液反应,发生卤代烃的水解溶液与羧酸的中和反应,反应方程式为: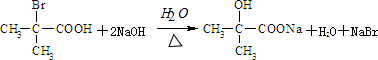 ,
,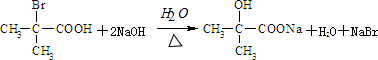 ;
; 的同分异构体有多种,其中既能发生银镜反应,又能发生酯化反应,说明分子中含有醛基-CHO与羟基-OH,符合结构的有机物为:HOCH2CH2CH2CHO、
的同分异构体有多种,其中既能发生银镜反应,又能发生酯化反应,说明分子中含有醛基-CHO与羟基-OH,符合结构的有机物为:HOCH2CH2CH2CHO、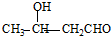 、CH3CH2CH(OH)CHO、HOCH2CH(CH3)CHO、
、CH3CH2CH(OH)CHO、HOCH2CH(CH3)CHO、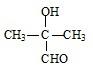 ,
,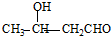 、CH3CH2CH(OH)CHO、HOCH2CH(CH3)CHO、
、CH3CH2CH(OH)CHO、HOCH2CH(CH3)CHO、 .
.


科目:高中化学 来源: 题型:
| A、5.0g C3H4中含有共用电子对的数目为NA |
| B、3.0 g淀粉和葡萄糖混合物中共含碳原子数为0.1NA |
| C、14 g乙烯和丙烯的混合物中含碳原子数为l.5NA |
| D、标准状况下,2.24L CHCl3含有的分子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| NaOH溶液 | 银氨溶液 | 新制Cu(OH)2悬浊液 | 金属钠 | |
| A | 中和反应 | - | 溶解 | 产生氢气 |
| B | - | 有银镜 | 加热后有砖红色沉淀 | 产生氢气 |
| C | 水解反应 | 有银镜 | 加热后有砖红色沉淀 | - |
| D | 水解反应 | - | - | - |
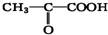 ),由以上事实推知乳酸的结构简式为
),由以上事实推知乳酸的结构简式为查看答案和解析>>
科目:高中化学 来源: 题型:
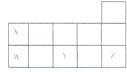
| A、YO2能使紫色石蕊试液先变红后褪色 |
| B、将W的氧化物溶于水可得W的含氧酸 |
| C、X的氢化物沸点比W的氢化物的沸点高 |
| D、Y的阴离子电子层结构与Z原子的相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B |
| C |
| A、B形成的单质存在同素异形体,C的单质不存在同素异形体 |
| B、C的最高价氧化物对应的水化物能与A的常见氢化物形成三种盐 |
| C、常温下,B的氢化物中无H+ |
| D、Y的种类比X多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 主族 周期 | ⅠA | 0族 | ||||||
| 一 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 二 | ② | ③ | ||||||
| 三 | ④ | ⑤ | ⑥ | |||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com