
【题目】同分异构现象是造成有机物种类繁多的重要原因之一。下列各组物质互为同分异构体的是
A.甲烷与丙烷B.CH2=CH2与CH3CH3C.蔗糖与麦芽糖D.纤维素与淀粉
 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】关于反应CaO + 3C→CaC2 + CO,下面哪种表述能最好地说明该反应是一个氧化还原反应
A.CaO失氧变为CaC2
B.C的状态发生了变化
C.Ca的化合价在反应前后发生了改变
D.C失去了电子,同时也得到了电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验原理或实验操作正确的是( )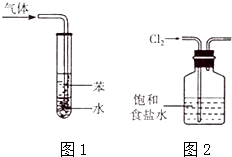
A.用pH试纸测量新制氯水的pH
B.用量筒量取 20mL 0.5000molL﹣1 H2SO4溶液于烧杯中,加水80mL,配制成0.1000molL﹣1H2SO4溶液
C.图1所示装置可用于吸收NH3或HC1气体,并防止倒吸
D.实验室用图2所示装置除去Cl2中的少量HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了提高煤的利用率,人们先把煤转化为CO和H2,再将它们转化为甲醇,某实验人员在一定温度下的密闭容器中,充入一定量的H2和CO,发生反应:
2H2(g)+CO(g)![]() CH3OH(g),测定的部分实验数据如下:
CH3OH(g),测定的部分实验数据如下:
t/s | 0 | 500 | 1 000 |
c(H2)/(mol·L-1) | 5.00 | 3.52 | 2.48 |
c(CO)/(mol·L-1) | 2.50 |
(1)在500 s内用H2表示的化学反应速率是 。
(2)在1 000 s内用CO表示的化学反应速率是 ,1 000 s时CO的转化率是 。
(3)在500 s时生成的甲醇的浓度是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组设计实验探究反应速率的测定和比较。
【实验目的】测定锌与稀硫酸反应的速率
【实验用品】锥形瓶、双孔塞、胶皮管、分液漏斗、直角导管、50mL注射器、铁架台、秒表、锌粒、1 mol/L硫酸、4 mol/L硫酸。
【实验步骤】
(1)取一套装置(如图所示),加入40 mL 1 mol/L的硫酸和锌粒,测量收集10 mL H2所需的时间。
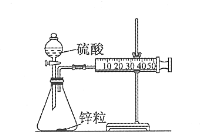
(2)取另一套装置,加入40 mL4 mol/L的硫酸和锌粒,测量收集10 mL H2所需的时间。
【实验现象】锌与稀硫酸反应 (写现象),收集10mL气体,(2)所用时间比(1)所用时间_________。
【实验结果】
加入试剂 | 反应时间 | 反应速率 |
40 mL 1 mol/L硫酸 | 长 | _________ |
40 mL 4 mol/L硫酸 | 短 | _________ |
【实验结论】4 mol/L硫酸与锌反应比1 mol/L硫酸与锌反应的速率 。
【注意事项】(1)锌的颗粒(即表面积)大小 ;
(2)40 mL的硫酸要迅速加入;
(3)装置 ,且计时要迅速准确;
(4)气体收集可以用排水量气装置(如图所示)代替。
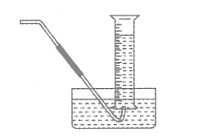
【实验讨论】除本实验测定反应速率的方法外,可行的方案还有(至少填两种):
(1) 。
(2) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中属于有机物的是( )
①乙醇 ②蛋白质 ③石墨 ④甲烷 ⑤蔗糖 ⑥碳酸 ⑦一氧化碳 ⑧碳酸钙 ⑨乙酸
A.①④⑤⑦⑧⑨B.①④⑤⑨C.①②④⑤⑨D.①②④ ⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物由碳、氢两种元素组成,其中含碳的质量分数为85.7%,在标准状况下11.2L此化合物的质量为14g,求此化合物的分子式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如图1所示装置分别进行探究实验(夹持装置已略去),请回答下列问题:
实验 | 药品 | 制取气体 | 量气管中的液体 |
Ⅰ | Cu、稀HNO3 | H2O | |
Ⅱ | NaOH固体、浓氨水 | NH3 | |
Ⅲ | Na2SO3固体、浓H2SO4 | SO2 | |
Ⅳ | 镁铝合金、NaOH溶液(足量) | H2 | H2O |
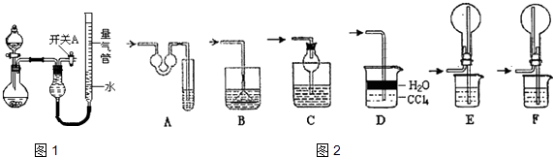
(1)实验过程中,使用分液漏斗滴加液体的操作是 .
(2)该同学认为实验I可通过收集并测量NO气体的体积来探究铜样品的纯度,你认为是否可行?(填“可行”或“不可行”).原因为
(3)实验Ⅲ烧瓶中产生的SO2气体通入溴水溶液中发生反应的离子方程式是 .
(4)实验Ⅱ中量气管中的液体最好是(填字母编号,下同).
a.浓NaOH溶液 b.氨水 c.煤油 d.氯化铵溶液
该实验剩余的NH3需吸收处理.如图2,以下各种尾气吸收装置中,适合于吸收NH3 , 而且能防止倒吸的有 .
(5)本实验应对量气管多次读数,读数时应注意:①将实验装置恢复到室温,② , ③视线与凹液面最低处相平.
(6)实验Ⅳ获得以下数据(所有气体体积已换算成标准状况,忽略滴入液体体积对气体体积的影响)
编号 | 镁铝合金度量 | 量气管第一次读数 | 量气管第二次读数 |
① | 1.0g | 10.0mL | 346.3mL |
② | 1.0g | 10.0mL | 335.0mL |
③ | 1.0g | 10.0mL | 345.7mL |
根据上述数据,可计算出镁铝合金中铝的质量分数为 . (H:1 Mg:24 Al:27)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】比较下列各组热化学方程式中ΔH的大小关系。
(1)S(s)+O2(g)===SO2(g) ΔH1
S(g)+O2(g)===SO2(g) ΔH2
ΔH1__________ΔH2
(2)CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH1
CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH2
ΔH1__________ΔH2
(3)4Al(s)+3O2(g)===2Al2O3(s) ΔH1
4Fe(s)+3O2(g)===2Fe2O3(s) ΔH2
ΔH1__________ΔH2
(4)煤作为燃料有2种途径:
途径1——直接燃烧:
C(s)+O2(g)===CO2(g) ΔH1<0
途径2——先制水煤气:
C(s)+H2O(g)===CO(g)+H2(g) ΔH2>0
再燃烧水煤气:
2CO(g)+O2(g)===2CO2(g) ΔH3<0
2H2(g)+O2(g)===2H2O(g) ΔH4<0
ΔH1、ΔH2、ΔH3、ΔH4的关系式是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com