
A、B、C、D、E、F是周期表中的前20号元素,原子序数逐渐增大。A元素是宇宙中含量最丰富的元素,其原子的原子核内可能没有中子。B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相等;C元素原子最外层p能级比s能级多1个电子;D原子p轨道上成对电子数等于未成对电子数;E的常见化合价为+3;F最高正价与最低负价的代数和为4;G+的M层电子全充满。用化学式或化学符号回答下列问题:
(1)G的基态原子的外围电子排布式为_______________________________________,周期表中属于________区。
(2)B与F形成的一种非极性分子的电子式为____________________________;F的一种具有强还原性的氧化物分子的VSEPR模型为________________。
(3)BD2在高温高压下所形成的晶胞如下图所示。该晶体的类型属于________(选填“分子”、“原子”、“离子”或“金属”)晶体。

(4)设C元素的气态氢化物为甲,最高价氧化物的水化物为乙,甲与乙反应的产物为丙。常温下,有以下3种溶液:①pH=11的甲的水溶液 ②pH=3的乙的水溶液 ③pH=3的丙溶液,3种溶液中水电离出的c(H+)之比为________________。
(5)丁、戊分别是E、F两种元素最高价含氧酸的钠盐,丁、戊溶液能发生反应。当丁、戊溶液以物质的量之比为1∶4混合后,溶液中各离子浓度大小顺序为____________________。
(6)A和C形成的某种氯化物CA2Cl可作杀菌剂,其原理为CA2Cl遇水反应生成一种具有强氧化性的含氧酸,写出CA2Cl与水反应的化学方程式:____________________________。
(7)往G的硫酸盐溶液中加入过量氨水,可生成一种配合物X,下列说法正确的是________。
A.X中所含化学键有离子键、极性键和配位键
B.X中G2+给出孤对电子,NH3提供空轨道
C.组成X的元素中第一电离能最大的是氧元素
D.SO 与PO
与PO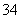 互为等电子体,空间构型均为正四面体
互为等电子体,空间构型均为正四面体
解析 由题意可推断:A:H,B:C,C:N,D:O,E:Al,F:S,G:Cu。(4)甲为NH3,乙为HNO3,丙为NH4NO3,水电离出来的H+浓度之比为:10-11∶10-11∶10-3=1∶1∶108。(5)丁为NaAlO2,戊为NaHSO4,当1∶4混合时,发生反应:
AlO +4H+===Al3++2H2O
+4H+===Al3++2H2O
1 4 1 0
c(Na+)>c(SO )>c(Al3+)>c(H+)>c(OH-)。
)>c(Al3+)>c(H+)>c(OH-)。
答案 (1)3d104s1 ds (2) 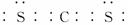 平面三角形 (3)原子 (4)1∶1∶108 (5)c(Na+)>c(SO
平面三角形 (3)原子 (4)1∶1∶108 (5)c(Na+)>c(SO )>c(Al3+)>c(H+)>c(OH-) (6)NH2Cl+H2O===HClO+NH3 (7)AD
)>c(Al3+)>c(H+)>c(OH-) (6)NH2Cl+H2O===HClO+NH3 (7)AD


 巧学巧练系列答案
巧学巧练系列答案 课课练江苏系列答案
课课练江苏系列答案科目:高中化学 来源: 题型:
Na、Cu、O、Si、S、Cl是常见的六种元素。
(1)Na位于元素周期表第________周期第________族;S的基态原子核外有________个未成对电子;Si的基态原子核外电子排布式为________________________。
(2)用“>”或“<”填空:
| 第一电离能 | 离子半径 | 熔点 | 酸性 |
| Si____S | O2-____Na+ | NaCl____Si | H2SO4____HClO4 |
(3)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101 kPa下,已知该反应每消耗1 mol CuCl(s),放热44.4 kJ,该反应的热化学方程式是________________________________________________________________________
________________________________________________________________________。
(4)ClO2常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某反应:A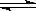 B + C 在室温下不能自发进行,在高温下能自发进行,对该反应过程△H、△S的判断正确的是( )
B + C 在室温下不能自发进行,在高温下能自发进行,对该反应过程△H、△S的判断正确的是( )
A.△H<0、△S<0 B.△H>0、△S<0
C.△H<0、△S>0 D.△H>0、△S>0
查看答案和解析>>
科目:高中化学 来源: 题型:
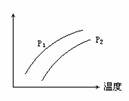
右图表示温度、压强对达平衡的可逆反应:2L(g) 2M(g)+N(g) △H>0的影响(P1<P2 ) 图中y轴表示的意义是 ( )
2M(g)+N(g) △H>0的影响(P1<P2 ) 图中y轴表示的意义是 ( )
A.混合物中L的百分含量
B.混合气体的密度
C.L的转化率
D.混合气体的平均分子量
查看答案和解析>>
科目:高中化学 来源: 题型:
在25 ℃时,有pH为x的盐酸和pH为y的NaOH溶液,取Vx L该盐酸同该NaOH溶液中和,需Vy L NaOH溶液。问:
(1)若x+y=14,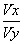 =___________(填数值);
=___________(填数值);
(2)若x+y=13,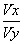 =__________(填数值);
=__________(填数值);
(3)若x+y>14,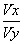 =____________________________________(表达式),
=____________________________________(表达式),
且Vx________Vy(填“>”、“<”或“=”)(题中x≤6,y≥8)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于金属及金属键的说法正确的是
A.金属键具有方向性与饱和性
B.金属键是金属阳离子与自由电子间的相互作用
C.金属导电是因为在外加电场作用下产生自由电子
D.金属具有光泽是因为金属阳离子吸收并放出可见光
查看答案和解析>>
科目:高中化学 来源: 题型:
肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如图所示。已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O===O为500、N—N为154,则断裂1 mol N—H键所需的能量(kJ)是
mol化学键所需的能量(kJ):N≡N为942、O===O为500、N—N为154,则断裂1 mol N—H键所需的能量(kJ)是

A.194 B.391
C.516 D.658
查看答案和解析>>
科目:高中化学 来源: 题型:
物质X的结构式如图所示,常被用于香料或作为饮料的酸化剂,在食品和医学上用作多价螯合剂,也是化学中间体。下列关于物质X的说法正确的是( )
A.X分子式C6H8O7
B.1 mol物质X可以和3 mol氢气发生加成
C.X分子内所有原子均在同一平面内
D.足量的X分别与等物质的量的NaHCO3、Na2CO3反应得到的气体物质的量相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com