
下列各组物质相互混合反应,既有气体生成,最终又有沉淀生成的是
①金属钠投入到FeCl3溶液 ②过量NaOH溶液和明矾溶液
③Ba(HCO3)2溶液和NaHSO4溶液 ④Na2O2投入FeCl3溶液
A.①④ B.②③④ C.②③ D.①③④
科目:高中化学 来源: 题型:
对于可逆反应4 NH3(g)+5O2(g)  4NO(g)+6 H2O(g)下列叙述正确的是
4NO(g)+6 H2O(g)下列叙述正确的是
A.达到化学平衡时,4v正(O2)= 5v逆(NO )
B.若单位时间内生成x mol NO,同时消耗x mol NH3 ,则反应达到平衡状态
C.达到化学平衡时,若缩小容器体积,则正反应速率减少,逆反应速率增大
D.在恒容容器中,若混合气体密度不再改变,则反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
下图所示是分离混合物时常用的仪器,从左至右,可以进行的混合物分离操作分别是




A.蒸馏、蒸发、分液、过滤 B.蒸馏、过滤、分液、蒸发
C.分液、过滤、蒸馏、蒸发 D.过滤、蒸发、分液、蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
海带中含碘元素,有人设计如下步骤来提取碘:①加入6%H2O2溶液 ②将海带烧成
灰,向灰中加入蒸馏水 ③加入CCl4振荡 ④过滤 ⑤用分液漏斗分液 ⑥加热煮沸
1~2分钟,合理的操作顺序为
A.②一⑥一④一①一③一⑤ B.②一①一⑥一③一④一⑤
C.②一①一③一⑥一⑤一④ D.②一③一①一⑥一⑤一④
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去)。则W、X不可能是


| 选项 | W | X |
| A | 盐酸 | Na2CO3溶液 |
| B | NaOH溶液 | AlCl3溶液 |
| C | CO2 | Ca(OH)2溶液 |
| D | Cl2 | Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某化学小组模拟“侯氏制碱法”,以NaCl、NH3、CO2和水等为原料以及下
某化学小组模拟“侯氏制碱法”,以NaCl、NH3、CO2和水等为原料以及下
图所示装置制取NaHCO3,反应的化学方程式为NH3+CO2+H2O+NaCl = NaHCO3↓+NH4Cl。
然后再将NaHCO3制成Na2CO3。Ks5u
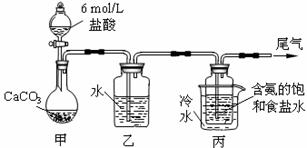 |
⑴ 装置乙的作用是 。为防止污染空
气,尾气中含有的 需要进行吸收处理。
⑵由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有 、
、 。NaHCO3转化为Na2CO3的化学方程式为 。
⑶若在⑵中灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热了t1 min
的NaHCO3 样品的组成进行了以下探究。
取加热了t1 min的NaHCO3样品29.6 g完全溶于水制成溶液,然后向此溶液中缓慢地滴
加稀盐酸,并不断搅拌。随着盐酸的加
入,溶液中有关离子的物质的量的变化
如右图所示。
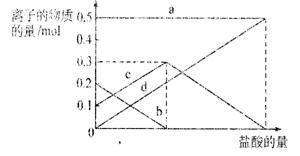
则曲线c对应的溶液中的离子是
(填离子符号);该样品中NaHCO3和
Na2CO3的物质的量之比是 。
⑷若取21.0 g NaHCO3固体,加热了t2 min后,剩余固体的质量为l4.8 g。如果把此剩余固体全部加入到200 mL 2 mol·L-1的盐酸中
则充分反应后溶液中H+ 的物质的量浓度为____________(设溶液体积变化忽略不计)。
查看答案和解析>>
科目:高中化学 来源: 题型:
溴及其化合物广泛应用于医药、农药、纤维、塑料组燃剂等,溴主要以Br-形式存在于海水中,海水呈弱碱性。回答下列问题:
(1)海水提溴过程中,向浓缩的海水中通入Cl2,将其中的Br-氧化,该过程的离子方程式为 ,再用空气吹出溴;然后用碳酸钠溶液吸收溴,溴歧化为Br-和BrO3-,其离子方程式为 。
(2)需要使用溴时,用硫酸酸化得到的Br-和BrO3-的混合物,而不用盐酸酸化混合物的原因可能是 。
(3)Cl2通入冷的石灰乳,用于制漂白粉,反应的化学方程式为
。
(4)为了除去工业Br2中微量的Cl2,可向工业Br2中 。
a.通入HBr b.加入Na2CO3溶液 c.加入NaBr溶液 d.加入Na2SO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
丙烯醇(CH2=CH—CH2OH)可发生的化学反应有( )
①加成 ②氧化 ③酯化 ④加聚 ⑤取代
A.只有①②③ B.只有①②③④ C.①②③④⑤ D.只有①③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com