
【题目】下列过程中涉及化学反应的是
A.通过“扫描隧道显微镜”操纵原子“书写”文字B.14C考古断代
C.煤焦油分馏得到苯及其同系物D.粮食酿酒
科目:高中化学 来源: 题型:
【题目】向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成沉淀Al(OH)3的量随AlCl3加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( ) 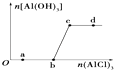
A.a点对应的溶液中:Na+、Fe3+、SO42﹣、HCO3﹣
B.b点对应的溶液中:Na+、S2﹣、SO42﹣、Cl﹣
C.c点对应的溶液中:K+、Ag+、Ca2+、NO3﹣
D.d点对应的溶液中:K+、NH4+、CO32﹣、SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“探险队员”﹣盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质或者是水溶液),盐酸必须避开它们,否则就无法通过. 
(1)在能“吃掉”盐酸的化学反应中,属于酸碱中和反应的有个,属于氧化还原反应的有个,其中能“吃掉”盐酸的盐是(填化学式),写出该反应的离子方程式 .
(2)在不能与盐酸反应的物质中,属于电解质的是(填写物质序号,下同),属于非电解质的是
(3)请你帮助它走出迷宫(用图中物质前的序号连接起来表示所走的路线)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是以高铁酸盐(K2FeO4)和锌为电极材料,具有能量密度大、体积小、重量轻、寿命长、无污染等优点,除比亚迪外目前还没有其他厂家宣称其产品可以大规模实用化.电池的总反应为:3Zn+2K2FeO4+8H2O ![]() 3Zn(OH)2+2Fe(OH)3+4KOH.下列说法正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH.下列说法正确的是( )
A.充电时阳极反应式为:Zn﹣2e﹣+2OH﹣=Zn(OH)2
B.0.1molK2FeO4发生反应,转移电子数约为1.806×1024
C.充电时K2FeO4发生氧化反应
D.放电时正极反应为:2FeO42﹣+6e﹣+8H2O=2Fe(OH)3+10OH﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用硫酸渣(主要含Fe2O3、FeO,杂质为Al2O3和SiO2等)生产铁基颜料铁黄(FeOOH) 的制备流程如图: 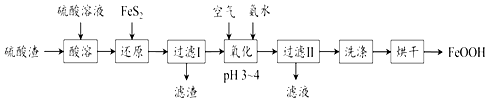
已知:FeS2难溶于水,不与H2SO4反应,在“还原”步骤中,Fe3+通过反应Ⅰ、Ⅱ被FeS2还原,其中反应Ⅰ为FeS2+14Fe3++8H2O═15Fe2++2SO42﹣+16H+;反应Ⅱ中氧化产物为单质硫.
(1)“酸溶”中硫酸要适当过量,目的是:①提高铁的浸出率;② .
(2)写出酸溶时硫酸渣中主要成分发生反应的一个化学方程式: .
(3)加入FeS2“还原”时反应Ⅱ的离子方程式为 . 滤渣的主要成分是FeS2、S和(填化学式)
(4)“氧化”时,生成FeOOH的离子方程式为 . 氧化时,温度不宜过高,否则会导致产品颜色偏红,可能含有的杂质是(填化学式).
(5)滤液中溶质是Al2(SO4)3和(填化学式).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实与胶体性质无关的是 ( )
A. 纳米科技的发展有赖于胶体的化学原理与方法
B. 三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀
C. 一束平行光线照射豆浆时,可看到光亮的通路
D. 万里长江流入大海处,形成长江三角沙洲
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式已配平):
![]() 试通过计算和推理完成下面的问题:
试通过计算和推理完成下面的问题:
(1)A物质可以导致酸雨的形成。A应该属于________(用字母代号填写)。
a. 酸 b. 碱 c. 盐 d. 酸性氧化物 e. 碱性氧化物
(2)A物质可以使酸性![]() 溶液褪色,此反应中(填写化学式,下同)_______失去电子,氧化剂是________。
溶液褪色,此反应中(填写化学式,下同)_______失去电子,氧化剂是________。
(3)足量的铜片与10mL 18mol/L的浓![]() 充分反应,如果该反应过程中转移了0.1mol电子,生成的
充分反应,如果该反应过程中转移了0.1mol电子,生成的![]() 的物质的量为_______mol,生成的A气体在标准状况下体积为________L(假设气体全部逸出)。
的物质的量为_______mol,生成的A气体在标准状况下体积为________L(假设气体全部逸出)。
(4)计算:将反应后得到的溶液与足量![]() 溶液混合,充分反应。反应后所得沉淀的质量为______g。
溶液混合,充分反应。反应后所得沉淀的质量为______g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在工业上常用CO和H2合成甲醇,反应方程式为:CO(g)+2H2(g)CH3OH(g)△H=akJ/mol
已知:①CO(g)+ ![]() O2(g)═CO2(g)△H1=﹣283.0kJ/mol
O2(g)═CO2(g)△H1=﹣283.0kJ/mol
②H2(g)+ ![]() O2(g)═H2O(g)△H2=﹣241.8kJ/mol
O2(g)═H2O(g)△H2=﹣241.8kJ/mol
③CH3OH(g)+ ![]() O2(g)═CO2(g)+2H2O(g)△H3=﹣192.2kJ/mol
O2(g)═CO2(g)+2H2O(g)△H3=﹣192.2kJ/mol
答下列问题:
(1)a=
(2)能说明反应CO(g)+2H2(g)CH3OH(g)已达平衡状态的是(填字母).
A.单位时间内生成1mol CH3OH(g)的同时消耗了1mol CO(g)
B.在恒温恒容的容器中,混合气体的密度保持不变
C.在绝热恒容的容器中,反应的平衡常数不再变化
D.在恒温恒压的容器中,气体的平均摩尔质量不再变化
(3)在T1℃时,体积为2L的恒容容器中充人物质的量之
和为3mol的H2和CO,反应达到平衡时CH3OH的体积分数(V%)与 ![]() 的关系如图1所示.
的关系如图1所示.
①当起始 ![]() =2,经过5min达到平衡,CO的转化率为0.6,则0~5min内平均反应速率v(H2)= . 若此时再向容器中加入CO(g)和CH3OH(g)各0.4mol,达新平衡时H2的转化率将(选填“增大”、“减小”或“不变”);
=2,经过5min达到平衡,CO的转化率为0.6,则0~5min内平均反应速率v(H2)= . 若此时再向容器中加入CO(g)和CH3OH(g)各0.4mol,达新平衡时H2的转化率将(选填“增大”、“减小”或“不变”);
②当 ![]() =3.5时,达到平衡状态后,CH3 OH的体积分数可能是图像中的点(选填“D”、“E”或“F”)
=3.5时,达到平衡状态后,CH3 OH的体积分数可能是图像中的点(选填“D”、“E”或“F”)
(4)CO和H2来自于天然气.已知CO2(g)+CH4 (g)2CO(g)+2H2 (g).在密闭容器中有浓度均为0.1molL﹣1的CH4与CO2 , 在一定条件下反应,测得CH4的平衡转化率与温度及压强的关系如图2,则压强p1p2(选填“大于”或“小于”);当压强为p2时,在y点:v(正)v(逆)(选填“大于”、“小于”或“等于”).若p2=3MPa,则T℃时该反应的平衡常数Kp=MPa2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数). 
(5)含有甲醇的废水会造成环境污染,可通入ClO2气体将其氧化为CO2 . 写出相关反应的离子方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光纤通讯是光导纤维传送信号的一种通讯手段,合成光导纤维及氮化硅(一种无机涂层)的工艺流程如图: 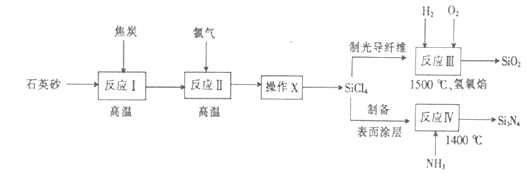
回答下列问题:
(1)反应I的化学方程式为 , 氧化剂为(填化学式).
(2)经反应II所得的四氯化硅粗品中所含的物质如表:
组分名称 | SiCl4 | SiHCl3 | SiH2Cl2 | HCl | BCl3 | PCl3 |
质量分数 | 0.545 | 0.405 | 0.0462 | 0.0003 | 0.00193 | 0.00157 |
沸点/℃ | 57.6 | 31.8 | 8.2 | ﹣85 | 12.5 | 75.5 |
图中“操作X”的名称为;PCl3的电子式为 .
(3)反应III和IV中尾气的用途为;反应IV的化学方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com