
【题目】化学计量在化学中占有重要地位,根据相关计算填空:
①3gHe是________ molHe,含有的质子数为_______个。
②1.204×1023个NH3含________mol氨分子,在标准状况下的体积为________L。
③29.4克硫酸中含有原子总数为________ mol,与_______克NH3含有相同数目的氢原子。
④在标准状况下,1.6g某气态氧化物RO2体积为0.56L,该气体的物质的量是________ ,摩尔质量是________ ,R的相对原子量为________ 。
⑤已知Wg气体A含有a个分子,那么在标准状况下,bg气体A所占的体积是________ (其中阿伏加德罗常数用NA表示)。
【答案】0.75mol 9.03×1023 0.2mol 4.48L 2.1 3.4 0.025mol 64g/mol 32 ![]()
【解析】
①He的相对原子质量是4,原子序数是2,所以根据公式![]() 和
和![]() 计算可知,3gHe含有0.75molHe原子,9.03×1023个质子;
计算可知,3gHe含有0.75molHe原子,9.03×1023个质子;
②根据公式![]() 和
和![]() 计算可知,1.204×1023个NH3即0.2mol,标况下的体积为4.48L;
计算可知,1.204×1023个NH3即0.2mol,标况下的体积为4.48L;
③1个H2SO4分子含有7个原子,根据公式![]() 可知,29.4g H2SO4即0.3mol,原子总计为2.1mol,其中含有氢原子0.6mol;含有 0.6mol氢原子的氨气,即0.2mol,根据公式
可知,29.4g H2SO4即0.3mol,原子总计为2.1mol,其中含有氢原子0.6mol;含有 0.6mol氢原子的氨气,即0.2mol,根据公式![]() 计算可知即为3.4g;
计算可知即为3.4g;
④根据公式![]() 可知,标况下0.56L的气体即0.025mol;根据公式
可知,标况下0.56L的气体即0.025mol;根据公式![]() 计算可知,气体的摩尔质量即为64g/mol;那么R的相对原子质量即为32;
计算可知,气体的摩尔质量即为64g/mol;那么R的相对原子质量即为32;
⑤bg气体所含的分子数为![]() ,根据公式
,根据公式![]() 和
和![]() 计算可知,bg气体A所占的体积即为:
计算可知,bg气体A所占的体积即为: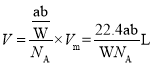 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子![]() 使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用
使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用![]() 表示
表示![]() 请认真观察如图,然后回答问题.
请认真观察如图,然后回答问题.

![]() 图中所示反应是______
图中所示反应是______![]() 填“吸热”或“放热”
填“吸热”或“放热”![]() 反应.
反应.
![]() 已知拆开1mol
已知拆开1mol![]() 键、1mol
键、1mol![]() 、1mol
、1mol![]() 键分别需要吸收的能量为436kJ、151kJ、
键分别需要吸收的能量为436kJ、151kJ、![]() 则由1mol氢气和1mol碘反应生成HI会______
则由1mol氢气和1mol碘反应生成HI会______![]() 填“放出”或“吸收”
填“放出”或“吸收”![]() ______kJ的热量
______kJ的热量![]() 在化学反应过程中,是将______转化为______.
在化学反应过程中,是将______转化为______.
![]() 下列反应中,属于放热反应的是______,属于吸热反应的是______.
下列反应中,属于放热反应的是______,属于吸热反应的是______.
![]() 物质燃烧
物质燃烧
![]() 炸药爆炸
炸药爆炸
![]() 酸碱中和反应
酸碱中和反应
![]() 二氧化碳通过炽热的碳
二氧化碳通过炽热的碳
![]() 食物因氧化而腐败
食物因氧化而腐败
![]() 与
与![]() 反应
反应
![]() 铁粉与稀盐酸反应.
铁粉与稀盐酸反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表述正确的是
A. 苯和氯气生成C6H6Cl6的反应是取代反应
B. 乙烯与溴水发生加成反应的产物是CH2CH2Br2
C. 等物质的量的甲烷与氯气反应的产物是CH3Cl
D. 硫酸作催化剂,CH3CO18OCH2CH3水解所得乙醇分子中有18O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】色酮类化合物K具有抗菌、降血脂等生理活性,其合成路线如图:

已知:① +HCl(R代表烃基)
+HCl(R代表烃基)
②![]() +R’OH
+R’OH![]() +RCOOH(R、R’代表烃基)
+RCOOH(R、R’代表烃基)
③ (R、R1、R2、R3、R4代表烃基)
(R、R1、R2、R3、R4代表烃基)
(1)A的结构简式是__;根据系统命名法,F的名称是__。
(2)B→C所需试剂a是__;试剂b的结构简式是__。
(3)C与足量的NaOH反应的化学方程式为__。
(4)G与新制Cu(OH)2反应的化学方程式为__。
(5)已知:①2H![]() J+H2O;②J的核磁共振氢谱只有两组峰。
J+H2O;②J的核磁共振氢谱只有两组峰。
以E和J为原料合成K分为三步反应,写出有关化合物的结构简式:

E:__;J:__;中间产物2:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“宏观-微观-符号”是学习化学的重要内容和方法。下列有关说法错误的是( )

A.甲乙容器中所给物质的组成微粒均为分子
B.甲乙容器可以得出结论为:凡是化学反应,反应前后分子总数不会发生变化
C.此反应后碳元素的化合价升高
D.图甲所示物质中碳、氢元素的质量比是3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某学生用98%的浓硫酸(密度为1.84 g/cm3)配制100 mL1mol/L的稀硫酸。其实验过程如下:
①该学生所用的98%的浓硫酸(密度为1.84 g/cm3)的物质的量浓度为_______;
②配制稀硫酸时所需要浓硫酸体积为_______mL,用_______量筒(“100 mL”或 “10 mL”)量取浓硫酸;
③将量取的浓硫酸沿烧杯内壁慢慢注入盛有约20mL水的烧杯里,并不断搅拌;
④将____________的上述溶液沿玻璃棒注入100 mL的容量瓶中,并用50mL蒸馏水分2~3次洗涤烧杯,洗涤液也注入容量瓶中,并摇匀;
⑤加水至距刻度线1~2cm时,改用_____________加水,使溶液凹液面跟刻度相平。
(2)该学生通过查阅资料可知,溶液的浓度还可用体积比法表示,如:1:10的硫酸就是将1体积的浓硫酸与10体积的水混合,计算体积比为1:10的硫酸的溶质质量分数为__________(列出计算式即可)。(已知:浓硫酸的质量分数为98%,密度为1.84 g/cm3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列说法中正确的是
A.2.4g金属镁变成镁离子时失去的电子数为0.1NA
B.标况下,mg气体A与ng气体B的分子数相同,则A、B两气体的密度之比为n∶m
C.含有NA个氦原子的氦气的体积约为11.2L
D.1.7gOH-中所含的电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. ![]() 的一溴代物和
的一溴代物和![]() 的一溴代物都有4种(不考虑立体异构)
的一溴代物都有4种(不考虑立体异构)
B. CH3CH=CHCH3分子中的四个碳原子在同一直线上
C. 按系统命名法,化合物 的名称是2,3,4-三甲基-2-乙基戊烷
的名称是2,3,4-三甲基-2-乙基戊烷
D. ![]() 与
与![]() 都是α-氨基酸且互为同系物
都是α-氨基酸且互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是( )
A. Cu2S(s)![]() Cu(s)
Cu(s)![]() CuCl2(s)
CuCl2(s)
B. SiO2(s)![]() H2SiO3(s)
H2SiO3(s)![]() Na2SiO3(aq)
Na2SiO3(aq)
C. Fe(s)![]() Fe2O3(s)
Fe2O3(s)![]() Fe2(SO4)3(aq)
Fe2(SO4)3(aq)
D. NaCl(aq)![]() Na2CO3(s)
Na2CO3(s)![]() NaOH(aq)
NaOH(aq)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com