
【题目】在化合物YX2和ZX2中,已知X、Y、Z都是前三周期的元素,X与Y同周期,Y与Z同主族,Y原子的最外层电子数是次外层电子数的2倍;X原子最外层上有6个电子。根据以上条件,回答问题:
(1)Y的原子结构示意图为___。
(2)YX2的结构式是___,分子内的共价键是___(填“极性键”或“非极性键”)。
(3)ZX2的化学式为___。
(4)用电子式表示YX2的形成过程___。
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源: 题型:
【题目】室温时,用0.0200mol/L稀盐酸滴定20.00mL0.0200mol/LNaY溶液,溶液中水的电离程度随所加稀盐酸的体积变化如图所示(忽略滴定过程中溶液的体积变化或密度变化),则下列有关说法正确的是()
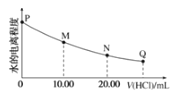
已知:K(HY)=5.0×10-11
A.M点溶液的pH>7
B.M点,c(Na+)=c(HY)+c(Y-)+c(Cl-)
C.可选取酚酞作为滴定指示剂
D.图中Q点水的电离程度最小,Kw<10-14
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.常温下,1.0L pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA
B.2.0g D216O和H218O混合物中含有的中子数目为0.9NA
C.标准状况下,22.4L HF中含有NA个HF分子
D.用惰性电极电解CuSO4溶液,若需加入98g Cu(OH)2才能使电解质溶液复原,则电解过程中转移电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】七水合硫酸镍为水绿色斜方棱形晶体,有甜味,俗称“翠矾”。某学习小组用含镍催化剂废渣(主要成分是镍单质,含少量铁、铝单质及其氧化物,以及少量难溶性杂质),制备七水合硫酸镍晶体,流程图如下:
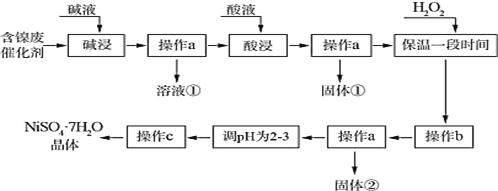
几种难溶碱开始沉淀和完全沉淀的 pH:
沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
开始沉淀 | 3.8 | 2.7 | 7.6 | 7.1 |
完全沉淀 | 5.2 | 3.2 | 9.7 | 9.2 |
回答下列问题:
(1)“碱浸”操作发生的离子方程式为____________。
(2)①“固体①”的主要成分是__________,双氧水作用为___________。
②如果加入双氧水量不足或“保温时间较短”,对实验结果的影响是_______________________,设计实验证明产品中是否含“杂质”:____________。(不考虑硫酸镍影响)
(3) “操作 b”中调节溶液 pH 范围是_________,“操作 c”之前,“调节 pH 为 2~3”的目的是_______。
(4) “操作 c”具体是指___________________、过滤、洗涤、干燥。
(5)取 4.000 g 硫酸镍晶体产品(NiSO4·7H2O)于锥形瓶中,加入足量的去离子水溶解,用0.2000 mol·L-1 的标准溶液EDTA(Na2H2Y)滴定至终点(发生Ni2++ H2Y2- = NiY2-+ 2H+ ),三次实验消耗标准液的体积分别为 69.10 mL、68.90 mL、59.00 mL,则产品纯度为_________%。(计算结果保留到小数点后 2 位,不考虑杂质反应)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期的三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和是5。X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和;Y元素原子的最外电子层上的电子数是它的电子层数的2倍,X和Z可以形成XZ3的化合物。请完成下列问题:
(1)Z元素的名称是___。
(2)XZ3化合物的化学式是___,电子式是__。
(3)分别写出X、Y的含氧酸的化学式__、__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.甲烷分子的比例模型为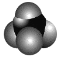 ,其二氯取代物有 2 种结构
,其二氯取代物有 2 种结构
B.苯和乙烯都能使溴水褪色,其褪色原理相同
C.相同质量的乙炔与苯分别在足量的氧气中完全燃烧,消耗氧气的物质的量相同
D.在一定条件下,乙烯与氢气反应生成乙烷属于取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由丙烯经下列反应制得F、G两种高分子化合物,它们都是常用的塑料。
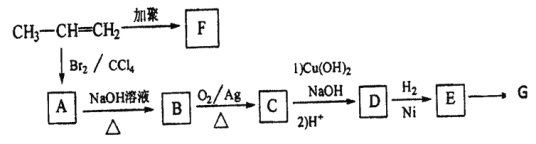
(1)F的结构简式为________。
(2)在一定条件下,两分子E能脱去两分子形成一种六元环状化合物,该化合物的结构简式为_______。
(3)①B→C 化学方程式为______。
②C与含有NaOH的Cu(OH)2悬浊液反应的化学方程式为______。
③E→G化学方程式为______。
(4)手性分子X为E的一种同分异构体,lmolX与足量金属钠反应产生lmol氢气,lmolX与足量银氨溶液反应能生成2molAg,则X的结构简式为_______。
(5)用G代替F制成一次性塑料餐盒的优点是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应NH4Cl+NaNO2![]() NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。下列表示反应中相关微粒的化学用语正确的是
NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。下列表示反应中相关微粒的化学用语正确的是
A. 中子数为18的氯原子:![]()
B. N2的结构式:N=N
C. Na+的结构示意图: 
D. H2O的电子式: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设计如下装置探究HCl溶液中阴、阳离子在电场中的相对迁移速率(已知:Cd的金属活动性大于Cu)。恒温下,在垂直的玻璃细管内,先放CdCl2溶液及显色剂,然后小心放入HCl溶液,在aa’处形成清晰的界面。通电后,可观察到清晰界面缓缓向上移动。下列说法不正确的是
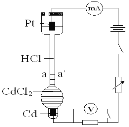
A.通电时,H+、Cd2+向Pt电极迁移,Cl-向Cd电极迁移
B.装置中总反应的化学方程式为:Cd + 2HCl![]() CdCl2 + H2↑
CdCl2 + H2↑
C.一定时间内,如果通过HCl溶液某一界面的总电量为5.0 C,测得H+所迁移的电量为4.1 C,说明该HCl溶液中H+的迁移速率约是Cl-的4.6倍
D.如果电源正负极反接,则下端产生大量Cl2,使界面不再清晰,实验失败
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com