
����Ŀ��POCl3���л��ϳɵĴ������о�С������Cl2��PCl3��H2O��105~109�����Ʊ�POCl3��
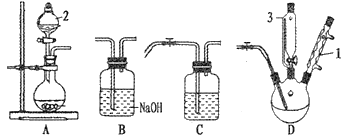
��֪:��PCl3�ױ�������ˮ�⣬�е�Ϊ76�棻��POCl3��ˮ�⣬�е�Ϊ105.8�档
(1)Aװ����ȡ������������2����������______________�����ӷ���ʽΪ________��
(2)PCl3������ʽΪ____________��������I����������____________��
(3)������3��װ���������________�����¶�Ϊ105--109��ʱ����ε��롣�Ʊ�POCl3�Ļ�ѧ��Ӧ����ʽ��________��
(4)�Ʊ�POCl3�Ĺؼ��DZ��豣֤m(Cl2)/m(H2O)��3.94������ֵС��3.94ʱ�ò���POCl3��ԭ����_________________��
(5)װ������˳����A--_____��C��ʢװ��������_______��
���𰸡� ��Һ©�� 2MnO4- + 16Cl- + 8H+ = 2Mn2+ + 5Cl2��+ 8H2O  �ѷ�Ӧ���������������������ת���� ˮ PCl3 + Cl2 + H2O
�ѷ�Ӧ���������������������ת���� ˮ PCl3 + Cl2 + H2O![]() POCl3+2HCl PCl3��POCl3������ˮ�� D-C-B Ũ����
POCl3+2HCl PCl3��POCl3������ˮ�� D-C-B Ũ����
�����������������(1)����Aװ��ͼʾ����������2�������ƣ�Aû�м���װ�ã��������ø��������Ũ���ᷴӦ��ȡ������(2) PCl3����ԭ�Ӿ�����8�����ȶ��ṹ��PCl3�е�Ϊ76�棬������I������ʹPCl3ʹ���������� (3)Cl2��PCl3��H2O��105~109�����Ʊ�POCl3������ԭ���غ㣬��Ӧ����POCl3��HCl������PCl3��POCl3��ˮ�����������3��װ������ʣ� (4) PCl3��POCl3������ˮ�⣬������Ҫ����������(5)װ��A�Ʊ�������װ��Bβ��������װ��C��ֹˮ���뷴Ӧ����װ��D�Ƿ�Ӧ������
������(1) Aװ��������2���������Ƿ�Һ©����Aװ���и��������Ũ���ᷴӦ��ȡ���������ӷ���ʽ��2MnO4- + 16Cl- + 8H+ = 2Mn2+ + 5Cl2��+ 8H2O��(2) PCl3����ԭ�Ӿ�����8�����ȶ��ṹ��PCl3�ĵ���ʽ�� ��PCl3�е�Ϊ76�棬������I������ʹPCl3ʹ�������������PCl3ת���ʣ�(3)Cl2��PCl3��H2O��105~109�����Ʊ�POCl3�� PCl3��POCl3��ˮ�⣬����������3��װ���������ˮ����Ӧ����ʽ��PCl3 + Cl2 + H2O
��PCl3�е�Ϊ76�棬������I������ʹPCl3ʹ�������������PCl3ת���ʣ�(3)Cl2��PCl3��H2O��105~109�����Ʊ�POCl3�� PCl3��POCl3��ˮ�⣬����������3��װ���������ˮ����Ӧ����ʽ��PCl3 + Cl2 + H2O![]() POCl3+2HCl��(4) PCl3��POCl3������ˮ�⣬������Ҫ����������n(Cl2)/n(H2O)��1������m(Cl2)/m(H2O)��3.94��(5)װ��A�Ʊ�������װ��Bβ��������װ��C��ֹˮ�������뷴Ӧ����װ��D�Ƿ�Ӧ��������������˳����A-- D-C-B��C��ʢ��Ũ���ᡣ
POCl3+2HCl��(4) PCl3��POCl3������ˮ�⣬������Ҫ����������n(Cl2)/n(H2O)��1������m(Cl2)/m(H2O)��3.94��(5)װ��A�Ʊ�������װ��Bβ��������װ��C��ֹˮ�������뷴Ӧ����װ��D�Ƿ�Ӧ��������������˳����A-- D-C-B��C��ʢ��Ũ���ᡣ


 �ܿ�����ĩ��̾�ϵ�д�
�ܿ�����ĩ��̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ձ���ѧ�ҷ���һ�ֿɽ���PET���ϵ�ϸ�����������PET���ϴ�������Ⱦ������PET˷���ɼס������ֵ���ϳ�:
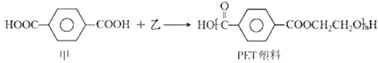
����˵���У���ȷ����
A. ���������Ҵ���Ϊͬϵ��
B. PET�Ļ�ѧʽΪ(C10H9O4)n
C. 1mol����Na2CO3��Ӧ�������CO21mol
D. ���Ϊͬ���칹��ķ����廯����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������顢2�����顢(����)��2,2�������顢2,3�������顣�������л�����й��������У���������������������˵��� (����)
A. ������ B. 2������
C. 3������ D. 2,2��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������廯����A(C9H12O)������ҩ�P���ϵĺϳɣ�A������ת����ϵ:
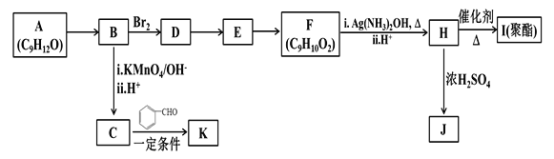
��֪������Ϣ��
��A�Ƿ����廯�����ҷ��Ӳ������д������ֲ�ͬ�����µ���ԭ�ӣ�
��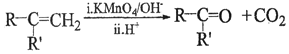
��RCOCH3+RCHO![]() RCOCH=CHR
RCOCH=CHR
�ش���������:
(1)A����B�ķ�Ӧ����Ϊ________����D����E�ķ�Ӧ����Ϊ________��
(2)H �Ĺ���������Ϊ________��
(3)I�Ľṹ��ʽΪ_______��
(4)��E����F�ķ�Ӧ����ʽΪ________ ��
(5)F�ж���ͬ���칹��,д��һ�ַ�������������ͬ���칹��Ľṹ��ʽΪ_______��
���ܷ���ˮ�ⷴӦ��������Ӧ�������ڷ����廯�����ҷ�����ֻ��һ������
�۾���5���˴Ź�������
(6)�����ͪ(![]() )��һ����Ҫ��ҽҩ�м���,��ο������ϳ�·�ߣ����һ�����嶡��[(CH3)3COH]�Ϳ�ȩ(
)��һ����Ҫ��ҽҩ�м���,��ο������ϳ�·�ߣ����һ�����嶡��[(CH3)3COH]�Ϳ�ȩ(![]() )Ϊԭ���Ʊ������ͪ�ĺϳ�·��(���Լ�����,�ýṹ��ʽ��ʾ�л���),�ü�ͷ��ʾת����ϵ����ͷ��ע���Լ��ͷ�Ӧ����)___________��
)Ϊԭ���Ʊ������ͪ�ĺϳ�·��(���Լ�����,�ýṹ��ʽ��ʾ�л���),�ü�ͷ��ʾת����ϵ����ͷ��ע���Լ��ͷ�Ӧ����)___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϳ���������(��Ҫ�ɷ�ΪAl2O3,SiO2��Fe2O3������)Ϊԭ���Ʊ����⻯�ƣ����⻯��(NaAlH4)���л��ϳɵ���Ҫ��ԭ���������������£�
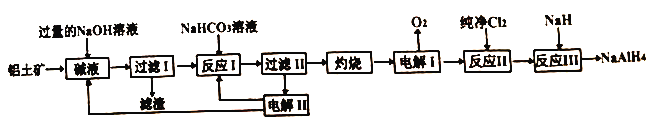 ��֪:SiO2�ڡ���Һ����ת��Ϊ��������Na2Al2SixO8)������
��֪:SiO2�ڡ���Һ����ת��Ϊ��������Na2Al2SixO8)������
(1)����NaOH��Һ�ܽ�������ʱΪ����߽����ʿɲ�ȡ�Ĵ�ʩ��_______��(��дһ��)
(2)���I�Ļ�ѧ����ʽ_______��
(3)�����ա������õ�����Ҫ������_______��_______�����żܡ����������ƾ��ơ�����ǯ��
(4)�����II���ǵ��Na2CO3��Һ��ԭ����ͼ��ʾ��
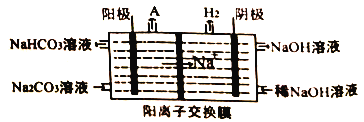
����AΪ_______��(�ѧʽ)
(5)��ӦIII�Ļ�ѧ����ʽΪ_______��ijͬѧ����������Ϊ���������һ�����ۣ����_______ (����������)��Һ������ʵ�ָ������ѭ�����á�
(6)ijͬѧ��Ϊ���Ʊ�����Ҳ���������ܣ��ټ���NaOH��Һ������Һ�������ӳ�����ȫʱ����ʱ��ҺpH��_______��(һ����Ϊ����������Ũ��С��10-5mol/Lʱ������ȫ��Ksp[Fe(OH)3]=1��10-35��Ksp[Al(OH)3]=3��10-34)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������Ǵ�������Ҫ��Ⱦ��ǵ�ǰ������������Ҫ�о�����֮һ��
(1)������ԭ����������
��N2(g)+O2(g)=2NO(g) ��H1 ��4NH3(g)+3O2(g)=2N2(g)+6H2O(l) ��H2
��4NH3(g)+6NO(g)=5N2(g)+6H2O(1) ��H=________��(�ú���H1����H2��ʽ�ӱ�ʾ)
���ݷ�Ӧ�ڣ��ɽ�����ֱ������ȼ�ϵ�أ���KOH��Һ���������Һ��д�������缫��Ӧʽ:____________��
(2)��һ�ܱ�������Ͷ��һ�����İ�����������Ӧ2NH3![]() N2+3H2��H>0����Ӧ������NH3��Ũ����ʱ��仯�������ͼ��ʾ��
N2+3H2��H>0����Ӧ������NH3��Ũ����ʱ��仯�������ͼ��ʾ��
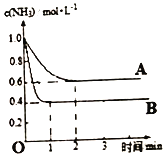
��ش�:
������A�У���Ӧ��ǰ2min��������ƽ����Ӧ����Ϊ________���������µ�ƽ�ⳣ��K=____��
��������������ͬʱ�����ı�ijһ������ʹ�÷�Ӧ������ͼ����B�ķ�Ӧ�����������������Ǹı�_________(�Ũ�ȡ�����ѹǿ�������¶ȡ�������)�������ж�����_________��
(3)һ���¶��£��ں�ѹ�ܱ�������N2O5�ɷ������з�Ӧ:
��2N2O5(g)![]() 4NO2(g)+O2(g) ��2NO2(g)
4NO2(g)+O2(g) ��2NO2(g)![]() 2NO(g)+O2(g)
2NO(g)+O2(g)
����ƽ��ʱ��c(NO2)=0.6mol/L��c(O2)=1.2mol/L����Ӧ����NO2��ת����Ϊ______��N2O5(g)����ʼŨ��Ӧ���ٴ���______mol/L.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�˵����ȷ����
A. һ�������·�ӦN2+3H2![]() 2NH3���ﵽƽ��ʱ��3v��(H2)=2v��(NH3)
2NH3���ﵽƽ��ʱ��3v��(H2)=2v��(NH3)
B. 10mLŨ��Ϊ1mol/L�������������Zn�۷�Ӧ��������������CH3COONa��Һ�����ܽ��ͷ�Ӧ���ʣ��ֲ�Ӱ��H2������
C. ��pH=a+1�İ�ˮϡ��ΪpH=a�Ĺ����У�c(OH��)/c(NH3H2O)��С
D. 25��ʱ��0.1 mol/L��NaHB��Һ�����ԣ�˵��H2BΪǿ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com