
(Т»)ЈЁ1Ј©јЧНйТІКЗТ»ЦЦЗеҪаИјБПЈ¬ө«І»НкИ«ИјЙХКұИИР§ВКҪөөНІў»бІъЙъУР¶ҫЖшМеФміЙОЫИҫЎЈ
ТСЦӘЈә CH4(g) + 2O2(g) ЈҪ CO2(g) + 2H2O(l) ҰӨH1ЈҪЁD890.3 kJ/mol
2CO (g) + O2(g) ЈҪ 2CO2(g) ҰӨH2ЈҪЁD566.0 kJ/mol
ФтјЧНйІ»НкИ«ИјЙХЙъіЙТ»Сх»ҜМјәНТәМ¬Л®КұөДИИР§ВКЦ»КЗНкИ«ИјЙХКұөД________ұ¶ЈЁјЖЛгҪб№ыұЈБф1О»РЎКэЈ©ЎЈ
ЈЁ2Ј©јЧНйИјБПөзіШҝЙТФМбЙэДЬБҝАыУГВКЎЈПВНјКЗАыУГјЧНйИјБПөзіШөзҪв50 mL 2 mol/LөДВИ»ҜНӯИЬТәөДЧ°ЦГКҫТвНјЈә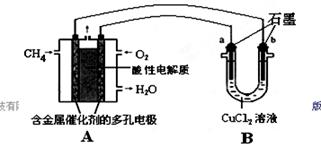
Зл»ШҙрЈә
ўЩјЧНйИјБПөзіШөДёәј«·ҙУҰКҪКЗ________ЎЈ
ўЪөұПЯВ·ЦРУР0.1 molөзЧУНЁ№эКұЈ¬________ЈЁМоЎ°aЎұ»тЎ°bЎұЈ©ј«ФцЦШ________gЎЈ
ЈЁ¶юЈ©ПВұнКЗјёЦЦИхөзҪвЦКөДөзАлЖҪәвіЈКэЎўДСИЬөзҪвЦКөД
ИЬ¶И»эKsp (25Ўж)ЎЈ
| өзҪвЦК | ЖҪәв·ҪіМКҪ | ЖҪәвіЈКэK | Ksp |
| CH3COOH | CH3COOH CH3COO-Ј«H+ CH3COO-Ј«H+ | 1.76ЎБ10-5 | |
| H2CO3 | H2CO3 H+Ј«HCO3- H+Ј«HCO3-HCO3-  H+Ј«CO32- H+Ј«CO32- | K1ЈҪ4.31ЎБ10-7 K2ЈҪ5.61ЎБ10-11 | |
| C6H5OH | C6H5OH  C6H5O-Ј«H+ C6H5O-Ј«H+ | 1.1ЎБ10-10 | |
| H3PO4 | H3PO4 H+Ј«H2PO4- H+Ј«H2PO4-H2PO4-  H+Ј«HPO32- H+Ј«HPO32-HPO42-  H+Ј«PO43- H+Ј«PO43- | K1ЈҪ7.52ЎБ10-3 K2ЈҪ6.23ЎБ10-8 K3ЈҪ2.20ЎБ10-13 | |
| NH3ЎӨH2O | NH3ЎӨH2O NH4+Ј«OH- NH4+Ј«OH- | 1.76ЎБ10-5 | |
| BaSO4 | BaSO4 Ba2+Ј«SO42- Ba2+Ј«SO42- | | 1.07ЎБ10-10 |
| BaCO3 | BaCO3 Ba2+Ј«CO32- Ba2+Ј«CO32- | | 2.58ЎБ10-9 |
ўе ЈЁ1Ј©0.7 ЈЁ2·ЦЈ© ЈЁ2Ј©ўЩCH4-8e-+2H2O=CO2+8H+ ўЪ b 3.2 ЈЁёч2·ЦЈ©
ўжЈЁ1Ј©ўЩўЬўЫўЪ ЈЁ2·ЦЈ© ЈЁ2Ј© = ЈЁ1·ЦЈ© ЈЁ3Ј© D ЈЁ2·ЦЈ© ЈЁ4Ј© D ЈЁ2·ЦЈ©
ҪвОцКФМв·ЦОцЈәўеЈЁ1Ј©јЧНйІ»НкИ«ИјЙХөДИИ»ҜС§·ҪіМКҪОӘ: CH4(g) + O2(g) ЈҪ CO(g) + 2H2O(l) ҰӨHЈҪЁD607.3 kJ/mol,ФтјЧНйІ»НкИ«ИјЙХЙъіЙТ»Сх»ҜМјәНТәМ¬Л®КұөДИИР§ВКЦ»КЗНкИ«ИјЙХКұөД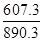 =0.7ұ¶ ЈЁ2Ј©ўЩөзҪвЦКОӘЛбРФ№Кёәј«·ҙУҰКҪОӘЈәCH4-8e-+2H2O=CO2+8H+ ўЪCu2+ФЪТхј«·Еөзјҙbј«Ј¬ГҝНЁ№э0.1molөзЧУЈ¬УР0.5molCu2+·ЕөзЈ¬јҙ3.2g ўжЈЁ1Ј© KЦөФҪҙуЛбРФФҪЗҝ ЈЁ2Ј©25ЎжКұҙЧЛбәН°ұЛ®өДөзАліМ¶ИПаН¬Ј¬№КҪ«өИМе»эөИЕЁ¶ИөДҙЧЛбәН°ұЛ®»мәПәуИЬТәіКЦРРФЈ¬№К»мәПТәЦРc(CH3COO-)=c(NH4+)Ј»ЈЁ3Ј©ТтОӘNH3ЎӨH2OөДөзАліМ¶ИФ¶ҙуУЪC6H5OHЈ¬№КПт10ml 0.01mol/LұҪ·УИЬТәЦРөОјУVml 0.01mol/L°ұЛ®Ј¬°ұЛ®өДМе»эІ»РиТӘөҪ10mLИЬТәөДpH>7,A ҙнЈ»BІ»ЧсСӯөзәЙКШәгЈ¬ҙнЈ»V=10КұЈ¬»мәПТәОӘұҪ·Уп§ИЬТәЈ¬ұҪ·Уп§Л®ҪвҙЩҪшЛ®өДөзАлЈ¬№К»мәПТәЦРЛ®өДөзАліМ¶ИҙуУЪ10ml 0.01mol/LұҪ·УИЬТәЦРЛ®өДөзАліМ¶ИЈ¬CҙнЈЁ4Ј©ЙэёЯОВ¶ИЈ¬BaSO4өДөзАлЖҪәвПтУТТЖ¶ҜЈ¬cЈЁSO42-Ј©әНc(Ba2+)¶јФцҙуЈ¬DҙнЎЈ
=0.7ұ¶ ЈЁ2Ј©ўЩөзҪвЦКОӘЛбРФ№Кёәј«·ҙУҰКҪОӘЈәCH4-8e-+2H2O=CO2+8H+ ўЪCu2+ФЪТхј«·Еөзјҙbј«Ј¬ГҝНЁ№э0.1molөзЧУЈ¬УР0.5molCu2+·ЕөзЈ¬јҙ3.2g ўжЈЁ1Ј© KЦөФҪҙуЛбРФФҪЗҝ ЈЁ2Ј©25ЎжКұҙЧЛбәН°ұЛ®өДөзАліМ¶ИПаН¬Ј¬№КҪ«өИМе»эөИЕЁ¶ИөДҙЧЛбәН°ұЛ®»мәПәуИЬТәіКЦРРФЈ¬№К»мәПТәЦРc(CH3COO-)=c(NH4+)Ј»ЈЁ3Ј©ТтОӘNH3ЎӨH2OөДөзАліМ¶ИФ¶ҙуУЪC6H5OHЈ¬№КПт10ml 0.01mol/LұҪ·УИЬТәЦРөОјУVml 0.01mol/L°ұЛ®Ј¬°ұЛ®өДМе»эІ»РиТӘөҪ10mLИЬТәөДpH>7,A ҙнЈ»BІ»ЧсСӯөзәЙКШәгЈ¬ҙнЈ»V=10КұЈ¬»мәПТәОӘұҪ·Уп§ИЬТәЈ¬ұҪ·Уп§Л®ҪвҙЩҪшЛ®өДөзАлЈ¬№К»мәПТәЦРЛ®өДөзАліМ¶ИҙуУЪ10ml 0.01mol/LұҪ·УИЬТәЦРЛ®өДөзАліМ¶ИЈ¬CҙнЈЁ4Ј©ЙэёЯОВ¶ИЈ¬BaSO4өДөзАлЖҪәвПтУТТЖ¶ҜЈ¬cЈЁSO42-Ј©әНc(Ba2+)¶јФцҙуЈ¬DҙнЎЈ
ҝјөгЈә»ҜС§·ҙУҰУлДЬБҝұд»ҜУлЛөИЬТәөДЧЫәПҝјІй



| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈәМоҝХМв
ПВұнКЗјёЦЦИхөзҪвЦКөДөзАлЖҪәвіЈКэЎўДСИЬөзҪвЦКөДИЬ¶И»эKspЈЁ25ЎжЈ©ЎЈ
| өзҪвЦК | өзАл·ҪіМКҪ | өзАліЈКэK | Ksp |
| H2CO3 | H2CO3 HCO3ЈӯЈ«HЈ« HCO3ЈӯЈ«HЈ«HCO3Јӯ  CO32ЈӯЈ«HЈ« CO32ЈӯЈ«HЈ« | K1ЈҪ4.31ЎБ10Јӯ7 K2ЈҪ5.61ЎБ10Јӯ11 | Јӯ |
| C6H5OH | C6H5OH C6H5OЈӯЈ«HЈ« C6H5OЈӯЈ«HЈ« | 1.1ЎБ10Јӯ10 | Јӯ |
| H3PO4 | H3PO4 H2PO4ЈӯЈ«HЈ« H2PO4ЈӯЈ«HЈ«H2PO4Јӯ  HPO42ЈӯЈ«HЈ« HPO42ЈӯЈ«HЈ«HPO42Јӯ  PO43ЈӯЈ«HЈ« PO43ЈӯЈ«HЈ« | K1ЈҪ7.52ЎБ10Јӯ3 K2ЈҪ6.23ЎБ10Јӯ6 K1ЈҪ2.20ЎБ10Јӯ13 | Јӯ |
| NH3ЎӨH2O | NH3ЎӨH2O OHЈӯЈ«NH4Ј« OHЈӯЈ«NH4Ј« | 1.76ЎБ10Јӯ5 | Јӯ |
| BaSO4 | BaSO4ЈЁsЈ© Ba2Ј«Ј«SO42Јӯ Ba2Ј«Ј«SO42Јӯ | Јӯ | 1.07ЎБ10Јӯ10 |
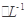 C6H5OHИЬТәЦРЛ®өДөзАліМ¶И
C6H5OHИЬТәЦРЛ®өДөзАліМ¶И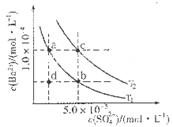
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈәМоҝХМв
°ҙТӘЗуНкіЙПВБР»ҜС§·ҙУҰКҪ
ЈЁ1Ј©БтЛбЗвДЖФЪЛ®ИЬТәЦРөДөзАл·ҪіМКҪЎЎЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈ»
ЈЁ2Ј©Na2CO3ИЬТәЛ®ҪвөДАлЧУ·ҪіМКҪЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЈ»
ЈЁ3Ј©Al2(SO4)3ИЬТәУлNaHCO3ИЬТә»мәП·ҙУҰөДАлЧУ·ҪіМКҪЎЎЎЎЎЎ ЎЎЎЎЎЎЈ»
ЈЁ4Ј©Mg3N2УлЛ®·ҙУҰөД»ҜС§·ҪіМКҪЎЎЎЎЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈ»
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈәМоҝХМв
өзАл¶ИұнКҫөзҪвЦКөДПа¶ФЗҝИхЈ¬өзАл¶ИөД¶ЁТеЈә
ҰБЈҪЈЁТСөзАлөДөзҪвЦК·ЦЧУКэЈҜИЬТәЦРФӯУРөзҪвЦКөДЧЬ·ЦЧУКэЈ©ЎБ100%ЎЈ
ТСЦӘ25ЎжКұјёЦЦОпЦК(ОўБЈ)өДөзАл¶И(ИЬТәЕЁ¶ИҫщОӘ0.1 molЎӨLЈӯ1)ИзПВұнЈә
| ұаәЕ | ОпЦК(ОўБЈ) | өзАл¶ИҰБ |
| A | БтЛбИЬТә(өЪТ»ІҪНкИ«өзАл)Јә өЪ¶юІҪ HSO4- HЈ«Ј«SO42- HЈ«Ј«SO42- | 10% |
| B | БтЛбЗвДЖИЬТәЈә HSO4- HЈ«Ј«SO42 HЈ«Ј«SO42 | 29% |
| C | ҙЧЛбЈә CH3COOH CH3COOЈӯЈ«HЈ« CH3COOЈӯЈ«HЈ« | 1.33% |
| D | СОЛбЈә HClЈҪHЈ«Ј«ClЈӯ | 100% |
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈәМоҝХМв
ДСИЬРФФУВұКҜ(K2SO4ЎӨMgSO4ЎӨ2CaSO4ЎӨ2H2O)КфУЪЎ°ҙфҝуЎұЈ¬ФЪЛ®ЦРҙжФЪИзПВИЬҪвЖҪәвЈә
K2SO4ЎӨMgSO4ЎӨ2CaSO4ЎӨ2H2O(s) 2Ca2Ј«Ј«2KЈ«Ј«Mg2Ј«Ј«4SO42-Ј«2H2OЎЈОӘДЬід·ЦАыУГјШЧКФҙЈ¬УГұҘәНCa(OH)2ИЬТәИЬҪюФУВұКҜЦЖұёБтЛбјШЈ¬№ӨТХБчіМИзПВЈә
2Ca2Ј«Ј«2KЈ«Ј«Mg2Ј«Ј«4SO42-Ј«2H2OЎЈОӘДЬід·ЦАыУГјШЧКФҙЈ¬УГұҘәНCa(OH)2ИЬТәИЬҪюФУВұКҜЦЖұёБтЛбјШЈ¬№ӨТХБчіМИзПВЈә
ЈЁ1Ј©ВЛФьЦчТӘіЙ·ЦУР________әНCaSO4ТФј°ОҙИЬФУВұКҜЎЈ
ЈЁ2Ј©УГ»ҜС§ЖҪәвТЖ¶ҜФӯАнҪвКНCa(OH)2ИЬТәДЬИЬҪвФУВұКҜҪюіцKЈ«өДФӯТтЈә
ЎЈ
ЈЁ3Ј©Ў°іэФУЎұ»·ҪЪЦРЈ¬ПИјУИл ИЬТәЈ¬ҫӯҪБ°иөИІЩЧчә󣬹эВЛЈ¬ФЩјУИл ИЬТәөчВЛТәpHЦБЦРРФЎЈ
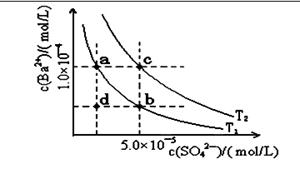
ЈЁ4Ј©І»Н¬ОВ¶ИПВЈ¬KЈ«өДҪюіцЕЁ¶ИУлИЬҪюКұјдөД№ШПөјыУТНјЎЈУЙНјҝЙөГЈ¬ЛжЧЕОВ¶ИЙэёЯЈ¬
ўЩ Ј¬
ўЪ Ј¬
ўЫИЬҪюіцөДKЈ«өДЖҪәвЕЁ¶ИФцҙуЎЈ
ЈЁ5Ј©УРИЛТФҝЙИЬРФМјЛбСООӘИЬҪюјБЈ¬ФтИЬҪю№эіМЦР»б·ўЙъЈәCaSO4(s)Ј«CO32- CaCO3(s)Ј«SO42-ЎЈТСЦӘ298 KКұЈ¬Ksp(CaCO3)ЈҪ2.80ЎБ10Јӯ9Ј¬Ksp(CaSO4)ЈҪ4.90ЎБ10Јӯ5Ј¬јЖЛгҙЛОВ¶ИПВёГ·ҙУҰөДЖҪәвіЈКэЈ¬KЈҪ ЎЈ
CaCO3(s)Ј«SO42-ЎЈТСЦӘ298 KКұЈ¬Ksp(CaCO3)ЈҪ2.80ЎБ10Јӯ9Ј¬Ksp(CaSO4)ЈҪ4.90ЎБ10Јӯ5Ј¬јЖЛгҙЛОВ¶ИПВёГ·ҙУҰөДЖҪәвіЈКэЈ¬KЈҪ ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈәМоҝХМв
Бтј°Жд»ҜәПОпУР№г·әөДУҰУГЈ¬¶ФSO2РФЦКөДСРҫҝКЗёЯЦР»ҜС§ҪМС§өДТ»ПоЦШТӘДЪИЭЎЈ
IЈ®¶ФұИСРҫҝКЗТ»ЦЦЦШТӘөДСРҫҝ·Ҫ·ЁЎЈИфҪ«БтөДөҘЦКј°Іҝ·Ц»ҜәПОп°ҙИзПВұнЛщКҫ·ЦіЙ3 ЧйЈ¬ФтөЪ2ЧйЦРОпЦКMөД»ҜС§КҪКЗ ЎЈ
| өЪ1Чй | өЪ2Чй | өЪ3Чй |
| S (өҘЦК) | SO2ЎўH2SO3ЎўMЎўNaHSO3 | SO3ЎўH2SO4ЎўNa2SO4ЎўNaHSO4 |

| n(SO32ЎӘ)Јәn(HSO3ЎӘ) | 91Јә9 | 1Јә1 | 9Јә91 |
| pH | 8.2 | 7.2 | 6.2 |
| РтәЕ | КөСй·Ҫ°ё | КөСйПЦПу | ҪбВЫ |
| ·Ҫ°ёўЩ | НщөЪТ»·ЭКФТәЦРјУИлKMnO4ИЬТәИЬТә | ЧПәмЙ«НКИҘ | SO2УлFe3+·ҙУҰЙъіЙБЛFe2+ |
| ·Ҫ°ёўЪ | НщөЪ¶ю·ЭКФТәЦРјУИл | | SO2УлFe3+·ҙУҰЙъіЙБЛFe2+ |
| ·Ҫ°ёўЫ | НщөЪ¶ю·ЭКФТәЦРјУИл | | SO2УлFe3+·ҙУҰЙъіЙБЛSO42ЎӘ |
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈәМоҝХМв
ОТ№ъДіҙуРНөзҪвНӯЙъІъЖуТөЈ¬ЖдТұБ¶№ӨТХЦРНӯЎўБт»ШКХВКҙпөҪ97ЈҘЎў87ЈҘЎЈПВНјұнКҫЖдТұБ¶јУ№ӨөДБчіМЈә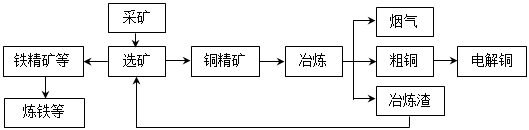
ТұБ¶ЦРөДЦчТӘ·ҙУҰЈәCu2S + O2 =" 2Cu" + SO2
ЈЁ1Ј©СМЖшЦРөДЦчТӘ·ПЖшКЗ________________Ј¬ҙУМбёЯЧКФҙАыУГВКәНјхЕЕҝјВЗЈ¬ЖдЧЫәПАыУГ·ҪКҪКЗЦЖ___________ЎЈ
ЈЁ2Ј©өзҪв·ЁБ¶НӯКұЈ¬Сфј«КЗ____________ЈЁМоЎ°ҙҝНӯ°еЎұ»тЎ°ҙЦНӯ°еЎұЈ©Ј»ҙЦНӯЦРә¬УРөДҪрЎўТшТФөҘЦКөДРОКҪФЪөзҪвІЫ_______________ЈЁМоЎ°Сфј«Ўұ»тЎ°Тхј«ЎұөДІЫөЧЈ¬Тхј«өДөзј«·ҙУҰКҪКЗ_________________________________________ЎЈ
ЈЁ3Ј©ФЪҫ«Б¶НӯөД№эіМЦРЈ¬өзҪвЦКИЬТәЦРc(Fe2+)Ўўc(Zn2+)»бЦрҪҘФцҙу¶шУ°ПмҪшТ»ІҪөзҪвЎЈ
јёЦЦОпЦКөДИЬ¶И»эіЈКэЈЁKSPЈ©Јә
| ОпЦК | Fe(OH)2 | Fe(OH)3 | Zn(OH)2 | Cu(OH)2 |
| KSP | 8.0ЎБ10Јӯ16 | 4.0ЎБ10Јӯ38 | 3.0ЎБ10Јӯ17 | 2.2ЎБ10Јӯ20 |
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈәМоҝХМв
СЗБЧЛбЈЁH3PO3Ј©КЗ¶юФӘЛбЈ¬H3PO3ИЬТәҙжФЪөзАлЖҪәвЈәH3PO3 H+ + H2PO3ЈӯЎЈСЗБЧЛбУлЧгБҝNaOHИЬТә·ҙУҰЈ¬ЙъәНNa2HPO3ЎЈ
H+ + H2PO3ЈӯЎЈСЗБЧЛбУлЧгБҝNaOHИЬТә·ҙУҰЈ¬ЙъәНNa2HPO3ЎЈ
ЈЁ1Ј©ўЩРҙіцСЗБЧЛбУлЙЩБҝNaOHИЬТә·ҙУҰөДАлЧУ·ҪіМКҪ_____________________________________ЎЈ
ўЪДіОВ¶ИПВЈ¬0.1000 molЎӨLЈӯ1өДH3PO3ИЬТәpHөД¶БКэОӘ1.6Ј¬јҙҙЛКұИЬТәЦРc (H+) = 2.5ЎБ10Јӯ2 molЎӨLЈӯ1Ј¬іэOHЎӘЦ®НвЖдЛыАлЧУөДЕЁ¶ИУЙРЎөҪҙуөДЛіРтКЗ Ј¬ёГОВ¶ИПВH3PO3өзАлЖҪәвөДЖҪәвіЈКэK= ЎЈЈЁH3PO3өЪ¶юІҪөзАләцВФІ»јЖЈ¬Ҫб№ыұЈБфБҪО»УРР§КэЧЦЈ©
ўЫПтH3PO3ИЬТәЦРөОјУNaOHИЬТәЦБЦРРФЈ¬ЛщөГИЬТәЦРcЈЁNa+Ј©_______ cЈЁH2PO3-Ј©+ 2cЈЁHPO32-Ј©ЈЁМоЎ°>ЎұЎў Ў°<Ўұ »тЎ°=ЎұЈ©ЎЈ
ЈЁ2Ј©СЗБЧЛбҫЯУРЗҝ»№ФӯРФЈ¬ҝЙК№өвЛ®НКЙ«Ј¬ёГ·ҙУҰөД»ҜС§·ҪіМКҪ_______________________ЎЈ
ЈЁ3Ј©өзҪвNa2HPO3ИЬТәТІҝЙөГөҪСЗБЧЛбЈ¬Ч°ЦГКҫТвНјИзПВЈә
ЛөГчЈәСфДӨЦ»ФКРнСфАлЧУНЁ№эЈ¬ТхДӨЦ»ФКРнТхАлЧУНЁ№эЎЈ
ўЩТхј«өДөзј«·ҙУҰКҪОӘ_____________________________ЎЈ
ўЪІъЖ·КТЦР·ҙУҰөДАлЧУ·ҪіМКҪОӘ_____________________ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈәјЖЛгМв
CuSO4ИЬТәУлK2C2O4ИЬТә·ҙУҰЈ¬өГөҪТ»ЦЦА¶Й«Ҫбҫ§Л®әПОпҫ§МеЎЈНЁ№эПВКцКөСйИ·¶ЁёГҫ§МеөДЧйіЙЈә
ўЩіЖИЎ0.1680gҫ§МеЈ¬јУИл№эБҝөДH2SO4ИЬТәЈ¬К№СщЖ·ИЬҪвәујУИлККБҝЛ®Ј¬јУИИҪь·РЈ¬УГ0.02000molЎӨL-1KMnO4ИЬТәөО¶ЁЦБЦХөгЈЁИЬТәұдОӘЗіЧПәмЙ«Ј©Ј¬ПыәД20.00mLЎЈ
ўЪҪУЧЕҪ«ИЬТәід·ЦјУИИЈ¬К№ЗіЧПәмЙ«ұдОӘА¶Й«Ј¬ҙЛКұMnOЎӘ4ЧӘ»ҜОӘMn2+ІўКН·ЕіцO2ЎЈ
ўЫАдИҙәујУИл2g KI№ММеЈЁ№эБҝЈ©әНККБҝNa2CO3Ј¬ИЬТәұдОӘЧШЙ«ІўЙъіЙіБөнЎЈ
ўЬУГ0.05000molЎӨL-1Na2S2O3ИЬТәөО¶ЁЈ¬ҪьЦХөгјУЦёКҫјБЈ¬өО¶ЁЦБЦХөгЈ¬ПыәД10.00mLЎЈ
ТСЦӘЈә2MnOЎӘ4+5H2C2O4+6H+==2Mn2++10CO2Ўь+8H2O
2Cu2++4IЎӘ=2CuIЎэ+I2
2Na2S2O3+I2=2NaI+Na2S4O6
ЈЁ1Ј©ІҪЦиўЪЦР·ўЙъ·ҙУҰөДАлЧУ·ҪіМКҪОӘ ЎЈ
ЈЁ2Ј©ІҪЦиўЬЦРјУИлөДЦёКҫјБОӘ ЎЈ
ЈЁ3Ј©НЁ№эјЖЛгРҙіцА¶Й«ҫ§МеөД»ҜС§КҪЈЁРҙіцјЖЛг№эіМЈ©ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com