
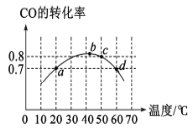
【题目】在2L恒容密闭容器分别投入2molCO和1molO2。进行反应:2CO(g)+O2(g)![]() 2CO2(g)。在相同的时间段(5min)下,测得CO的转化率与温度的关系如图所示。下列说法正确的是
2CO2(g)。在相同的时间段(5min)下,测得CO的转化率与温度的关系如图所示。下列说法正确的是
A.化学平衡常数:K(b)<K(c)<K(d)
B.a点,vO2(正)=0.14mo1·L-1·min-1
C.d点vCO(正)等于a点vCO(正)
D.50℃时,该反应的化学平衡常数K=160L·mol-1
【答案】D
【解析】
根据图示,b点时CO的转化率最大,则b点时反应达到平衡状态,随温度升高,CO的转化率降低,说明反应逆向进行,则正反应为放热反应,据此分析解答。
A.根据分析,2CO(g)+O2(g)![]() 2CO2(g)为放热反应,b、c、d点温度依次升高,温度升高,反应逆向进行,平衡常数减小,则化学平衡常数:K(b)>K(c)>K(d),故A错误;
2CO2(g)为放热反应,b、c、d点温度依次升高,温度升高,反应逆向进行,平衡常数减小,则化学平衡常数:K(b)>K(c)>K(d),故A错误;
B.a点时,CO的转化率为0.7,则CO物质的量的变化量为2mol×0.7=1.4mol,则CO的平均反应速率=![]() =0.14 mo1·L-1·min-1,根据反应速率之比等于化学反应计量系数值比,vO2(正)=
=0.14 mo1·L-1·min-1,根据反应速率之比等于化学反应计量系数值比,vO2(正)=![]() vCO (正)=0.14mo1·L-1·min-1×
vCO (正)=0.14mo1·L-1·min-1×![]() =0.07 mo1·L-1·min-1,即5min内,O2的平均反应速率为0.07 mo1·L-1·min-1,故B错误;
=0.07 mo1·L-1·min-1,即5min内,O2的平均反应速率为0.07 mo1·L-1·min-1,故B错误;
C.a、b两点的温度不同,a点的温度低,b点的温度高,温度越高反应速率越快,则两点vCO(正)不相等,b点vCO(正)大于a点vCO(正),故C错误;
D.50℃时,CO的转化率为0.8,列三段式:

该反应的化学平衡常数K=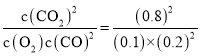 =160L·mol-1,故D正确;
=160L·mol-1,故D正确;
答案选D。


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
【题目】常温下,在27.5 g水中溶解12.5 g CuSO45H2O,恰好达到饱和,该溶液密度为1.18 g·cm-3,求:
(1)该溶液中阴阳离子的总物质的量._________________
(2)该溶液中CuSO4的物质的量浓度(保留二位小数)。________________
(3)取出20.0 mL该溶液,加入足量Ba(OH)2溶液,反应后可得到沉淀质量多少克?(保留一位小数)____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过硝酸钠(NaNO4)能与水发生反应∶NaNO4+H2O= NaNO3+H2O2,下列说法不正确的是( )
A.过硝酸钠可用于杀菌消毒
B.过硝酸钠中含有-O-O-结构
C.过硝酸钠具有强氧化性,没有还原性
D.将过硝酸钠加入酸性FeSO4溶液中发生的离子方程式∶![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】应用下列实验装置或方案能达到实验目的的是
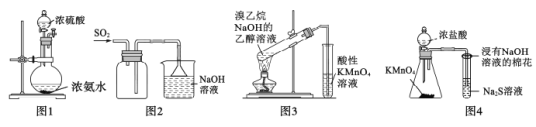
A.用图1装置制备少量氨气
B.用图2所示装置收集SO2
C.用图3所示装置检验是否有乙烯产生
D.用图4装置比较KMnO4、C12、S的氧化性强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用高分子吸附树脂提取卤水中的碘(主要以I-形式存在)的工艺流程如下
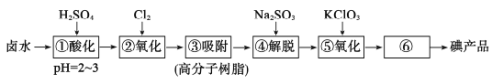
下列说法正确的是
A.流程中①和④所得溶液中,I-离子的浓度相等
B.流程中⑥的分离碘产品的操作方法是萃取
C.流程中④发生离子反应:2I2+SO![]() +H2O=4I-+SO
+H2O=4I-+SO![]() +2H+
+2H+
D.制备10mol I2,理论上需KC1O3的质量约为408g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸碱中和滴定是中学化学常见实验。
Ⅰ.下图表示50mL酸式滴定管中液面的位置,如果液面处的读数是a,则滴定管中剩余液体的体积是______mL。
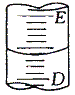
A、a B、大于a C、小于(50-a) D、大于(50-a)
Ⅱ.某同学欲测定某浓硫酸样品的物质的量浓度,进行了以下实验操作:
A 冷却至室温后,在100mL容量瓶中定容配成100mL稀硫酸。
B 量取20.00mL稀硫酸于锥形瓶中并滴入几滴指示剂。
C 将酸式滴定管和碱式滴定管用蒸馏水洗涤干净,并用各待盛溶液润洗。
D 将物质的量浓度为1.50 mol·L-1的标准NaOH溶液装入碱式滴定管,调节液面记下读数V1。
E 继续滴定至终点,记下读数为V2。
F 在锥形瓶下垫一张白纸,把锥形瓶移到碱式滴定管下小心滴入NaOH标准溶液,边滴边摇动锥形瓶。
G 量取浓硫酸样品5 mL,在烧杯中用蒸馏水溶解。
H 重复以上实验。
请回答下列问题:
(1)该实验正确操作步骤的顺序为____→ A →_____→_____→D→_____→_____→ H(用编号字母填写)。
(2)量取5mL浓硫酸的仪器是________________________;量取20.00mL稀硫酸的仪器是_________。
(3)选用的指示剂是_____________。滴定过程中,视线应注视____________________;判断到达滴定终点的现象是________________;读数时,视线应____________(填“高于”、“低于”或“相平于”)溶液凹液面的最低处。
(4)下表是实验测得的有关数据:
滴定序号 | 待测稀硫酸的体积(mL) | 所消耗NaOH标准溶液液的体积(mL) | |
V1 | V2 | ||
① | 20.00 | 0.50 | 22.60 |
② | 20.00 | 6.00 | 27.90 |
请计算出该浓硫酸样品的浓度为____________mol·L-1 (不必写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为了探究原电池产生电流的过程,设计了如图实验。
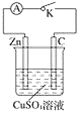
(1)打开K,观察到的现象为________________。
(2)关闭K,观察到的现象是_________。此电池的负极的电极反应式为_____。
(3)关闭K,溶液中阳离子向_______(填“Zn”或“C”)极移动,外电路中,电子流动方向是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①H2(g)+![]() O2(g)=H2O(g) ΔH1=akJ·mol1
O2(g)=H2O(g) ΔH1=akJ·mol1
②2H2(g)+O2(g)=2H2O(g) ΔH2=bkJ·mol1
③H2(g)+![]() O2(g)=H2O(l) ΔH3=ckJ·mol1
O2(g)=H2O(l) ΔH3=ckJ·mol1
④2H2(g)+O2(g)=2H2O(l) ΔH4=d kJ·mol1
下列关系式中正确的是
A.a<c<0B.b>d>0C.2a=b<0D.2c=d>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在开展研究性学习活动中,某研究小组的同学设计了如下3套实验装置,用来收集和验证铁在高温下与水蒸气反应的气体产物。

(1)请指出能正确得出实验结论的装置(填"A"、"B"或"C")_____。
(2)写出铁在高温下与水蒸气反应的化学方程式_______。
(3)怎样用简单方法检验收集到的气体,简述检验操作的方法和现象________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com