
| A. | H2 | B. | CO | C. | CH3OH | D. | C2H5OH |
分析 物质足量的O2中充分燃烧后生成CO2、H2O,通过过量的Na2O2,发生反应2CO2+2Na2O2=2Na2CO3+O2,2H2O+2Na2O2=4NaOH+O2,由方程式可知,过氧化钠增重=与CO2同物质的量的CO质量+与H2O同物质的量的H2质量,组成增重质量的组成可以表示为nCO•mH2,即化学式可以改写成nCO•mH2,完全燃烧后过氧化钠增重等于该物质的质量,据此结合选项解答.
解答 解:物质足量的O2中充分燃烧后生成CO2、H2O,通过过量的Na2O2,发生反应2CO2+2Na2O2=2Na2CO3+O2,2H2O+2Na2O2=4NaOH+O2,由方程式可知,过氧化钠增重=与CO2同物质的量的CO质量+与H2O同物质的量的H2质量,组成增重质量的组成可以表示为nCO•mH2,即化学式可以改写成nCO•mH2,完全燃烧后过氧化钠增重等于该物质的质量,
A.根据反应2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O、2H2O+2Na2O2=4NaOH+O2↑可知:H2+Na2O2=2NaOH,可知agH2反应后固体的质量恰好也增加了a g,故A不选;
B.根据C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2、CO2+2Na2O2=2Na2CO3+O2可知CO+Na2O2=Na2CO3,所以agCO反应后固体的质量恰好也增加了a g,故B不选;
C.CH3OH可以改写成CO•2H2,故agCH2O完全燃烧,反应后固体的质量恰好也增加了a g,故C不选;
D.C2H5OH 可以改写成C•CO•2H2,agC2H5OH燃烧,反应后固体的质量不是a g,故D选;
故选D.
点评 本题考查化学方程式的计算,题目难度中等,注意把握过氧化钠与二氧化碳和水反应的质量增加的质量关系,根据关系式得出固体增加的质量相当于CO和H2的质量.


科目:高中化学 来源: 题型:选择题
| A. | 该化合物仅含碳、氢两种元素 | B. | 该化合物中碳、氢原子个数比为1:4 | ||
| C. | 无法确定该化合物是否含有氧元素 | D. | 该化合物中一定不含有氧元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
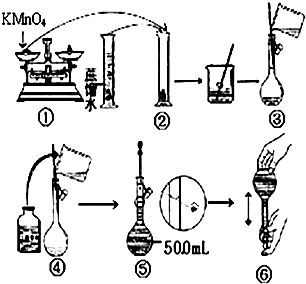 人体血液里Ca2+离子的浓度一般采用g/cm3来表示.抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度.某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度:
人体血液里Ca2+离子的浓度一般采用g/cm3来表示.抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度.某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
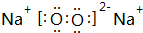 (用电子式表示)
(用电子式表示)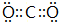 (用电子式表示)
(用电子式表示)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
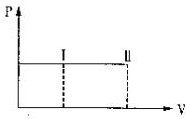 一带有活塞的密封容器中盛有A、B组成的混合气体,在通常条件下,从状态I反应到状态II时,气体体积(V)与气体压强(P)的变化曲线如图所示.
一带有活塞的密封容器中盛有A、B组成的混合气体,在通常条件下,从状态I反应到状态II时,气体体积(V)与气体压强(P)的变化曲线如图所示.| A. | 是放热反应 | |
| B. | 反应后气体总分子数增多 | |
| C. | 是吸热反应 | |
| D. | 反应物具有的总能量等于生成物具有的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂分子中都含有碳碳双键 | B. | 葡萄糖分子中含有羟基和醛基 | ||
| C. | 水分子中含有羟基 | D. | 乙酸乙酯分子中含有羧基 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入NaOH,溶液pH升高,c(SO32-)增大 | B. | 氯化钡有两性 | ||
| C. | 两支试管中的白色沉淀都是BaSO4 | D. | SO2具有两性且水溶液有酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
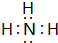 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com