
【题目】下列反应中属于氧化还原反应,但水既不作氧化剂又不作还原剂的是( )
A.H2O+Na2O=2NaOHB.2H2O+2F2=4HF+O2
C.2H2O![]() O2↑+2H2↑D.3NO2+H2O=2HNO3+NO
O2↑+2H2↑D.3NO2+H2O=2HNO3+NO
【答案】D
【解析】
属于氧化还原反应,说明反应中有元素化合价的变化,水既不作氧化剂,又不作还原剂,说明水中的氢、氧元素化合价在反应中无变化。
A.H2O+Na2O=2NaOH中,元素化合价没有变化,不属于氧化还原反应,A不符合题意;
B.2H2O+2F2=4HF+O2中,水中O元素的化合价升高,水为还原剂,B不符合题意;
C.2H2O![]() O2↑+2H2↑中,H元素的化合价降低,O元素的化合价升高,则水既作氧化剂又作还原剂,C不符合题意;
O2↑+2H2↑中,H元素的化合价降低,O元素的化合价升高,则水既作氧化剂又作还原剂,C不符合题意;
D.3NO2+H2O=2HNO3+NO中,N元素的化合价既升高又降低,则属于氧化还原反应,NO2既作氧化剂又作还原剂,水中H、O元素的化合价都没有变化时,水既不作氧化剂又不作还原剂,D符合题意;故答案为:D。


科目:高中化学 来源: 题型:
【题目】金属铬和氢气在工业上都有重要的用途。已知:铬能与稀硫酸反应,生成氢气和硫酸亚铬(CrSO4)。铜铬构成原电池如图所示,盐桥中装的是饱和KCl琼脂溶液,下列关于此电池的说法正确的是

A.盐桥的作用是使整个装置构成通路、保持溶液呈电中性,凡是有盐桥的原电池,盐桥中均可以用饱和KCl琼脂溶液
B.理论上1molCr溶解,盐桥中将有2molCl-进入左池,2molK+进入右池
C.此过程中H+得电子,发生氧化反应
D.电子从铬极通过导线到铜极,又通过盐桥到转移到左烧杯中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图甲中①②③④表示不同化学元素所组成的化合物,图乙表示由四个单体构成的化合物。以下说法不正确的是( )

A. 若图甲中的②大量存在于皮下和内脏器官周围等部位,则②是脂肪
B. 若图甲中④能吸收、传递和转换光能,则④可用无水乙醇提取
C. 图乙中若单体是氨基酸,则该化合物彻底水解后的产物中氧原子数增加3个
D. 图乙中若单体是四种脱氧核苷酸,则该化合物彻底水解后的产物有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“异丙苯氧化法”生产丙酮和苯酚的合成路线如下,各反应的原子利用率均为100%。下列说法正确的是
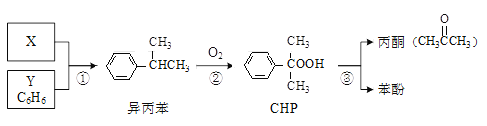
A. X的分子式为C3H8B. Y与异丙苯可用酸性KMnO4溶液鉴别
C. CHP与CH3COOH含有相同的官能团D. 可以用分液的方法分离苯酚和丙酮
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲用98%的浓硫酸(密度为1.84g·cm-3)配制成浓度为0.5mol·L-1的稀硫酸500毫升.
(1)选用的主要仪器除了烧杯、玻璃棒、胶头滴管外还有:_______________(写两个)
(2)请将下列各操作,按正确的序号填在横线上。
A.用量筒量取浓H2SO4
B.反复颠倒摇匀
C.用胶头滴管加蒸馏水至刻度线
D.稀释浓H2SO4
E.将溶液转入容量瓶
其操作正确的顺序依次为____________________________。
(3)简要回答下列问题:
①98%的浓硫酸的物质的量浓度为_____________mol·L-1
②配制成浓度为0.5mol·L-1的稀硫酸500毫升.所需98%的浓硫酸的体积为____________mL;(保留小数点后一位)
③将浓硫酸沿烧杯内壁慢慢注入盛水的烧杯中,并用玻璃棒不断搅拌的目的是_____;
④定容时必须使溶液凹液面与刻度线相切,若仰视刻度则使浓度___________。(“偏高”、“偏低”、“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。

(1)装置B中盛放饱和NaCl溶液,该装置的主要作用是_________;F中的试剂是__________。
(2)实验步骤:如图连接装置后,先___________(填实验操作),再装药品,然后点燃________(填“ A” 或“C” )处酒精灯,当_________(填实验现象)时,再点燃另一处酒精灯。
(3)写出装置G 中发生反应的离子方程式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在室温下进行下图所示实验。(已知:H2C2O4为二元弱酸)
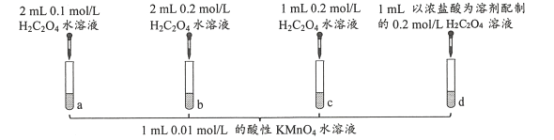
试管a、b、c中溶液褪色分别耗时690s、677s、600s。下列说法正确的是
A.反应的离子方程式为2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O
B.试管c反应至300 s时,溶液中剩余的c(KMnO4)=0.0025 mol/L
C.对比试管a、b,得到的结论是H2C2O4水溶液浓度增大,反应速率加快
D.对比试管c、d,可验证H+浓度对反应速率的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用H2还原WO3制备金属W的装置如图所示(Zn粒中往往含有硫等杂质,焦性没食子酸溶液用于吸收少量氧气),下列说法正确的是
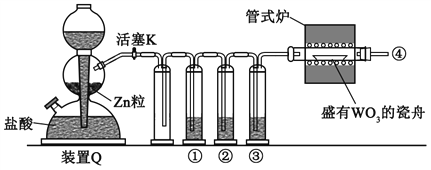
A. ①、②、③中依次盛装KMnO4溶液、浓H2SO4、焦性没食子酸溶液
B. 管式炉加热前,用试管在④处收集气体并点燃,通过声音判断气体纯度
C. 结束反应时,先关闭活塞K,再停止加热
D. 装置Q(启普发生器)也可用于二氧化锰与浓盐酸反应制备氯气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com