
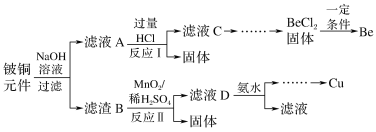
����Ŀ����ͭ�ǹ㷺Ӧ�������������Ԫ�������úϽ�ij����С���ij����ͭԪ��(��25%BeO��71%CuS������FeS��SiO2)�л������ͭ���ֽ����Ĺ���������ͼ��
��֪����.�롢��Ԫ�صĻ�ѧ�������ƣ�������������������Һ��Ӧ���ɿ�����ˮ��Na2BeO2
��.�����²�����������ܶȻ��������±���
������ | Cu(OH)2 | Fe(OH)3 | Mn(OH)2 |
�ܶȻ�����(Ksp) | 2.2��10-20 | 4.0��10-38 | 2.1��10-13 |
��1����ҺA����Ҫ�ɷֳ�NaOH�⣬����__(�ѧʽ)��д����ӦI�к��뻯������������ᷴӦ�����ӷ���ʽ��__��
(2)����ҺC�к�NaCl��BeCl2������HCl��Ϊ�ᴿBeCl2���������ʵ�鲽��˳��Ϊ__(����ĸ)��
a.��������İ�ˮ b.ͨ�������CO2 c.���������NaOH d.����������HCl e.ϴ�� f.����
�ڴ�BeCl2��Һ�еõ�BeCl2����IJ�����__��
��3����MnO2�ܽ����������е���Ԫ������Ϊ���ʡ�д����Ӧ����CuS������Ӧ�Ļ�ѧ����ʽ��__��
������ŨHNO3�ܽ�������ȱ����__(��дһ��)��
��4����ҺD��c(Cu2+)=2.2mol��L-1��c(Fe3+)=0.008mol��L-1��c(Mn2+)=0.01mol��L-1����μ���ϡ��ˮ����pH�ɽ������η��룬���ȳ�������__(�����ӷ���)��Ϊʹͭ���ӿ�ʼ������������Ӧ������Һ��pH����__��
��5�����NaCl��BeCl2������ο��Ʊ������룬��ͼ�ǵ��װ��ͼ��
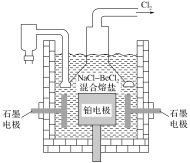
��ʯī�缫�ϵĵ缫��ӦʽΪ__��
�ڵ��õ���Be������Լ��1%��Na������ȥBe������Na�ķ���Ϊ__��
��֪�������ʵ��ۡ��е����±���
���� | �۵�(K) | �е�(K) |
Be | 1551 | 3243 |
Na | 370 | 1156 |
���𰸡�Na2BeO2��Na2SiO3 BeO22-+4H+=Be2++2H2O afed Ҫ��HCl�����������ᾧ MnO2+CuS+2H2SO4=MnSO4+S+CuSO4+2H2O �������Ⱦ���������� Fe3+ 4 Be2++2e-=Be ���Կ����¶�1156��3243K֮����ȴ
��������
Be��AlԪ�ػ�ѧ�������ƣ��Ͼ���ͭԪ���м���NaOH��Һ��BeO��SiO2��Ӧת����Na2BeO2��Na2SiO3������ҺA�У�����B�к�CuS��FeS����ҺA�м������HCl��Na2SiO3��Ӧ����H2SiO3������NaCl��Na2BeO2�����HCl��Ӧ����NaCl��BeCl2��H2O����ҺC�к�HCl��NaCl��BeCl2��MnO2���������ԣ�����B�м���MnO2��H2SO4��CuS��FeS��Ӧ����CuSO4��Fe2��SO4��3��S��MnO2����ԭΪMnSO4����ҺD����Ҫ��CuSO4��Fe2��SO4��3��MnSO4���������Cu��OH��2��Fe��OH��3��Mn��OH��2���ܶȻ�����ҺD�м��백ˮ�õ��ij���FΪFe��OH��3����ҺE�м��백ˮ����pHʹCu2+��Mn2+���롣
��1���Ͼ���ͭԪ���ijɷ�BeO��CuS��FeS��SiO2��������Ϣi��BeO�������������SiO2���������������������������Һ��Ӧ����Ӧ����ʽΪBeO+2NaOH=Na2BeO2+H2O��SiO2+2NaOH=Na2SiO3+H2O��CuS��FeS�����������Ʒ�Ӧ�������ҺA����Ҫ�ɷ���NaOH��Na2SiO3��Na2BeO2��������Ϣi����ӦI��ΪNa2BeO2��������ᷴӦ����Ӧ�����ӷ���ʽΪBeO22��+4H��=Be2��+2H2O���ʴ�Ϊ��Na2BeO2��Na2SiO3��BeO22-+4H+=Be2++2H2O��
��2����Be����Ԫ�ػ�ѧ�������ƣ�������ҺC���ȼ�������İ�ˮ������Be��OH��2������Ȼ����ˡ�ϴ�ӣ��ټ���������HCl������BeCl2������������afed���ʴ�Ϊ��afed��
��BeCl2��ǿ�������Σ�BeCl2����Һ�лᷢ��ˮ�⣬ʹ��Һ�����ԣ�Ϊ��ֹBeCl2ˮ�⣬���BeCl2��Һ�еõ�BeCl2����Ӧ��HCl�����������ᾧ������BeCl2ˮ�⣬�ʴ�Ϊ��Ҫ��HCl�����������ᾧ��
��3������ӦII��CuS��Sת��ΪS���ʣ�MnO2��Mn����ԭΪMn2�������ݻ��ϼ�������������ƽ�ɵ÷�Ӧ�Ļ�ѧ��Ӧ����ʽΪMnO2+CuS+2H2SO4=S+MnSO4+CuSO4+2H2O���ʴ�Ϊ��MnO2+CuS+2H2SO4=MnSO4+S+CuSO4+2H2O��
������ŨHNO3�ܽ�����������ᱻ��ԭ���ɵ����������Ⱦ�������ʴ�Ϊ���������Ⱦ���������壻
��4��������ܶȻ���֪��Cu2����ʼ����ʱc��OH����=1��10-10mol/L����ҺpHΪ4��Fe3����ʼ����ʱ��c��OH����=1��10-12mol/L��Mn2����ʼ����ʱc��OH����=1��10-6mol/L��������ȳ�������Fe3���������ɵij���FΪFe��OH��3���ʴ�Ϊ��Fe3+��4��
��5������ͼ��֪�����缫�Ϸ���������Ӧ����������Ϊ���ص���������ʯī�缫Ϊ�������������������õ��ӷ�����ԭ��Ӧ�����룬�缫��ӦʽΪBe2++2e-=Be���ʴ�Ϊ��Be2++2e-=Be��
���ɱ������ݿ�֪������۷е�����ƣ�����Կ����¶�11563243K֮����ȴ��ȥBe����������Na���ʴ�Ϊ�����Կ����¶�1156��3243K֮����ȴ��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���� NA ��ʾ�����ӵ�������ֵ,����˵����ȷ���ǣ���
A.��⾫��ͭ,�����·ͨ�� NA ������ʱ,����������С 32 g
B.��Ӧ 3H2��g��+N2��g��![]() 2NH3��g����H=-92 kJ��mol-1,���ų� 9.2 kJ ����ʱ,��Ӧ�� N2 Ϊ2.24L
2NH3��g����H=-92 kJ��mol-1,���ų� 9.2 kJ ����ʱ,��Ӧ�� N2 Ϊ2.24L
C.���³�ѹ�� 27 �� Al �� 33.6L ������ȫ��Ӧ������ת����С�� 3NA
D.1 mol��L-1 �Ȼ�ͭ��Һ��,�� Cl-����ĿΪ 2NA,�� Cu2+����Ŀ��С�� NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ������ɫ�Ľ����������ڽ����ӹ�����Ƶȡ���ҵ�Ը�����[��Ҫ�ɷ���Fe(CrO2)2]Ϊԭ��ұ���������ǿ������Na2Cr2O7���乤��������ͼ��ʾ��

��֪����������ʱ������ӦFe(CrO2)2��Na2CO3��O2��Na2CrO4��Fe2O3��CO2(δ��ƽ)
�ش��������⣺
��1�������������Ҫ�ɷ�Fe(CrO2)2д�����������ʽ��__����������ʱ������߷�Ӧ���ʵķ���Ϊ___(д��һ������)��
��2��Na2CrO4���������ữ�����ӷ���ʽΪ__����ʵ�����У�����a���õ��IJ���������__��
��3��Na2CrO4�и�Ԫ�ػ��ϼ�Ϊ__������1molNa2CrO4ʱ��ת�Ƶ��ӵ����ʵ���Ϊ__mol��
��4�������йع��ұ�����CrO42-�ķ�ˮҪ����ѧ������ʹ��Ũ�Ƚ���5.0��10-7mol��L-1���²����ŷţ��ɲ��ü�������Ա�������BaCrO4����[Ksp(BaCrO4)=1.2��10-10]���ټ������ᴦ�������Ba2+�ķ���������ˮ����������Ա��κ�ˮ��Ba2+��Ũ��Ӧ����__mol��L-1����ˮ������ﵽ���ұ������ŷš�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�ܽ��Ҳ�������ʵ���Ũ�ȱ�ʾ��25��ʱ��Ag2CrO4�ڲ�ͬŨ��CrO42-��Һ�е��ܽ����ͼ��ʾ,����˵����ȷ����

A.ͼ��a��b����c(Ag+)��ͬ
B.ͼ��a����b��Ag2CrO4�ܶȻ����
C.��a������Һ�м�������AgNO3���ܽ�ȿɱ�Ϊc��
D.���¶��£�Ag2CrO4�ܶȻ���������Ϊ10-12
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() ��
��![]() �������������ܱ������У���һ�������·������з�Ӧ��
�������������ܱ������У���һ�������·������з�Ӧ��![]() ������ƽ��ʱ��
������ƽ��ʱ��![]() Ϊ
Ϊ![]() �������ʱ����
�������ʱ����![]()
![]() ��
��![]() ������ͬ�¶����ٴ�ƽ��ʱ
������ͬ�¶����ٴ�ƽ��ʱ![]() �����ʵ����ǣ� ��
�����ʵ����ǣ� ��
A.![]() B.
B.![]() C.����
C.����![]() ����
����![]() D.��
D.��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��a��b��c��d��ԭ������������������AΪdԪ����ɵķǽ������ʣ��ס��ҡ�����������Ϊ��������Ԫ����ɵĶ�Ԫ����Ԫ�������������ΪҺ�塣����˵����ȷ���ǣ� ��

A.�����Ӱ뾶��c>b
B.��Ӧ��Ϊ���ȷ�Ӧ
C.�ڷ�Ӧ���������뻹ԭ�����ʵ���֮��Ϊ1��1
D.b��d�ֱ���a�γɵĻ������У���ѧ������һ����ȫ��ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л����˵����ȷ���ǣ� ��
A.�Ҵ��ͱ�������Ϊͬϵ��
B.����ϩ(![]() )�����е�����̼ԭ�ӹ���
)�����е�����̼ԭ�ӹ���
C.����ʽΪC5H10O2������������ͬ���칹�干��9��(�����������칹)
D.��������( ![]() )�Ķ��ȴ�����6�ֽṹ(�����������칹)
)�Ķ��ȴ�����6�ֽṹ(�����������칹)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2����1��3�������ɼ䱽�����Ȼǻ�������������ȥ��������ɡ�ԭ�����£�

�������ʵ�����������£�
���� | ��Է������� | ��״ | �۵�/�� | ˮ����(����) |
�䱽���� | 110 | ��ɫ��״���� | 110.7 | ���� |
2����1��3������ | 155 | �ۺ�ɫ��״���� | 87.8 | ���� |
�Ʊ��������£�
��һ�����ǻ�����ȡ71.5g�䱽���ӣ���ɷ�ĩ������ƿ�У�������������Ũ���Ტ���Ͻ��裬�����¶���һ����Χ��15min(��ͼ1)��
�ڶ��������������ǻ���Ӧ��������ƿ������ˮ�У������ȴ��������������������¶ȼ�������15min��
������������������Ӧ������ϡ��Һת�Ƶ�Բ����ƿB�У�Ȼ����ͼ2��ʾװ�ý���ˮ��������(ˮ���������ʹ���ᴿ���л����ڵ���100����������ˮ����һ������������Ӷ��ﵽ�����ᴿ��Ŀ��)��

��ش��������⣺
��1���ǻ������п����¶�����ʵķ�ΧΪ(����ĸ)__��
a.30�桫60�� b.60�桫65�� c.65�桫70�� d.70�桫100��
��2��ͼ2�е��������Ƿ���Ի�Ϊͼ1����������___����������������������
��3��������������ȡ���������ľ��������__��
��4��ͼ2�У���ƿA�г�����������ѹ���ã����ܷ�ֹװ����ѹǿ���������¹ʣ����ܷ�ֹ__��������C�п��ܿ�����������__����Ӧһ��ʱ���ֹͣ����ʱ�IJ�����__(���й������;ƾ��ƵIJ���)��
��5��ˮ���������Ƿ�����ᴿ�л���ķ���֮һ�����ᴿ���ʱ���߱���������ȷ����__��
a.���ܻ�������ˮ������������
b.�ڷ�������ˮ��������ѧ��Ӧ
c.�ѻӷ���
d.������ˮ
��6����ʵ�����ջ��12.0g�ۺ�ɫ���壬��2����1��3�����ӵIJ���ԼΪ__��������3λ��Ч���֣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ���ܿ�ʯ(��Ҫ�ɷ�Ϊ Co2O3�������� SiO2�����������̡�þ���ƵȽ���Ԫ�ص�������)��ȡCoC2O42H2O ����Ĺ����������£�
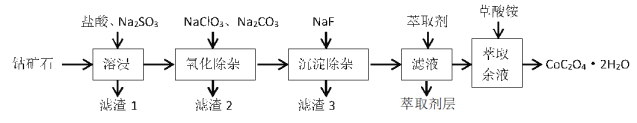
��֪����������������������ʽ����ʱ��Һ pH ���
������ | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
��ȫ������ pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)�ܽ������� Co2O3 ������Ӧ�����ӷ���ʽΪ_____��
(2)�������ӹ����м��� Na2CO3 ����ҪĿ����__________���������� NaClO3��������_____��
(3)���� 3 �ijɷ���____________����Һ�м�����ȡ����Ŀ���dz�ȥ_________Ԫ��(��Ԫ�ط���)��
(4)��ȡ��Һ�м������狀�ȡ CoC2O4��2H2O ����IJ�����___________��
(5)���ܻ����� LiCoO2�ǷϾ�﮵�ص��������ϣ�����˫��ˮ��ϡ H2SO4 ��ϼ��ȵõ� CoSO4�������ã��ù��̷�����Ӧ�Ļ�ѧ����ʽ��____________��
(6)��֪ij�¶��� Ksp(MgF2)=7.35��10-11��Ksp(CaF2)=1.05��10-10�����������NaF��Һ��������Һ��c(Ca2+)/c(Mg2+) =___________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com