
【题目】重水(D2O)的离子积为1.6×10-15,可以用pH一样的定义来规定pD= -lg[D+],以下关于pD的叙述不正确的是( )
A.中性溶液的pD〉7.0
B.含0.01mol NaOD的D2O溶液1L,其pD=12.0
C.溶解0.01molDCl的D2O溶液1L,其pD=2.0
D.在100mL0.25mol/L的DCl重水溶液中,加入50mL0.2mol/LNaOD的重水溶液,其pD=1.0
【答案】B
【解析】
重水D2O中c(D+)=c(OD-),D2O的离子积![]() ,结合pD=-lgc(D+)计算判断;
,结合pD=-lgc(D+)计算判断;
A. 重水D2O中c(D+)=c(OD),呈中性,D2O的离子积![]() ,则c(D+)=4×108mol/L,pD=lgc(D+)═lg4×108=7.4,所以中性溶液的pD =7.4>7.0,A正确;
,则c(D+)=4×108mol/L,pD=lgc(D+)═lg4×108=7.4,所以中性溶液的pD =7.4>7.0,A正确;
B. 0.01mol/L的NaOD的D2O溶液中,c(OD)=0.01mol/L,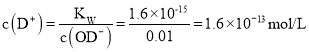 ,pD=lg1.6×1013=12.8, B错误;
,pD=lg1.6×1013=12.8, B错误;
C. 0.01mol/L的DCl的D2O溶液中c(D+)=0.01mol/L,pD=lg0.01=2.0,C正确;
D. 100mL0.25 molL1的DCl重水溶液和50mL0.2 molL1的NaOD的重水溶液混合时,DCl过量,所以 ,pD=1.0,D正确;
,pD=1.0,D正确;
答案选B。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】水溶液中的离子反应在许多领域都有广泛的应用,请回答下列问题。
(1)在配制氯化铁溶液时,常常会出现浑浊,可以加入少量的__________防止上述问题。
(2)明矾具有净水的作用,原因是:___________________________(用离子方程式表示)。
(3)将25 ℃时pH=12的NaOH溶液a L与pH=1的HCl溶液b L混合。若所得混合液为中性,则a∶b=______________。
(4)加热蒸干AlCl3溶液并灼烧所得固体,最终得到的产物是______________
(5)常温下,已知Ksp[M(OH)3] =1.0×1038,要使溶液中的M3+降至105mol/L,则应调节溶液pH=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用 0.10 mol·L-1NaOH溶液分别滴定20.00 mL 0.10 mol·L-1HCl溶液和20.00 mL 0.10 mol·L-1CH3COOH溶液,得到2条滴定曲线,如下图所示,则下列说法正确的是
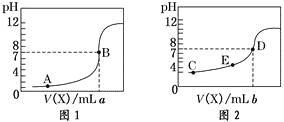
A.图2是滴定盐酸的曲线
B.a与b的关系是:a<b
C.E点对应离子浓度由大到小的顺序为: c(CH3COO-) >c(Na+) >c(H+) >c(OH-)
D.这两次滴定都可以用甲基橙作为指示剂且颜色变化为红变橙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于体积相同的①(NH4) 2SO4、②NH4HSO4、③H2SO4溶液,下列说法正确的是( )
A.溶液的pH相同时,3种溶液物质的量浓度大小顺序是③>②>①
B.溶液的pH相同时,将3种溶液稀释相同倍数,pH变化最大的是①
C.溶液的pH相同时,由水电离出的![]() 大小顺序是③>②>①
大小顺序是③>②>①
D.若3种溶液的物质的量浓度都相同,则溶液的pH大小顺序是①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子一定能在指定溶液中大量共存的是
A.c水(H+)=1×10-12 mol·L -1的溶液:Al3+、Fe3+、Cl-、SO42-
B.![]() =1×10-13mol·L -1的溶液:NH4+、Ca2+、Cl-、NO3-
=1×10-13mol·L -1的溶液:NH4+、Ca2+、Cl-、NO3-
C.澄清透明的无色溶液:K+、NH4+、MnO4-、HCO3-
D.和Al反应放出H2的溶液:Mg2+、Cu2+、NO3-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据图海水综合利用的工业流程图判断,下列说法正确的是
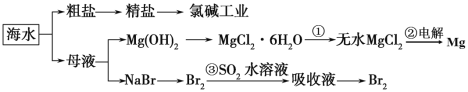
A.过程①中将MgCl2·6H2O灼烧即可制得无水MgCl2
B.在工业上可用电解MgCl2溶液的方法生产金属镁
C.过程③反应后溶液呈强酸性,故生产中需解决其对金属设备的腐蚀问题
D.氯碱工业生产中适当增加电流强度可增大电解反应的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】留兰香(薄荷中的一种)可用来治疗感冒咳嗽、胃痛腹胀、神经性头痛等,其有效成分为葛缕酮(结构简式如图)。下列有关葛缕酮的说法正确的是
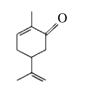
A.葛缕酮的分子式为C10H16O
B.葛缕酮使溴水和酸性KMnO4溶液褪色的原理相同
C.葛缕酮中所有碳原子可能处于同一个平面
D.羟基直接连苯环且苯环上有2个取代基的葛缕酮的同分异构体有12种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在下列给定条件的溶液中,一定能大量共存的离子组是( )
A.滴加甲基橙试剂显红色的溶液中:Na+、Fe2+、Cl-、NO3-
B.含有大量Al3+的水溶液中:Na+、NH4+、HCO3-、Br-
C.![]() =0.1mol·L-1的溶液:Na+、K+、SO32-、NO3-
=0.1mol·L-1的溶液:Na+、K+、SO32-、NO3-
D.水电离产生的c(H+)为1×10-l2mol·L-1的溶液:AlO2-、Na+、Cl-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2008年10月8日,瑞典皇家科学院宣布将诺贝尔化学奖授予日本科学家下村修、美国科学家马丁沙尔菲与美籍华裔科学家钱永健,以表彰三人因在发现和研究绿色荧光蛋白方面做出的贡献。蛋白质是一类复杂的含氮化合物,每种蛋白质都有其恒定的含氮量[约在14%~18%(本题涉及的含量均为质量分数)],故食品中蛋白质的含量测定常用凯氏定氮法,其测定原理是:
Ⅰ.蛋白质中的氮(用氨基表示)在强热和CuSO4、浓H2SO4作用下,生成一种无机含氮化合物,反应式为:2(-NH2)+H2SO4+2H+![]() ;
;
Ⅱ.该无机化合物在凯氏定氮器中与碱作用,通过蒸馏释放出NH3,收集于H3BO3溶液中,生成(NH4)2B4O7;
Ⅲ.用已知浓度的HCl标准溶液滴定,根据HCl消耗的量计算出氮的含量,然后乘以相应的换算系数,即得蛋白质的含量。
(1)上述原理第Ⅰ步生成的无机含氮化合物化学式为_________;
(2)乳制品的换算系数为6.38,即若检测出氮的含量为1%,蛋白质的含量则为6.38%.不法分子通过在低蛋白含量的奶粉中加入三聚氰胺(Melamine)来“提高”奶粉中的蛋白质含量,导致许多婴幼儿肾结石。
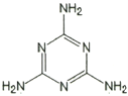
①三聚氰胺的结构如图所示,其化学式为_________,含氮量(氮元素的质量分数)为_________;
②下列关于三聚氰胺的说法中,正确的有_________;
A.三聚氰胺是一种白色结晶粉末,无色无味,所以掺入奶粉后不易被发现
B.三聚氰胺分子中所有原子可能在同一个平面上
C.三聚氰胺呈弱碱性,可以和酸反应生成相应的盐
③假定奶粉中蛋白质含量为16%即为合格,不法分子在一罐总质量为500g、蛋白质含量为0的假奶粉中掺入_________g的三聚氰胺就可使奶粉“达标”。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com