
【题目】用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
A.32 g S8(分子结构:![]() )中的共价键数目为NA
)中的共价键数目为NA
B.1L、0.1mol/L的Na2CO3溶液中含阴离子总数为0.1NA个
C.标准状况下,22.4LHF含NA个分子
D.标准状况下,11.2 L Cl2溶于水,溶液中Cl-、ClO-和HClO的微粒数之和为NA
科目:高中化学 来源: 题型:
【题目】下列关于电解质溶液的说法正确的是
A.某温度下 c(H+)=![]() 的溶液一定是中性溶液
的溶液一定是中性溶液
B.室温下,向 0.1 mol·L-1 的 CH COOH 溶液中加入少量显碱性的 CH COONa,CH COOH 的电离程度一定增大
C.浓度均为 0.1 mol·L-1 的①(NH4 ) 2CO3 、②NH4HSO4 、③(NH4)2Fe(SO4)2、④NH4 Cl 溶液中,c(NH4+)的大小顺序为①>③>②>④
D.强酸强碱盐的水溶液一定呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi)、镆(Mc)为元素周期表中原子序数依次增大的同族元素。回答下列问题:
(1)砷在周期表中的位置_____,![]() Mc 的中子数为_____。已知存在P(S,红磷)、P(S,黑磷) 、P(S,白磷),它们互称为_____。
Mc 的中子数为_____。已知存在P(S,红磷)、P(S,黑磷) 、P(S,白磷),它们互称为_____。
(2)热稳定性:NH3_____PH3(填“>”或“<”),砷的最高价氧化物对应水化物的化学式为_____是一种_____酸(填“强”或“弱”) 。
(3)PH3 和卤化氢反应与 NH3 相似,产物的结构和性质也相似。写出 PH3 和 HI 反应的化学方程式_____。
(4)SbCl3 能发生较强烈的水解,生成难溶的 SbOCl,写出该反应的化学方程式_____,因此,配制 SbCl3溶液时应注意_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学学习小组设计以下实验方案,测定某含有NaCl的小苏打样品中![]() 的质量分数。
的质量分数。
(方案一)查资料:NaCl加热至![]() 时熔化而不分解,
时熔化而不分解,![]() 受热分解,
受热分解,![]() 。由此设计实验:用电子天平称取
。由此设计实验:用电子天平称取![]() 样品,置于坩埚中用酒精灯加热(如图,灼烧温度高于
样品,置于坩埚中用酒精灯加热(如图,灼烧温度高于![]() ,不超过
,不超过![]() ),至恒重后,冷却,称量剩余固体质量为
),至恒重后,冷却,称量剩余固体质量为![]() 。
。
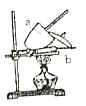
(1)实验中至少称量____次。
(2)实验中,达到恒重操作的标准是__________。
(方案二)根据“![]() 溶液呈碱性,
溶液呈碱性,![]() ”的性质设计实验:准确称取1.000 g样品,用容量瓶配成100 mL溶液,用滴定管量取20.00 mL于锥形瓶中,加入2滴甲基橙为指示剂,用0.1000mol/L盐酸标准溶液滴定。平行两份,两次实验的数据如下:
”的性质设计实验:准确称取1.000 g样品,用容量瓶配成100 mL溶液,用滴定管量取20.00 mL于锥形瓶中,加入2滴甲基橙为指示剂,用0.1000mol/L盐酸标准溶液滴定。平行两份,两次实验的数据如下:
1 | 2 | |
| 20.00 | 20.00 |
| 0.00 | 0.20 |
| 19.98 | 20.22 |
(3)实验中,当其它操作均正确时,下列操作不会引起实验误差的是(______)。
A.容量瓶用蒸馏水洗净后,瓶内有水残留,直接配制溶液
B.滴定管内壁有水珠就装入标准液
C.锥形瓶内壁有水珠,用待测液润洗后再使用
D.锥形瓶用蒸馏水洗净后,直接放入待测液进行测定
span>(4)滴定终点的判断:__________。
(5)两次实验消耗盐酸体积的平均值为__________mL。
(6)样品中![]() 的质量分数__________。
的质量分数__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出以乙炔为原料制备![]() (聚氯乙烯)的过程中所发生的反应类型:____________、_____________。
(聚氯乙烯)的过程中所发生的反应类型:____________、_____________。![]() (聚乙烯)材料目前被公认为安全材料,也可用于制作保鲜膜和一次性餐盒。辨别
(聚乙烯)材料目前被公认为安全材料,也可用于制作保鲜膜和一次性餐盒。辨别![]() 和
和![]() 有三种方法,一是闻气味法:具有刺激性气味的是___________________;二是测密度法:密度大的应是___________________;三是燃烧法:
有三种方法,一是闻气味法:具有刺激性气味的是___________________;二是测密度法:密度大的应是___________________;三是燃烧法:![]() 的单体和
的单体和![]() 的单体在足量空气中燃烧的实验现象的明显区别是__________。
的单体在足量空气中燃烧的实验现象的明显区别是__________。
(2)![]() (
(![]() )是一种阻隔性高、韧性强、化学稳定性好的理想包装材料,广泛用于肉制品、豆制品等的包装。写出合成
)是一种阻隔性高、韧性强、化学稳定性好的理想包装材料,广泛用于肉制品、豆制品等的包装。写出合成![]() 的单体的同分异构体的结构简式_________。
的单体的同分异构体的结构简式_________。
(3) “白色污染”是指各种塑料制品对环境的污染。焚烧塑料会生成有毒物质二噁英,二噁英是含有如图所示母体的系列化合物,下列关于如图所示物质的说法不正确的是___________________(填序号)。

a.该物质在氧气中完全燃烧的产物是![]() 和
和![]()
b.该物质属于烃
c.该物质的一卤代物只有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 分解速率受多种因素影响。实验测得
分解速率受多种因素影响。实验测得![]() 时不同条件下
时不同条件下![]() 浓度随时间的变化如图所示
浓度随时间的变化如图所示![]() 起始浓度均为
起始浓度均为![]() 。下列说法正确的是
。下列说法正确的是![]()
![]()
实验条件 |
|
|
|
① | 0 | 0 | |
② |
| 0 | |
③ |
| 3 | |
④ |
| 3 |
A.![]() 内,④条件下
内,④条件下![]() 的平均反应速率为
的平均反应速率为![]()
B.分析②③条件可知,![]() 浓度越大,
浓度越大,![]() 分解速率越慢
分解速率越慢
C.少量![]() 存在时,溶液碱性越强,
存在时,溶液碱性越强,![]() 分解速率越快
分解速率越快
D.分析①②条件可知,无![]() 时,碱性条件有利于双氧水的分解
时,碱性条件有利于双氧水的分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO和苯都是重要的化工原料,如图是某有机物D的合成过程。已知化合物C可与水混溶。

请回答:
(1)反应①的反应类型是__。
(2)若反应③中原子利用率达100%,则反应③还应加的试剂是__(填化学式)。
(3)下列说法正确的是__(填序号)。
A.一定条件下,化合物C可与水反应生成
B.化合物A和C均为不饱和烃,均能使溴水褪色
C.水或碳酸钠溶液均能鉴别苯和化合物C,但不能用酸性KMnO4溶液鉴别
D.完全燃烧,等质量的A与苯耗氧量相等,等物质的量的A与B耗氧量也相等
(4)④的反应机理与制取乙酸乙酯相似,写出其化学方程式:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某恒容密闭容器中,按物质的量之比为 1:1 投入 A 和 B,发生以下反应:A(g)+ B(?)![]() aD(g)(a 为正整数)。达平衡后,如果升高温度时,D 的质量分数增加;减小压强,D 的质量分数减小。在一定温度和一定压强下达平衡时,D 的物质的量分数为 50%,则下列说法正确的是
aD(g)(a 为正整数)。达平衡后,如果升高温度时,D 的质量分数增加;减小压强,D 的质量分数减小。在一定温度和一定压强下达平衡时,D 的物质的量分数为 50%,则下列说法正确的是
A.B 可能是固体也可能是液体
B.该反应的△H<0
C.在一定温度和一定压强下达平衡时,A 的转化率为 67%
D.当混合气体密度不变时,该反应达平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
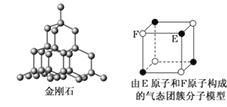
【题目】有关晶体的结构如下图所示,下列说法中不正确的是
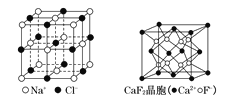
A.在NaCl晶体中,距Na+最近的Cl-形成正八面体
B.在CaF2晶体中,每个晶胞平均占有4个Ca2+
C.在金刚石晶体中,6个碳原子形成一个环且不在同一平面上
D.该气态团簇分子的分子式为EF或FE
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com