
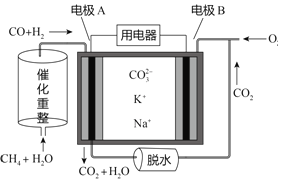
【题目】一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是
A. 反应CH4+H2O![]() 3H2+CO,每消耗1molCH4转移8mol电子
3H2+CO,每消耗1molCH4转移8mol电子
B. 电池工作时,CO32-向电极A移动
C. 电极A上只有H2参与电极反应,反应式为H2+2OH--2e-=2H2O
D. 电极B上发生的电极反应为O2+4e-=2O2-
【答案】B
【解析】A.根据C元素的化合价变化结合电子守恒来分析;
B.原电池中阴离子向负极移动;
C.原电池工作时,CO和H2失电子在负极反应,则A为负极,CO和H2被氧化生成二氧化碳和水;
D.在原电池的正极上是氧气得电子发生还原反应。
A.CH4→CO,化合价由-4价→+2价,上升6价,则1molCH4参加反应共转移6mol电子,A错误;
B.通氧气的一极为正极,则B为正极,A为负极,原电池中阴离子向负极移动,A为负极,所以CO32-向电极A移动,B正确;
C.通氧气的一极为正极,则B为正极,A为负极,负极上CO和H2被氧化生成二氧化碳和水,电极A反应为:H2+CO+2CO32--4e-=H2O+3CO2,C错误;
D.B电极上氧气得电子发生还原反应O2+2CO2+4e-=2CO32-,D错误。
答案选B。


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】某课外兴趣小组用右图装置进行实验,试回答: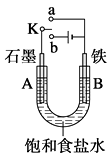
(1)若开始时开关K与a连接,则A电极反应式为。
(2)若开始时开关K与b连接,这种方法经常用于金属的防护,这种防护措施叫做 , 则A电极反应式为;B电极反应式为。
(3)开关K与b连接,将饱和食盐水换成CuSO4溶液,则A电极反应式为 , 该反应的离子方程式为 ,电解一段时间后(溶液仍然为蓝色),溶液的pH值将(填“变大”、“变小”、“不变”),若将电解质溶液恢复至原状,应补充 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正丁烷与异丁烷互为同分异构体的依据是( )
A.具有相似的化学性质
B.具有相同的物理性质
C.分子具有相同的空间结构
D.分子式相同,但分子内碳原子的连接方式不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示装置中,观察到电流计指针偏转,M棒变粗,N棒变细,其中P为电解质溶液。由此判断M、N、P所代表的物质可能是( )

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若不断地升高温度,实现“雪花→水→水蒸气→氧气和氢气”的转化。在转化的各阶段被破坏的粒子间的主要相互作用依次是
A. 氢键;分子间作用力;非极性键
B. 氢键;氢键;极性键[
C. 氢键;极性键;分子间作用力
D. 分子间作用力;氢键;非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是25 ℃时某些弱酸的电离平衡常数。
化学式 | CH3COOH | HClO | H2CO3 | H2C2O4 |
Ka | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 | Ka1=5.9×10-2 |
(1)H2C2O4与含等物质的量的KOH的溶液反应后所得溶液呈酸性,该溶液中各离子浓度由大到小的顺序为。
(2)向0.1 mol·L-1 CH3COOH溶液中滴加NaOH溶液至c(CH3COOH)∶c(CH3COO-)=5∶9,此时溶液pH=。
(3)向碳酸钠溶液中滴加少量氯水的离子方程式为。
(4)若0.1mol·L-1CH3COOH溶液与0.1mol·L-1NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,则c(Na+)-c(CH3COO-)=mol·L-1(填精确计算结果)。
(5)将CH3COOH溶液与大理石反应所产生的标况下44.8L气体全部通入到2L 1.5mol/L的NaOH溶液中充分反应,则溶液中所有离子的物质的量浓度由大到小的顺序为。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】As2O3在医药、电子等领域有重要应用。某含砷元素(As)的工业废水经如下流程转化为粗As2O3。
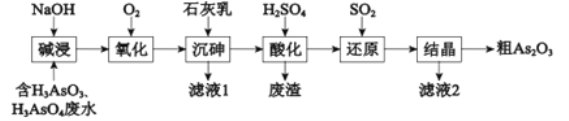
(1)“碱浸”的目的是将废水中的H3AsO3和H3AsO4转化为盐.H3AsO4转化为Na3AsO4反应的化学方程式是__________.
(2)“氧化”时,1molAsO33-转化为AsO43-至少需要O2___________.
(3)“沉砷”是将砷元素转化为Ca5(AsO4)3OH沉淀,发生的主要反应有:
a.Ca(OH)2(s)![]() Ca2+(aq)+2OH-(aq)△H<0
Ca2+(aq)+2OH-(aq)△H<0
b.5Ca2++OH-+3AsO43-![]() Ca5(AsO4)3OH △H>0
Ca5(AsO4)3OH △H>0
研究表明:“沉砷”的最佳温度是85℃.高于85℃后,随温度升高,沉淀率________(填“提高”或“下降”)。用化学平衡原理解释其原因是_________。
(4)“还原”过程中H3AsO4转化为H3AsO3,反应的化学方程式是_________.
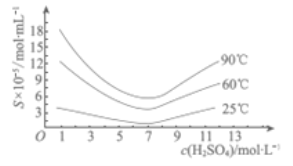
(5)“还原”后加热溶液,H3AsO3分解为As2O3,同时结晶得到粗As2O3.As2O3在不同温度和不同浓度硫酸中的溶解度(S)曲线如右图所示.为了提高粗As2O3的沉淀率,“结晶”过程进行的操作是___________.
(6)下列说法中,正确的是__________(填字母).
a.粗As2O3中含有CaSO4
b.工业生产中,滤液1、2和废渣一同弃掉
c.通过先“沉砷”后“酸化”的顺序,可以达到富集砷元素的目的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乳酸薄荷酯简称ML,可添加到牙膏、口香糖、饮料等中,有长效的清凉效果,其结构简式如下图所示。下列说法正确的是

A. ML的分子式为:C13H28O3 B. 1mol ML完全水解能消耗2mol NaOH
C. ML发生消去反应的产物只有一种结构 D. ML分子中的所有碳原子在同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关反应的叙述不正确的是
A.有元素化合价发生变化的反应一定是氧化还原反应
B.分解反应的反应物只有一种
C.化合反应的生成物只有一种
D.有单质生成的反应一定是置换反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com