
【题目】依据Cd(Hg)+Hg2SO4=3Hg+Cd2++SO42-反应原理,设计出韦斯顿标准电池,其简易装置如图。下列有关该电池的说法正确的是( )
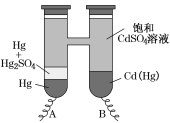
A.电池工作时Cd2+向电极B移动
B.电极A上发生反应Hg2SO4+2e-=2Hg+SO42-
C.电极B上发生反应Cd(Hg)-4e-=Hg2++Cd2+
D.反应中每生成a mol Hg转移3a mol电子
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,C(s)+CO2(g)![]() 2CO (g) ΔH>0。下列有关叙述正确的是
2CO (g) ΔH>0。下列有关叙述正确的是
A. 升高温度,v(正)增大,v(逆)减小
B. 增大压强,v(正)增大,v(逆)增大
C. 恒温恒压,再充入N2,反应速率不变
D. 增加炭的用量,v(正)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C都为短周期元素,它们在周期表中的位置如图所示。已知B、C两元素在周期表中族序数之和是A元素族序数的2倍;B、C元素的原子序数之和是A元素原子序数的4倍,则A、B、C符合的一组是( )

A.铍、钠、铝B.硼、镁、硅C.碳、铝、磷D.氧、磷、氯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可以证明可逆反应N2+3H2![]() 2NH3已达到平衡状态的是( )
2NH3已达到平衡状态的是( )
①一个N![]() N键断裂的同时,有6个N-H键断裂
N键断裂的同时,有6个N-H键断裂
②v(NH3)=0.4mol·L-1·min-1,v(H2)=0.6mol·L-1·min-1
③保持其他条件不变时,体系压强不再改变;
④NH3、N2、H2的体积分数都不再改变;
⑤恒温恒容时,混合气体质量保持不变;
A.②③④B.①②④C.①③④D.③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L恒温密闭容器中发生反应![]() ;经2min,B的浓度减少
;经2min,B的浓度减少![]() 。对此反应的下列表述不正确的是( )
。对此反应的下列表述不正确的是( )
A.用A表示的反应速率是![]()
B.用B表示的反应速率是![]()
C.在2min末时,容器内压强不变
D.在这2min内C和D两物质浓度都逐渐增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下6种说法中正确的数目是
![]() 在硝酸蒸气的氛围中蒸干
在硝酸蒸气的氛围中蒸干![]() 溶液会得到
溶液会得到![]() 固体
固体
![]() 溶解度和
溶解度和![]() 一样只与温度有关
一样只与温度有关
![]() 使用精密pH试纸测出84消毒液的pH为
使用精密pH试纸测出84消毒液的pH为![]()
![]() 升温对于强酸、强碱pH不发生变化,弱酸升温pH变小
升温对于强酸、强碱pH不发生变化,弱酸升温pH变小
![]() 滴定氨水用甲基橙做指示剂效果更好
滴定氨水用甲基橙做指示剂效果更好
![]() 实验室制氢气,为加快氢气的生成速率,可向稀硫酸中滴加少量
实验室制氢气,为加快氢气的生成速率,可向稀硫酸中滴加少量![]() 溶液.
溶液.
A.1B.2C.3D.全部正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示。
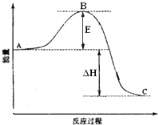
(已知1molSO2(g)氧化为1molSO3(g)的△H=-99kJ·mol-1。)请回答下列问题:
(1)图中A、C分别表示____、____,E的大小对该反应的反应热____(填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点____(填“变大”、“变小”或“不变”)。
(2)图中ΔH=____kJ·mol-1。
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化为V2O5。写也该催化循环机理的化学方程式____。
(4)已知单质硫的燃烧热为296kJ·mol-1,计算由S(s)生成3molSO3(g)的ΔH=____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】300 ℃时,将2 mol A和2 mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g)![]() 2 C(g)+2D(g) ΔH=Q, 2 min末达到平衡,生成0.8 mol D。
2 C(g)+2D(g) ΔH=Q, 2 min末达到平衡,生成0.8 mol D。
(1)300℃时,该反应的平衡常数表达式为K=______________,已知K300℃<K350℃,则ΔH____0(填“>”或“<”)。
(2)在2 min末时,B的平衡浓度为________,D的平均反应速率为________。
(3)若温度不变,缩小容器容积,则A的转化率________(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A+B→C △H <0,分两步进行 ① A+B→X △H>0 ② X→C △H<0 。下列示意图中,能正确表示总反应过程中能量变化的是
A.  B.
B. 
C.  D.
D. 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com