
ЎҫМвДҝЎҝКөСйКТЦРЛщУГөДВИЖшКЗУГПВБР·Ҫ·ЁЦЖИЎөДЈәMnO2+4HCl(ЕЁ) ![]() MnCl2+Cl2Ўь+2H2OЈ¬Т»ҙОКөСйЦР,УГ№эБҝөДЕЁСОЛб(ЖдГЬ¶ИОӘ1.19g/mLHClөДЦКБҝ·ЦКэОӘ36.5%)ёъТ»¶ЁБҝөД¶юСх»ҜГМ·ҙУҰ,¶юСх»ҜГМНкИ«ИЬҪв,ІъЙъБЛ5.6L(ұкЧјЧҙҝцПВ)өДВИЖшЎЈКФјЖЛг:
MnCl2+Cl2Ўь+2H2OЈ¬Т»ҙОКөСйЦР,УГ№эБҝөДЕЁСОЛб(ЖдГЬ¶ИОӘ1.19g/mLHClөДЦКБҝ·ЦКэОӘ36.5%)ёъТ»¶ЁБҝөД¶юСх»ҜГМ·ҙУҰ,¶юСх»ҜГМНкИ«ИЬҪв,ІъЙъБЛ5.6L(ұкЧјЧҙҝцПВ)өДВИЖшЎЈКФјЖЛг:
ЈЁ1Ј©ЕЁСОЛбөДОпЦКөДБҝЕЁ¶И_____Ј»
ЈЁ2Ј©·ҙУҰөДHClөДОпЦКөДБҝ____Ј»
ЈЁ3Ј©¶юСх»ҜГМөДЦКБҝ______ЎЈ

| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝўсЎўРҙіцПВБРУР»ъОпөДПөНіГьГы
(1) 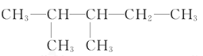 _____________
_____________
(2)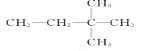 ______________
______________
IIЎўРҙіцПВБРУР»ъ»ҜәПОпөДҪб№№јтКҪЈ®
(3)2Ј¬2Ј¬3ИэјЧ»щ©Ғ3©ҒТТ»щјәНйЈә___________Ј®
(4)2©ҒјЧ»щ©Ғ3©ҒТТ»щёэНйЈә________Ј®
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝөвј°Жд»ҜәПОпФЪЙъІъЙъ»оЦРУҰУГ№г·әЎЈ»ШҙрПВБРОКМв:
ЈЁ1Ј©өҘЦКөвУл·ъ·ҙУҰҝЙөГIF5Ј¬КөСйұнГчТәМ¬IF5ҫЯУРТ»¶ЁөДөјөзРФФӯТтФЪУЪIF5өДЧФЕјөзАлЈЁИз:2H2O![]() H3O++OH-Ј©Ј¬IF5өДЧФЕјөзАл·ҪіМКҪОӘ_________
H3O++OH-Ј©Ј¬IF5өДЧФЕјөзАл·ҪіМКҪОӘ_________
ЈЁ2Ј©СЗБтЛбДЖәНөвЛбјШФЪЛбРФИЬТәЦРөД·ҙУҰКЗ:Na2SO3+KIO3+H2SO4 ЎъNa2SO4+K2SO4+I2+H2OЈЁОҙЕдЖҪЈ©ёГ·ҙУҰ№эіМәН»ъАнҪПёҙФУЈ¬Т»°гИПОӘ·ЦОӘТФПВІҪ:
ўЩIO3-+SO32-ЎъIO2-+SO42-ЈЁВэЈ©
ўЪIO2-+SO32-ЎъIO-+SO42-ЈЁҝмЈ©
ўЫ5I-+6H++I03-Ўъ3I2+3H2OЈЁҝмЈ©
ўЬI2+SO32-+H2O-Ўъ2I+SO42-+2H+ЈЁҝмЈ©
ёщҫЭЙПКцМхјюНЖІвЈ¬ҙЛ·ҙУҰөДЧЬ·ҙУҰЛЩВКУЙ_______ІҪ·ҙУҰҫц¶ЁЈЁМоРтәЕЈ©ЎЈИфФӨПИјУИЛөн·ЫИЬТәЈ¬УЙМвКцҝҙұШФЪ_____________АлЧУПыәДНкКұЈ¬ІЕ»бУРөн·ЫұдА¶өДПЦПуІъЙъЎЈ
ЈЁ3Ј©АлЧУөДОьёҪКЗЦШТӘөДСРҫҝҝОМв
ўЩТСЦӘSO2УлI2өД·ҙУҰЈ¬ЛЩВКј«ҝмЗТЖҪәвіЈКэҙуИЬТәЦРҙжФЪИзПВЖҪәв:I2(aq)+l-(aq)=l3-(aq)ПЦҪ«1 mol SO2»әНЁИлә¬1mol l2өДЛ®ИЬТәЦРЦБЗЎәГНкИ«·ҙУҰИЬТәЦРl3-өДОпЦКөДБҝn(l3-)КұјдЈЁtЈ©өДұд»ҜЗъПЯИзНј1ЛщКҫЎЈҝӘКјҪЧ¶ОЈ¬n(l3-)ЦрҪҘФцҙуөДФӯТтКЗ_____
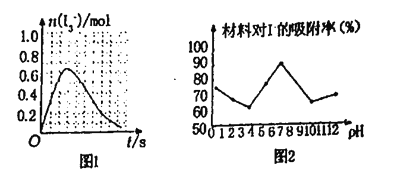
ўЪҝЖСРРЎЧйУГРВРНІДБПAg/TiO2¶ФИЬТәЦРөвАлЧУҪшРРОьёҪСРҫҝЎЈИзНј2КЗІ»Н¬pHМхјюПВЈ¬өвАлЧУОьёҪР§№ыөДұд»ҜЗъПЯЎЈҫЭҙЛНЖ¶ПAg/TiO2ІДБПЧоККәПОьёҪ___________ЈЁМоЎ°ЛбРФЎұЎ°ЦРРФЎұ»тЎ°јоРФЎұЈ©ИЬТәЦРөДI-ЎЈ
ўЫВИ»ҜТшёҙәПОьёҪјБТІҝЙУРР§ОьёҪөвАлЧУВИ»ҜТшёҙәПОьёҪјБ¶ФөвАлЧУөДОьёҪ·ҙУҰОӘ:I-(aq)+AgCl(s)=Agl(s)+Cl-(aq)Ј¬·ҙУҰҙпөҪЖҪәвәуИЬТәЦРc(Cl-)=1.0molЎӨL-1.ФтИЬТәЦРc(I-)=______molЎӨL-1ЈЫk(AgCl)=2.0ЎБ10-10Ј¬k(Agl)=8.4ЎБ10-17ЈЭ
ЈЁ4Ј©Fe3+УлI-ФЪИЬТәЦР·ўЙъ·ҙУҰ:2Fe3++2I- ![]() 2Fe2++I2Ј¬ёГ·ҙУҰөДХэ·ҙУҰЛЩВКәНFe2+УлI-өДЕЁ¶И№ШПөОӘv=kЎӨcm(I-)ЎӨcn(Fe3+)ЈЁЖдЦРkОӘіЈКэЈ©ЎЈTЎжКұЈ¬КөСйІвөГcЈЁI-Ј©ЎўcЈЁFe3+Ј©Ул·ҙУҰЛЩВКөД№ШПөИзПВұнЈә
2Fe2++I2Ј¬ёГ·ҙУҰөДХэ·ҙУҰЛЩВКәНFe2+УлI-өДЕЁ¶И№ШПөОӘv=kЎӨcm(I-)ЎӨcn(Fe3+)ЈЁЖдЦРkОӘіЈКэЈ©ЎЈTЎжКұЈ¬КөСйІвөГcЈЁI-Ј©ЎўcЈЁFe3+Ј©Ул·ҙУҰЛЩВКөД№ШПөИзПВұнЈә
cЈЁI-Ј©/molL-1 | cЈЁFe3+Ј©/molL-1 | v/molL-1s-1 | |
ўЩ | 0.20 | 0.80 | 0.032k |
ўЪ | 0.60 | 0.40 | 0.144k |
ўЫ | 0.80 | 0.20 | 0.128k |
ўЩФЪv=kЎӨcm(I-)ЎӨcn(Fe3+)ЦРmЎўnөДЦөОӘ_____________ЈЁМоРтәЕЈ©
A.m=1n=1 B.m=1Ўўn=2 C.m=2Ўўn=1 D.m=2Ўўn=2
ўЪI-ЕЁ¶И¶Ф·ҙУҰЛЩВКөДУ°Пм_____ЈЁМоЎ°ҙуУЪЎұЎўЎ°РЎУЪЎұ»тЎ°өИУЪЎұЈ©Fe3+ЕЁ¶И¶Ф·ҙУҰЛЩВКөДУ°ПмЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝ»ҜәПОпKКЗУР»ъ№вөзІДБПЦРјдМеЎЈУЙ·јПгЧе»ҜәПОпAЦЖұёKөДәПіЙВ·ПЯИзПВЈә
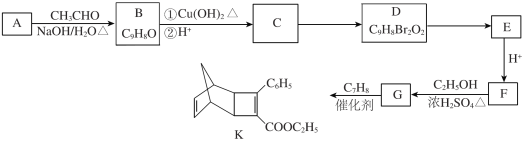
ТСЦӘЈә![]()
![]()
»ШҙрПВБРОКМвЈә
(1)AөДҪб№№јтКҪКЗ________ЎЈ
(2)CЦР№ЩДЬНЕКЗ________ЎЈ
(3)DЎъEөД·ҙУҰАаРНКЗ________ЎЈ
(4)УЙFЙъіЙGөД»ҜС§·ҪіМКҪКЗ________ЎЈ
(5)C7H8өДҪб№№јтКҪКЗ________ЎЈ
(6)·јПгЧе»ҜәПОпXКЗGөДН¬·ЦТм№№МеЈ¬ёГ·ЦЧУЦРіэұҪ»·НвЈ¬І»ә¬ЖдЛы»·ЧҙҪб№№Ј¬ЖдұҪ»·ЙПЦ»УР1ЦЦ»ҜС§»·ҫіөДЗвЎЈXДЬУлұҘәНМјЛбЗвДЖИЬТә·ҙУҰ·ЕіцCO2Ј¬Рҙіц·ыәПЙПКцТӘЗуөДXөДҪб№№јтКҪЈә________ЎЈ
(7)ТФ»·ОмНйәНМюQОӘФӯБПҫӯЛДІҪ·ҙУҰЦЖұё»ҜәПОп![]() Ј¬РҙіцУР№ШОпЦКөДҪб№№јтКҪЈЁЖдЛыОЮ»ъКФјБИОСЎЈ©ЎЈ
Ј¬РҙіцУР№ШОпЦКөДҪб№№јтКҪЈЁЖдЛыОЮ»ъКФјБИОСЎЈ©ЎЈ![]() QЈә____Ј»ЦРјдІъОп1Јә________Ј»ЦРјдІъОп2Јә____Ј»ЦРјдІъОп3Јә________ЎЈ
QЈә____Ј»ЦРјдІъОп1Јә________Ј»ЦРјдІъОп2Јә____Ј»ЦРјдІъОп3Јә________ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝФЪМе»эПаН¬өДБҪёцГЬұХИЭЖчЦР·ЦұрідВъC2H4әНC3H6ЖшМеЈ¬өұХвБҪёцГЬұХИЭЖчЦРОВ¶ИәНЖшМеГЬ¶ИПаөИКұЈ¬ПВБРЛө·ЁХэИ·өДКЗ
A. БҪЦЦЖшМеөД·ЦЧУКэПаөИ B. CЈІHЈҙұИCЈіHЈ¶өДЦКБҝРЎ
C. БҪЦЦЖшМеөДС№ЗҝПаөИ D. БҪЦЦЖшМеөДФӯЧУКэПаөИЈ®
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝҪ« 51.2g Cu НкИ«ИЬУЪККБҝЕЁПхЛбЦРЈ¬КХјҜөҪөӘөДСх»ҜОпЈЁә¬ NOЎўN2O4ЎўNO2Ј©өД»мәПОп№І 0.8molЈ¬ ХвР©ЖшМеЗЎәГДЬұ» 600mL 2 molЎӨLЎӘ1NaOH ИЬТәНкИ«ОьКХЈ¬ЙъіЙә¬ NaNO3 әНNaNO2 өДСОИЬТәЈ¬ЖдЦР NaNO3 өДОпЦКөДБҝОӘ( )
A. 0.2mol B. 0.4mol C. 0.6mol D. 0.8mol
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝ450ЎжКұЈ¬ФЪДіәгИЭГЬұХИЭЖчЦРҙжФЪ·ҙУҰЈәC(s)Ј«2NO(g)![]() N2(g)Ј«CO2(g)Ј¬ПВБРЛө·ЁДЬЧч ОӘЕР¶ПёГ·ҙУҰҙпөҪ»ҜС§ЖҪәвЧҙМ¬ұкЦҫөДКЗ
N2(g)Ј«CO2(g)Ј¬ПВБРЛө·ЁДЬЧч ОӘЕР¶ПёГ·ҙУҰҙпөҪ»ҜС§ЖҪәвЧҙМ¬ұкЦҫөДКЗ
A. ИЭЖчДЪС№ЗҝұЈіЦІ»ұдB. vХэ(N2)=2vДж(NO)
C. N2УлCO2өДОпЦКөДБҝЦ®ұИОӘ1ЎГ1D. ИЭЖчДЪ»мәПЖшМеөДГЬ¶ИұЈіЦІ»ұд
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝ°ҙТӘЗуНкіЙПВБРМвДҝЈә
(1)РҙіцУГNa2O2УлЛ®өД»ҜС§·ҪіМКҪЈә__________________________________
(2)РҙіцFeФЪCl2ЦРИјЙХ»ҜС§·ҪіМКҪЈә__________________________________
(3)РҙіцУГCl2УлNaOHЦЖПы¶ҫТәөДАлЧУ·ҪіМКҪЈә______________________________
(4)РҙіцNaHCO3өзАл·ҪіМКҪЈә___________________________________
(5)РҙіцЗвСх»ҜДЖИЬТәУлПЎБтЛб·ҙУҰөДАлЧУ·ҪіМКҪ__________________
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝәЈЛ®КЗЦШТӘөДЧКФҙЈ¬ҝЙТФЦЖұёТ»ПөБРОпЦКЈ¬
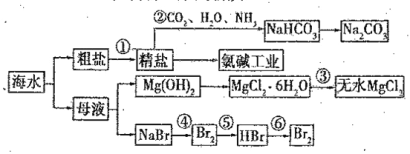
ПВБРЛө·ЁХэИ·өДКЗЈЁ Ј©
AЈ®ІҪЦиўЪЦРЈ¬УҰПИНЁCO2 Ј¬ФЩНЁNH3
BЈ®ІҪЦиўЫҝЙҪ«MgCl2ЎӨ6H2Oҫ§МеФЪҝХЖшЦРЦұҪУјУИИНСЛ®
CЈ®ІҪЦиўЬЎўўЭЎўўЮ·ҙУҰЦРЈ¬деФӘЛШҫщұ»Сх»Ҝ
DЈ®іэИҘҙЦСОЦРөД SO42-ЎўCa2+ ЎўMg2+ өИФУЦКЈ¬јУИлКФјБј°Па№ШІЩЧчЛіРтҝЙТФКЗЈәNaOHИЬТәЎъBaCl2 ИЬТәЎъNa2CO3 ИЬТәЎъ№эВЛЎъСОЛб
Ійҝҙҙр°ёәНҪвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com