
【题目】Ⅰ、写出下列有机物的系统命名
(1) 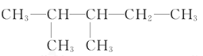 _____________
_____________
(2)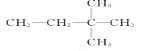 ______________
______________
II、写出下列有机化合物的结构简式.
(3)2,2,3三甲基﹣3﹣乙基己烷:___________.
(4)2﹣甲基﹣3﹣乙基庚烷:________.
【答案】2,3-二甲基戊烷 2,2-二甲基丁烷 CH3C(CH3)2C(CH3)(CH2CH3)CH2CH2CH3 CH3CH(CH3)CH(CH2CH3)CH2CH2CH2CH3
【解析】
(1)烷烃命名原则:
①长——选最长碳链为主链;
②多——遇等长碳链时,支链最多为主链;
③近——离支链最近一端编号;
④小——支链编号之和最小;看结构简式,从右端或左端看,均符合“近—离支链最近一端编号”的原则;
⑤简——两取代基距离主链两端等距离时,从简单取代基开始编号;如取代基不同,就把简单的写在前面,复杂的写在后面。
(1)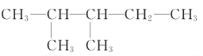 中最长碳链含有5个C,主链为戊烷,编号从距离甲基最近的左端开始,在2、3号C各含有1个甲基,该有机物名称为:2,3-二甲基戊烷,故答案为:2,3-二甲基戊烷;
中最长碳链含有5个C,主链为戊烷,编号从距离甲基最近的左端开始,在2、3号C各含有1个甲基,该有机物名称为:2,3-二甲基戊烷,故答案为:2,3-二甲基戊烷;
(2)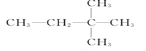 中最长碳链含有4个C,主链为丁烷,编号从距离甲基最近的右端开始,在2号C含有2个甲基,该有机物名称为:2,2-二甲基丁烷,故答案为:2,2-二甲基丁烷。
中最长碳链含有4个C,主链为丁烷,编号从距离甲基最近的右端开始,在2号C含有2个甲基,该有机物名称为:2,2-二甲基丁烷,故答案为:2,2-二甲基丁烷。
(3)2,2,3-三甲基-3-乙基己烷中主链含6个C,2号C上有2个甲基,3号C上有1个甲基、1个乙基,所以该有机物的结构简式为:CH3C(CH3)2C(CH3)(CH2CH3)CH2CH2CH3,故答案为:CH3C(CH3)2C(CH3)(CH2CH3)CH2CH2CH3。
(4)2-甲基-3-乙基庚烷中主链含7个C,2号C上有1个甲基,3号C上有1个乙基,所以该有机物的结构简式为CH3CH(CH3)CH(CH2CH3)CH2CH2CH2CH3,故答案为:CH3CH(CH3)CH(CH2CH3)CH2CH2CH2CH3。


科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、X均为短周期元素形成的无机物,存在下图所示转化关系(部分生成物和反应条件略去);已知A 由短周期非金属元素组成,B具有漂白性且光照易分解。请回答以下问题:
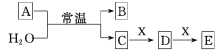
(1)若A为单质,且C为一元强酸。
①写出一种工业制备单质A的离子方程式: ____________________。
②X可能为________(填字母代号)。
a.NaOH b.AlCl3 c.Na2CO3 d.NaAlO2
(2)若A为两种元素形成的化合物,且E与水反应生成的G的浓溶液遇C有白烟产生。
①A与H2O反应的化学方程式为_____________________________。
②室温下,NH2OH(羟氨)会发生分解生成C、D,试写出其分解反应的化学方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气净化中的一个反应如下:2NO(g)+2CO(g)![]() N2(g)+2CO2(g)△H=-373.4kJ/mol,若反应在恒容的密闭容器中达到平衡状态,下列有关说法正确的是( )
N2(g)+2CO2(g)△H=-373.4kJ/mol,若反应在恒容的密闭容器中达到平衡状态,下列有关说法正确的是( )
A.其它条件不变,加入催化剂,△H变大
B.充入氦气使体系压强增大,可提高反应物的转化率
C.及时除去二氧化碳,有利于NO的转化
D.若升高温度,该反应的平衡常数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿托酸是一种常用的医药中间体,其结构如图所示: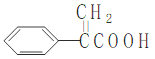 。下列有关说法中错误的是( )
。下列有关说法中错误的是( )
A.溴单质能与阿托酸发生加成反应
B.阿托酸能与硝酸发生取代反应
C.可用酸性KMnO4溶液区别阿托酸与苯
D.阿托酸分子中含有4个碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等体积,不同浓度的NaCl、MgCl2、AlCl3三种溶液分别与等体积等物质和量浓度的AgNO3溶液恰好完全反应,则NaCl、MgCl2、AlCl3三种溶液中Cl-的物质的量浓度之比是
A.1:2:3B.3:2:1C.6:3:2D.1:1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘酸钾可用作食用盐的加碘剂,为无色或白色颗粒或粉末状结晶 ,加热至560℃ 开始分解,是一种较强的氧化剂,水溶液呈中性,溶解度在0℃ 时为4.74g,100℃ 时为32.3g。 下图是利用过氧化氢氧化法制备碘酸钾的工业流程 :
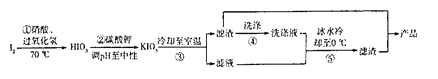
(1)步骤①需控制温度在70℃ 左右,不能太高,可能的原因是_______;不能太低 ,原因是________________________
(2)写出步骤②中主要反应的离子方程式:__________
(3)步骤⑤用冰水冷却至0℃ ,过滤出碘酸钾晶体,再用适量冰水洗涤2~3次。用冰水洗涤的优点是_____________
(4)产品纯度测定:取产品9.0g,加适量水溶解并配成250mL溶液。取出25.00mL该溶液并用稀硫酸酸化,加入过量的KI溶液,使碘酸钾反应完全,最后加入指示剂,用物质的量浓度为1.00molL-1的Na2S2O3溶液滴定,消耗25.00mL该滴定液时恰好达到滴定终点。已知![]()
①实验中可用_______作指示剂。
②产品的纯度为_____%(精确到小数点后两位)。求得的纯度比实际值偏大,可能的原因是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。该反应进行过程中能量的变化(单位为kJ·mol-1)如图所示。请回答下列问题:
CH3OH(g)+H2O(g)。该反应进行过程中能量的变化(单位为kJ·mol-1)如图所示。请回答下列问题:

(1)观察图象可知上述反应过程中,断裂反应物中的化学键吸收的总能量________(填“大于”“小于”或“等于”)形成生成物中的化学键释放的总能量。
(2)甲醇的结构类似于乙醇,试写出甲醇的结构式:______。甲醇分子中的化学键类型是____(填“离子键”或“共价键”)。
(3)科研人员开发出一种新型甲醇燃料电池。其电解质溶液是KOH溶液,在该电池的负极发生反应的物质是________,发生的是________(填“氧化”或“还原”)反应。
(4)欲使合成甲醇的化学反应速率加快,请写出两条措施:_______。
(5)下列事实能表明该反应已达平衡状态的是________(填序号)。
A. CO2(g)的浓度不再发生变化
B. 单位时间内消耗1mol CO2的同时生成3mol H2
C. 在一个绝热的容器中,混合物的温度不再发生变化
D. 在一个容积固定的容器内,压强不再发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中所用的氯气是用下列方法制取的:MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,一次实验中,用过量的浓盐酸(其密度为1.19g/mLHCl的质量分数为36.5%)跟一定量的二氧化锰反应,二氧化锰完全溶解,产生了5.6L(标准状况下)的氯气。试计算:
MnCl2+Cl2↑+2H2O,一次实验中,用过量的浓盐酸(其密度为1.19g/mLHCl的质量分数为36.5%)跟一定量的二氧化锰反应,二氧化锰完全溶解,产生了5.6L(标准状况下)的氯气。试计算:
(1)浓盐酸的物质的量浓度_____;
(2)反应的HCl的物质的量____;
(3)二氧化锰的质量______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com