
����Ŀ�����ǻ�ѧʵ���Ҽ����������е���Ҫ���ʣ�Ӧ�ù㷺��
(1)��֪25��ʱ��N2��g��+O2��g��![]() 2NO��g�� ��H1��+183kJ��mol
2NO��g�� ��H1��+183kJ��mol
2H2��g��+O2��g����2H2O��1�� ��H2��-571.6kJ��mol
4NH3��g��+5O2��g����4NO��g��+6H2O��1�� ��H3��-1164.4kJ��mol
��N2��g��+3H2��g��![]() 2NH3��g�� ��H��________kJ��mol
2NH3��g�� ��H��________kJ��mol
(2)�ں��º����ܱ������н��кϳɰ���Ӧ����ʼͶ��ʱ������Ũ�����±���
N2 | H2 | NH3 | |
Ͷ��I | 1.0mol/L | 3.0mol/L | 0 |
Ͷ��II | 0.5mol/L | 1.5mol/L | 1.0mol/L |
�ٰ�Ͷ��I���з�Ӧ����ôﵽ��ѧƽ��״̬ʱH2��ת����Ϊ40��������Ͷ��II���з�Ӧ����ʼʱ��Ӧ���еķ���Ϊ________��������������������������
��L��L1��L2����X�ɷֱ����ѹǿ���¶ȡ���ͼ��ʾLһ��ʱ���ϳɰ���Ӧ��H2��g����ƽ��ת������X
�ı仯��ϵ��
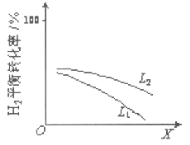
iX��������������_________��
ii�ж�L1��L2�Ĵ�С��ϵ�����������ɣ�_____________��
���𰸡�-92.2 ���� �¶� L1<L2�����¶�һ��ʱ��ѹǿԽ��ƽ��ת����Խ��
��������
��1����֪25��ʱ����N2��g��+O2��g��2NO��g����H=+183kJ/mol
��2H2��g��+O2��g��2H2O��l����H=��571.6kJ/mol
��4NH3��g��+5O2��g��4NO��g��+6H2O��l����H=��1164.4kJ/mol
���ݸ�˹���ɢ�+�ڡ�![]() ��
��![]() ���۵ã�N2��g��+3H2��g��2NH3��g����H=��+183��571.6��+��1164.4��kJ/mol =��92.2kJ/mol��
���۵ã�N2��g��+3H2��g��2NH3��g����H=��+183��571.6��+��1164.4��kJ/mol =��92.2kJ/mol��
��2���ٰ�Ͷ�Ϣ�����ȫת�����ұߣ�����Ͷ�Ϣ���ȫ��ͬ��Ϊ��ȫ��Чƽ�⣬����Ͷ�Ϣ���з�Ӧƽ��ʱH2��Ũ��ҲΪ3.0mol/L����1��40%��=1.8mol/L������Ͷ�Ϣ���з�Ӧ����ʼʱ��Ӧ���еķ���Ϊ������
��i����ͼ��֪��XԽ������ת����Խ�ͣ������¶�ƽ�����淴Ӧ�����ƶ���������ת���ʼ�С����X��ʾ�¶ȣ�
ii����N2��g��+3H2��g��2NH3��g����H��0���¶ȸߣ�����ת����С��ѹǿ��ƽ�������ƶ�������ת���ʴ�ͼ�е��¶�ʱL2��Ӧ������ת���ʴ���ѹǿL1��L2��


 ������״Ԫ���Ծ�ϵ�д�
������״Ԫ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ʤ���������ࡱָ���ǵ�����������ʹ����ʷ�ƾõ�Ⱦ��֮һ������Ϊ��ͳ�Ʊ������Ĺ��̣�

����˵������ȷ���ǣ� ��
A. �����ķ���ʽΪC16H10N2O2
B. ���ݷ����̷����ķ�ӦΪȡ����Ӧ
C. ����ӵı����ϵĶ��ȴ�����4��
D. 1 mol�������H2�ӳ�ʱ������4 mol H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ԭ������Ȼ��һ����Ҫ�Ļ���ԭ��,������ʵ������������ԭ�����͵���
A. NO2������ѹ������ɫ�ȱ�����dz
B. ��2HI(g) ![]() H2(g)��I2(g)ƽ����ϵ��ѹ����ɫѸ�ٱ���
H2(g)��I2(g)ƽ����ϵ��ѹ����ɫѸ�ٱ���
C. �ϳɰ���ҵ���ø��¡���ѹ������߰��IJ���
D. ��������������Һʱ��������������м�Է�ֹ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ػ������ڻ�����ҽҩ�����ϵ��������Ź㷺��Ӧ�á��ش��������⣺
��1�����й��ڽ�������������˵������ȷ����______��������ĸ���ţ�
a��������û�з������뱥����
b���������ǽ���ԭ�������ɵ��Ӽ�������
c�������۷е㲻ͬ��ԭ������ý�����ǿ������
d�����������ۿɽ��ͽ������ϵ���չ�ԣ����ܽ��ͽ��������õĵ�����
��2�����㷺���ڴ���������ҵ����̬��ԭ�ӵļ۲�����Ų�ͼΪ_________________��
��3����ï���ֽ�˫�����ϩ����[Fe(C5H5)2]���۵���172.5��173 �棬100 ��������������ï������_____���塣��֪�����еĴ��������÷���![]() ��ʾ������m���������γɴ�������ԭ������n���������γɴ������ĵ��������籽�����еĴ������ɱ�ʾΪ
��ʾ������m���������γɴ�������ԭ������n���������γɴ������ĵ��������籽�����еĴ������ɱ�ʾΪ![]() ������֪��ï����ÿ��ï������һ����λ����ɣ���ÿ�����еĴ�����Ӧ��ʾΪ________________��
������֪��ï����ÿ��ï������һ����λ����ɣ���ÿ�����еĴ�����Ӧ��ʾΪ________________��
��4��ͭ�����γ�һ�����ӻ�����[Cu(NH3)4(H2O)2]SO4����Ҫȷ��[Cu(NH3)4(H2O)2]SO4�Ǿ��廹�ǷǾ��壬���ѧ�ķ����Ƕ������______ʵ�飬���������ӵĿռ乹����_____���û��������ʱ����ʧȥ�������H2O��ԭ����_______________________��
��5��������֣�ֻ��þ������̼����Ԫ�صľ���Ҳ���г����ԣ��������γɵľ�������������ṹ��ͼ��ʾ��
����Mg���ڵ�Ni��________����
��ԭ����������ɱ�ʾ�����ڲ���ԭ�ӵ����λ�á��þ�����ԭ�ӵ��������ΪaΪ(0��0��0)��bΪ(1/2��1/2��0)��dΪ(1��1��1)����cԭ�ӵ��������Ϊ_______��
����������Ni��Mg֮�����̾���Ϊa pm�������ӵ�������ֵΪNA��������ܶ��ѣ�______g��cm��3(�ú�a��NA�Ĵ���ʽ��ʾ)��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС���ͬѧ���������������ؾ���K3[Fe(C2O4)3]��3H2O�ֽ��ʵ��̽������С�����ۣ��������������װ�ý���ʵ�顣��ƿB��ʢ�б���NH4Cl�ͱ���NaNO2���Һ(������ʵ������N2)�������C1��װ�м�ʯ�ҡ�

(1)B�з�����Ӧ�Ļ�ѧ����ʽΪ______________________________________��
(2)C2��������_________________��C3��ʢװ���Լ���___________________��
(3)��ʵ���й۲쵽E1��E4�еij���ʯ��ˮ������ǣ���E3�е�������___________________��֤�����������___________________��
(4)ʵ��װ������2���ƾ��ƣ��ȵ�ȼA1��һ��ʱ���Ϩ��A1���رջ���a���ٵ�ȼA2����D�е���Ʒ��ַ�Ӧ���ٴδ���a����ȼA1����ڶ��ε�ȼA1��������________________________________________________________��
(5)��С��ͬѧ�������Ϻ���֪�� D�й�������У���Ԫ�ز�������������ʽ���ڣ�����ֻ��K2CO3��ʵ����C2��C3������5.4g����D�й�������������ˮ�������������������Ϊ6.88g��ͨ�����㣬�����������Ԫ�صĴ�����ʽΪ______�����ʾ����������ʵ�������
��Ҫͨ��ʵ���о��������ۣ���3%H2O2������ˮ�⣬����Ҫ�����Լ��е�___________��
A��1.0 mol��L��1HNO3 B��1.0 mol��L��1���� C��1.0 mol��L��1NaOH��Һ
D��0.1 mol��L��1KI��Һ E��0.1 mol��L��1CuSO4��Һ F��20%KSCN��Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ����ѧ��ѧ�г����ڻ����ķ�����ᴿ��װ�ã������װ�ûش��������⣺
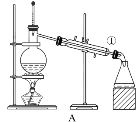
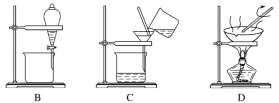
��1�����Ȼ�����Һ�еõ��Ȼ��ع���ѡ��װ��___(�����װ��ͼ����ĸ����ͬ)����ȥ����ˮ�е�Cl��������ѡ��װ��____��
��2���ӵ�ˮ�з����I2��ѡ��װ��___���÷��뷽��������Ϊ____��
��3��װ��A�Тٵ�������____����ˮ�ķ�����____��װ��B�ڷ�ҺʱΪʹҺ��˳�����£�Ӧ���еľ��������____��
��4����ˮ���̲��ŷḻ����Դ����ʵ������ȡ������ˮ��������ͼ���̵�ʵ�飺
![]()
����1�������к�Ca2����Mg2����SO42-�����ʣ���Ҫ�ᴿ������ۺ����á������ᴿ�IJ����У��ټ��������Na2CO3��Һ���ڼ��������BaCl2��Һ���ۼ��������NaOH��Һ���ܵ�����Һ��pH����7�����ܽ⣻���ˣ�����������ȷ�IJ���˳����____(����ĸ)��
a���ݢڢۢ٢ޢܢ� b���ݢ٢ڢۢޢܢ�
c���ݢڢ٢ۢܢޢ� d���ݢۢڢ٢ޢܢ�
����2������ѡ˳�����ʱ������ܵĻ�ѧ����ʽ��____��
����3���ɺ�ˮ���Ȼ��ƾ����ʵ�������Ҫ�õ�����Ҫװ����___(�Ӹ���������װ����ѡ��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС������H2C2O4��Һ������KMnO4��Һ��Ӧ��̽������������Ի�ѧ��Ӧ���ʵ�Ӱ������ʵ��ʱ���ȷֱ���ȡ������Һ��Ȼ�����Թ���Ѹ����Ͼ��ȣ���ʼ��ʱ��ͨ���ⶨ��ɫ����ʱ�����жϷ�Ӧ�Ŀ�������С����������·�����
ʵ���� | �����£��Թ��������Լ���������/mL | ��������Һ��ɫ������ɫ����ʱ��/min | |||
0.6mol/L H2C2O4��Һ | H2O | 0.2mol/LKMnO4��Һ | 3mol/L ϡ���� | ||
1 | 3.0 | 2.0 | 2.0 | 3.0 | 4.0 |
2 | 3.0 | 3.0 | 2.0 | 2.0 | 5.2 |
3 | 3.0 | 4.0 | 2.0 | 1.0 | 6.4 |
(1)�����ϱ��е�ʵ�����ݣ����Եõ��Ľ�����______________________________��
(2)��С��ͬѧ���ݾ��������n(Mn2+)��ʱ��仯���Ƶ�ʾ��ͼ����ͼ1��ʾ������ͬѧ�������е�ʵ�����Ϸ��֣���ʵ�������n(Mn2+)��ʱ��仯������Ӧ��ͼ2��ʾ����С��ͬѧ����ͼ2��ʾ��Ϣ������µļ��裬����������ʵ��̽����

��С��ͬѧ����ļ�����___________________________________��
�����������С��ͬѧ���ʵ�鷽��������д���пհס�
ʵ���� | �����£��Թ��������Լ���������/mL | �����Թ��м�����������X | ��������Һ��ɫ������ɫ����ʱ��/min | |||
0.6mol/L H2C2O4��Һ | H2O | 0.2mol/LKMnO4��Һ | 3mol/L ϡ���� | |||
4 | 3.0 | 2.0 | 2.0 | 3.0 | t | |
����X��__________��
������С��ͬѧ����ļ��������ʱ��t__________4.0min����>��=��<����
(3)Ϊ̽���¶ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬��С��ͬѧ��������ʵ������ϼ�������ʵ�飬���������С��ͬѧ��ɸ�ʵ�鷽�����____________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�����ϩ����������ȷ���ǣ� ��
A.��ʹ��ˮ��ɫB.�ܹ�ȼ�գ�ͬʱ��������
C.�������Ը�����ط����ӳɷ�ӦD.�����������߷��Ӳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)ij�л�����C��H��O����Ԫ����ɣ����ģ����ͼ��ʾ��
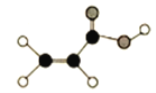
�ٺ��еĹ�����������_______��
��д�����л���������Ʒ�Ӧ�Ļ�ѧ����ʽ_______��
(2)���ֳ����л�����ӵı���ģ��ʾ��ͼ���£����мס��ҡ���Ϊ������Ϊ���������

�ٿ��Լ�����ҵ��Լ�Ϊ_________��
a.ϡ���� b.������Ȼ�̼��Һ c.ˮ d.���Ը��������Һ
�������������ж�����������ζ���Ҳ�����ˮ���ܶȱ�ˮС����_________�������ƣ���
���ҺͶ������ʵ�����1.5mol����ȫȼ����Ҫ�����������ʵ�����_______��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com