
【题目】若某原子在处于能量最低状态时,外围电子排布为![]() ,则下列说法错误的是( )
,则下列说法错误的是( )
A. 该元素可能有+3价
B. 该元素位于第5周期第IIIB族
C. 该元素原子核外共有39个不同运动状态的电子
D. 该元素基态原子第N能层上还有5个空轨道
【答案】D
【解析】
某原子在处于能量最低状态时,外围电子排布为4d15s2,应为Y元素,位于周期表第ⅢB族,处于d区,为金属元素,原子核外电子排布为[Kr]4d15s2。
A项、由Y原子的外围电子排布为4d15s2可知,该原子可能失去5s轨道上的2个电子和4d轨道上的1个电子得到Y3+离子,故A正确;
B项、由基态原子的核外电子排布可知该元素位于周期表第五周期第ⅢB族,故B正确;
C项、由原子核外电子排布为[Kr]4d15s2可知Y元素原子中共有39个电子,有39个不同运动状态的电子,故C正确;
D项、该元素原子处于能量最低状态时,原子中共有1个未成对电子,为4d1,第N能层的4d能级上有4个空轨道,故D错误。
故选D。


科目:高中化学 来源: 题型:
【题目】松油醇是一种调香香精,它是α、β、γ三种同分异构体组成的混合物,可由松节油分馏产品A(下式中的18是为区分两个羟基而人为加上去的)经下列反应制得:
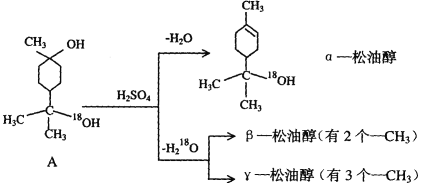
(1)A分子中的官能团名称是_________________。
(2)A分子能发生的反应类型是________。
a.加成 b.取代 c.催化氧化 d.消去
(3)α-松油醇的分子式_________________。
(4)α-松油醇所属的有机物类别是________。
a.酸 b.醛 c.烯烃 d.不饱和醇
(5)写结构简式:β-松油醇_____________,γ-松油醇_____________。
(6)写出α-松油醇与乙酸发生酯化反应的方程:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用图所示装置检验乙烯时不需要除杂的是
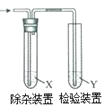
乙烯的制备 | 试剂X | 试剂Y | |
A | CH3CH2Br与NaOH乙醇溶液共热 | H2O | KMnO4酸性溶液 |
B | CH3CH2Br与NaOH乙醇溶液共热 | H2O | Br2的CCl4溶液 |
C | CH3CH2OH与浓H2SO4共热至170℃ | NaOH溶液 | KMnO4酸性溶液 |
D | CH3CH2OH与浓H2SO4共热至170℃ | NaOH溶液 | Br2的CCl4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物I(分子式为C19H20O4)属于芳香酯类物质,是一种调香剂,其合成路线如下:

已知:①A属于脂肪烃,核磁共振氢谱显示有2组峰,面积比为3:1,其蒸气密度是相同条件下H2的28倍;D分子式为C4H8O3;E分子式为C4H6O2,能使溴水褪色。
②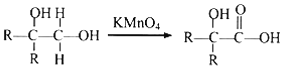 其中R为烃基。
其中R为烃基。
③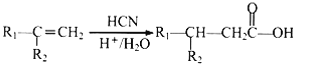 其中R1和R2均为烃基。
其中R1和R2均为烃基。
回答下列问题:
(1)A的结构简式为___________________。
(2)D中官能团的名称是______________________。
(3)反应②的化学方程式为______________。
(4)E的同系物K比E多一个碳原子,K有多种链状同分异构体,其中能发生银镜反应且能水解的有_______种。
(5)反应①~⑦属于取代反应的是__________(填序号)。
(6)反应⑦的化学方程式为_________________。
(7)参照上述合成路线,以 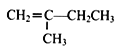 为原料(无机试剂任选),经4步反应制备可降解塑料
为原料(无机试剂任选),经4步反应制备可降解塑料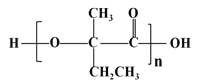 _____________。
_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表标出的是元素周期表的一部分元素,回答下列问题:
1 | ||||||||||||||||||
2 | A | B | C | |||||||||||||||
3 | D | E | F | G | H | I | J | K | ||||||||||
4 | M | |||||||||||||||||
(1)在上表用字母标出的12种元素中,化学性质最不活泼的是____(用元素符号表示,下同),金属性最强的是___,除稀有气体外第三周期中原子半径最小的是____,属于过渡元素的是___(该空格用表中的字母表示)。
(2)J的氢化物的电子式为____,最高价氧化物对应的水化物的化学式为___。
(3)为比较元素A和G的非金属性强弱,用下图所示的装置进行实验(夹持仪器已略去,装置气密性良好)。溶液B应该选用_____溶液,作用是_____,能说明A和G非金属性强弱的化学方程式是______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知酸性: ![]() >H2CO3>
>H2CO3>![]() >HCO3-;现要将
>HCO3-;现要将![]() 转变为
转变为 ![]() ,可行的方法是
,可行的方法是
A.向该溶液中加入足量的稀硫酸,加热
B.将该物质与稀硫酸共热后,再加入足量的NaOH溶液
C.将该物质与足量的NaOH溶液共热,再通入足量CO2气体
D.将该物质与稀硫酸共热后,再加入足量的Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ksp(CaCO3)=2.8×10-9及表中有关信息:
弱酸 | CH3COOH | H2CO3 |
电离平衡常数(常温) | Ka=1.8×10-5 | Ka1=4.3×10-7; Ka2=5.6×10-11 |
下列判断正确的是
A. 向Na2CO3溶液中滴入酚酞,溶液变红,主要原因是CO32-+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
B. 常温时,CH3COOH与CH3COONa混合溶液的pH=6,则 =18
=18
C. NaHCO3溶液中:c(OH-)-c(H+)=c(H2CO3)-c(CO32-)
D. 2×10-4 mol/L的Na2CO3溶液与CaCl2溶液等体积混合出现沉淀,则CaCl2溶液的浓度一定是5.6×10-5 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)燃料电池是一种高效、环境友好的发电装置。氢氧燃料电池已用于航天飞机。以氢氧化钾溶液为电解质溶液的这种电池的负极反应式为________,这种电池在放电使用一段时间后,电解质溶液中的c(OH-)将____(填“增大”“减小”或“不变”)。
(2)如图是银锌原电池装置的示意图,以硫酸铜为电解质溶液。回答下列问题:
锌为____极,该电极上发生_______反应(“氧化”或“还原”),电极反应式为___________,该原电池的总反应离子方程式为_______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图中装置进行实验,实验一段时间后,现象与预测不一致的是

①中物质 | ②中物质 | 实验预测 | |
A | 浓氨水 | 酚酞试液 | ②中溶液变为红色 |
B | 浓硝酸 | 淀粉KI溶液 | ②中溶液变为蓝色 |
C | 浓盐酸 | 浓氨水 | 大烧杯中有白烟 |
D | 饱和的亚硫酸溶液 | 稀溴水 | ②中无明显变化 |
A. AB. BC. CD. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com