
����Ŀ���±��������Ԫ�����ڱ���һ����Ԫ�أ��ش��������⣺
1 | ||||||||||||||||||
2 | A | B | C | |||||||||||||||
3 | D | E | F | G | H | I | J | K | ||||||||||
4 | M | |||||||||||||||||
��1�����ϱ�����ĸ�����12��Ԫ���У���ѧ��������õ���____����Ԫ�ط��ű�ʾ����ͬ������������ǿ����___����ϡ�����������������ԭ�Ӱ뾶��С����____�����ڹ���Ԫ�ص���___���ÿո��ñ��е���ĸ��ʾ����
��2��J���⻯��ĵ���ʽΪ____������������Ӧ��ˮ����Ļ�ѧʽΪ___��
��3��Ϊ�Ƚ�Ԫ��A��G�ķǽ�����ǿ��������ͼ��ʾ��װ�ý���ʵ�飨�г���������ȥ��װ�����������ã�����ҺBӦ��ѡ��_____��Һ��������_____����˵��A��G�ǽ�����ǿ���Ļ�ѧ����ʽ��______��

���𰸡�Ar Na Cl M ![]() HClO4 ����NaHCO3 ��ȥCO2�е�HCl���� Na2SiO3 +CO2 +H2O = H2SiO3 ��+ Na2CO3������NaHCO3Ҳ�ɣ�
HClO4 ����NaHCO3 ��ȥCO2�е�HCl���� Na2SiO3 +CO2 +H2O = H2SiO3 ��+ Na2CO3������NaHCO3Ҳ�ɣ�
��������
����Ԫ�������ڱ��е����λ�������жϳ�Ԫ�����ƣ�Ȼ����Ԫ���������Լ��й����ʵ����ʷ������
����Ԫ�������ڱ��е�λ�ÿ�֪A��C��B��O��C��F��D��Na��E��Mg��F��Al��G��Si��H��P��I��S��J��Cl��K��Ar��M��Mn����
��1�����ϱ�����ĸ�����12��Ԫ���У���ѧ��������õ���ϡ������Ԫ��Ar����������ǿ����Na��ͬ������������ԭ�Ӱ뾶��С�����ϡ�����������������ԭ�Ӱ뾶��С����Cl�����ڹ���Ԫ�ص���M��
��2��J���⻯���ǹ��ۻ�����HCl������ʽΪ![]() ����Ԫ�ص������+7�ۣ�������������Ӧ��ˮ����Ļ�ѧʽΪHClO4��
����Ԫ�ص������+7�ۣ�������������Ӧ��ˮ����Ļ�ѧʽΪHClO4��
��3��Ҫ�Ƚ�Ԫ��C��Si�ķǽ�����ǿ�������Ը��ݽ�ǿ���Ʊ��������жϣ���������ʹ���ʯ��Ӧ���ɵĶ�����̼�к����Ȼ�������ʵ�飬��Ҫ���ñ���̼��������Һ��ȥ������ҺBӦ��ѡ�ñ���NaHCO3��Һ�������dz�ȥCO2�е�HCl���ʣ���˵��C��Si�ǽ�����ǿ���Ļ�ѧ����ʽ��Na2SiO3+CO2+H2O��H2SiO3��+Na2CO3��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС���ͬѧ����MnO2��Ũ���ᷴӦ����ȡ�������������֤������Ư���ԣ�����װ��(������������Ҫ����������װ��)���£�����˵����ȷ���ǣ� ��

A. װ��E�з�����Ӧ�����ӷ���ʽΪ��Cl2+OH-=Cl-+ClO-+H2O
B. �������������Ⱥ�˳��װ������˳������ΪDABAE
C. װ��E����Ҫ��;���Ʊ�NaClO
D. װ��D�������dz�ȥ�����е�HCl���ṩˮ��������֤HClO����Ư����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ũ����������ķ�Ӧ������һֱ̽�ֺ��о�����Ҫ����֮һ��
��.ͭ��Ũ���ᷴӦ�Ĺ����У������к�ɫ���ʳ��֣��Һ�ɫ����ΪCu2S������Cu2S�ķ�ӦΪaCu+bH2SO4![]() cCu2S+dCuSO4+eH2O����a��b=______.
cCu2S+dCuSO4+eH2O����a��b=______.
��.Ϊ�о����ʲ�������Ũ����ķ�Ӧ��ijѧϰС����̼�ظ�(������̼�ĺϽ�)����������̽�����
��̽��һ��(1)�����£���ҵ������������ʢ�����Ũ���ᣬ��ԭ����________��
(2)����Ũ�����ڼ���ʱ�Ļ�ѧ����ʽΪ��______________��
(3)��ȡ̼�ظ�6.0g����15.0mlŨ�����У����ȣ���ַ�Ӧ��õ���ҺX���ռ����������Y��
�ټ�ͬѧ��ΪX�г�Fe3+֮����ܺ���Fe2+����Ҫȷ�����е�Fe2+��Ӧѡ��____________��
a��KSCN��Һ����ˮ b�����ۺ�KSCN��Һ c��Ũ��ˮ d������KMnO4��Һ
����ͬѧȡ560mL(��״��������Yͨ��������ˮ�У�������Ӧ���������BaCl2��Һ�����ʵ�������ø������4.66g���ɴ���֪����Y��SO2���������Ϊ_______��
��̽��������������ʵ����SO2��������ķ�������ͬѧ��Ϊ����Y�л����ܺ���Q1��Q2�������壬����Q1�����ڱ�״�����ܶ�Ϊ0.0893g/L��Ϊ�����������̽��ʵ��װ��(ͼ�мг�����ʡ�ԣ������й�������ȫ��Ӧ)��
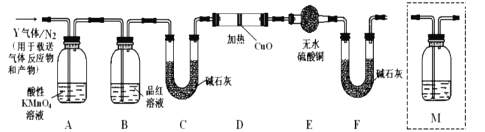
(4)װ��B���Լ���������__________��
(5)����Y�����е�![]() ������������ɵ�___________(�û�ѧ����ʽ��ʾ)��
������������ɵ�___________(�û�ѧ����ʽ��ʾ)��
(6)Ϊȷ��![]() �Ĵ��ڣ�����װ��������ϴ��ƿM��___________��
�Ĵ��ڣ�����װ��������ϴ��ƿM��___________��
a��A֮ǰ b��A-B�� c��B-C�� d��C-D��
��7���������Y�к���![]() ��Ԥ��ʵ������Ӧ��_________________��
��Ԥ��ʵ������Ӧ��_________________��
��.��һ��������Zn��100mLһ��Ũ�ȵ�H2SO4��ַ�Ӧ��
(1)����Ӧǰc(H2SO4)=12.0mol/L����Ӧ�����ʣ��п��������������65.0g������Ӧ�����Һϡ����1L����ʱ��Һ��c(SO42-)=______mo/L������SO2���(��״����)V(SO2)=______L��
(2)��(1)�в��������建��ͨ��100mL a mo/L NaOH��Һ�У�SO2��NaOH����ȫ���ģ���a��ȡֵ��ΧΪ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ӦA(g) + 3B(g)![]() 2C(g) + D(g)������ijʱ�������A��Ũ�ȱ仯��ʾ�Ļ�ѧ��Ӧ����Ϊ1mol��L-1��min-1�����ڴ�ʱ�������C��Ũ�ȱ仯��ʾ�Ļ�ѧ��Ӧ����Ϊ
2C(g) + D(g)������ijʱ�������A��Ũ�ȱ仯��ʾ�Ļ�ѧ��Ӧ����Ϊ1mol��L-1��min-1�����ڴ�ʱ�������C��Ũ�ȱ仯��ʾ�Ļ�ѧ��Ӧ����Ϊ
A. 0.5 mol��L-1��min-1B. 2 mol��L-1��min-1
C. 3 mol��L-1��min-1D. 1 mol��L-1��min-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ��������A��B��C������ͼ��ʾ��ת����ϵ������H����H1+��H2����A��C������( )

��Fe��FeCl3 ��C��CO2 ��AlCl3��NaAlO2 ��NaOH��NaHCO3 ��S��CuS ��Na2CO3��CO2
A���ڢۢܢ� B���ڢۢܢݢ� C���٢ڢۢܢ� D���٢ڢۢܢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����ijϡ�����pH = 2���������۴������
A. ����Һ��c��H+��=1��10-2 mol/LB. ����Һ��c��H+����c��(OH����
C. ����Һ��c(OH- ) =1��10-7 mol/LD. Kw = c(H+)��c(OH- ) = 1��10-14
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯�����Ц�H��0���ǣ� ��
A.������ľ̿��ԭ������̼B.��ҵ��ˮú���ķ�Ӧ
C.Ba(OH)28H2O��NH4Cl�ķ�ӦD.Һ��ʯ������ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʳ���¶���ڿ�������ɷֲ������仯����
A.Na2O2B.��ˮC.Na2CO3D.Fe(OH)2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݿ�ͼ����������˵������ȷ����
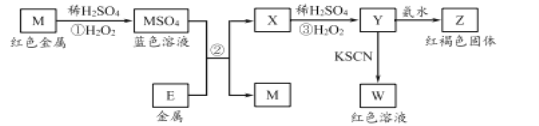
A. �ҹ�������������ʹ�÷�Ӧ��ұ������M�Ĺ���
B. M2+�������Ա�E2+��������ǿ
C. �ڷ�Ӧ����������ϡ���ᣬ���ܹ۲쵽���ɫ����
D. �ڷ�Ӧ����ϡ����ȱ��ֳ��������ֱ��ֳ�����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com