
【题目】在室温时,向![]() 溶液中滴加
溶液中滴加![]() 溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示
溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示![]() 无气体溢出
无气体溢出![]() ,以下说法不正确的是
,以下说法不正确的是![]()
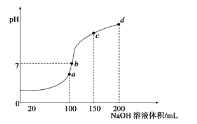
A.a点时水的电离程度最大
B.b点时溶液中的离子浓度关系有![]()
C.c点时溶液中的粒子浓度大小关系为![]()
D.d点时溶液中![]()
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:
【题目】(1)把0.2mol X气体和0.4mol Y气体混合于2L密闭容器中,使它们发生如下反应:![]() 末生成0.3mol W。若测知Z的浓度变化表示的反应速率为0.05mol
末生成0.3mol W。若测知Z的浓度变化表示的反应速率为0.05mol ![]() 。计算:
。计算:
①前2min内用Y 的浓度变化表示的反应速率为 ![]()
②化学方程式中n的值是 。
(2)在一定温度下,将4mol SO2与2mol O2放入4L的密闭容器中,在一定条件下反应,2SO2+O2![]() 2SO3。10min 时达到平衡状态。此时容器内压强比反应前减少20%,计算SO2的转化率为 。
2SO3。10min 时达到平衡状态。此时容器内压强比反应前减少20%,计算SO2的转化率为 。
(3)某温度时在2L容器中A、B、C 三种气态物质的物质的量(n)随时间(l)变化的曲线如图所示,由图中数据分析:

①该反应的化学方程式为
②下列叙述能说明上述反应达到平衡状态的是 。
A、混合气体的总物质的量不随时间的变化而变化
B、相同时间内消耗2n mol 的A的同时生成4nmol 的C
C、混合气体的总质量不随时间的变化而变化
D、容器内压强不再发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程都与热量变化有关,其中叙述正确的是
A.Ba(OH)2·8H2O与NH4Cl常温下混合就能反应,故该反应放热
B.已知2H2(g)+O2(g)=2H2O(g)ΔH=-483.6kJ·mol–1,故H2的燃烧热为241.8kJ·mol–1
C.已知H+-(aq)+OH-(aq)==H2O-(l)ΔH=-57.31kJ·mol–1,故Ba2+(aq)+H+(aq)+OH-(aq)+SO42-(aq)=H2O(1)+BaSO4(s)ΔH<-57.31kJ·mol–1
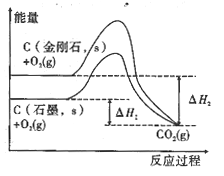
D.由图可知,反应C(金刚石,s)=C(石墨,s)的焓变ΔH=ΔH1-ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
回答下列问题:
(1).上述反应中属于放热反应的是________。
(2).H2的燃烧热![]() ________________;C的燃烧热
________________;C的燃烧热![]() ________________。
________________。
(3).燃烧![]() 生成液态水,放出的热量为________。
生成液态水,放出的热量为________。
(4).写出CO燃烧的热化学方程式:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,H3A水溶液(一种酸溶液)中含A的各种粒子的分布分数[平衡时某种粒子的浓度占各种粒子浓度之和的分数(α)]与pH的关系如图所示。下列叙述正确的是( )
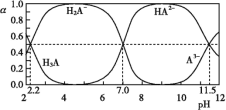
A.根据图,可得Ka1(H3A)≈10-7
B.将等物质的量的NaH2A和Na2HA混合物溶于水,所得的溶液中α(H2A-)=α(HA2-)
C.以酚酞为指示剂(变色范围pH 8.2~10.0),将NaOH溶液逐滴加入H3A溶液中,当溶液由无色变为浅红色时停止滴加,则生成NaH2A
D.在上述含A的各种粒子的体系中,若溶液pH为11.5时,则c(H2A-)+5c(A3-)+c(OH-)=c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
A.常温常压下,![]() 甲基
甲基![]() 中含有的中子数为
中含有的中子数为![]()
B.将![]() 溶于稀氨水中,所得溶液呈中性,则溶液中
溶于稀氨水中,所得溶液呈中性,则溶液中![]() 的数目为
的数目为![]()
C.![]() 和
和![]() 在催化剂和加热条件下充分反应生成NO的分子数为
在催化剂和加热条件下充分反应生成NO的分子数为![]()
D.常温下,![]() 的
的![]() 溶液中,发生电离的水分子数为
溶液中,发生电离的水分子数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某二元酸(化学式用H2A表示)在水中的电离方程式是H2A═H++HA-,HA-![]() H++A2-;试完成下列问题:
H++A2-;试完成下列问题:
NaHA溶液显__(填“酸性”、“中性”或“碱性”),Na2A溶液显__(填“酸性”、“中性”或“碱性”)。理由是__(用离子方程式表示)。
(2)pH=5的NH4Cl溶液与pH=5的HCl溶液中由水电离出的c(H+)分别是__、__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知室温时,![]() 某一元酸HA在水中有
某一元酸HA在水中有![]() 发生电离,下列叙述不正确的是
发生电离,下列叙述不正确的是![]()
①该溶液的![]() ;
;
②升高温度,溶液的pH增大;
③此酸的电离平衡常数约为![]() ;
;
④加水稀释后,各离子的浓度均减小;
⑤由HA电离出的![]() 约为水电离出的
约为水电离出的![]() 的
的![]() 倍;
倍;
⑥适当增大HA的浓度,HA的电离平衡正向移动,电离平衡常数增大。
A.②④⑥B.①④⑤C.②⑤⑥D.②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况,试判断哪些违反了泡利原理________,哪些违反了洪特规则________。
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
(2)![]() 可用于制造火柴,其分子结构如图所示。
可用于制造火柴,其分子结构如图所示。

![]() 分子中硫原子的杂化轨道类型为________。
分子中硫原子的杂化轨道类型为________。
![]() 每个
每个![]() 分子中含有的孤电子对的数目为________。
分子中含有的孤电子对的数目为________。
(3)科学家合成了一种阳离子“![]() ”,其结构是对称的,5个N排成“V”形,每个N都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“
”,其结构是对称的,5个N排成“V”形,每个N都达到8电子稳定结构,且含有2个氮氮三键;此后又合成了一种含有“![]() ”的化学式为“
”的化学式为“![]() ”的离子晶体,其电子式为________。分子
”的离子晶体,其电子式为________。分子![]() 中键与键之间的夹角为
中键与键之间的夹角为![]() ,并有对称性,分子中每个原子的最外层均满足8电子稳定结构,其结构式为________________。
,并有对称性,分子中每个原子的最外层均满足8电子稳定结构,其结构式为________________。
(4)直链多磷酸根阴离子是由两个或两个以上磷氧四面体通过共用顶角氧原子连接起来的,如图所示。则由n个磷氧四面体形成的这类磷酸根离子的通式为________。
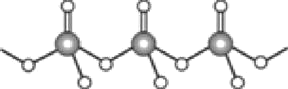
(5)碳酸盐中的阳离子不同,热分解温度就不同。下表为四种碳酸盐的热分解温度和金属阳离子半径
碳酸盐 |
|
|
|
|
热分解温度 | 402 | 900 | 1172 | 1360 |
金属阳离子半径 | 66 | 99 | 112 | 135 |
随着金属阳离子半径的增大,碳酸盐的热分解温度逐步升高,原因是_____________。
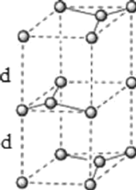
(6)石墨的晶体结构和晶胞结构如图所示。已知石墨的密度为![]() ,
,![]() 键的键长为
键的键长为![]() ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为![]() ,则石墨晶体的层间距为________cm。
,则石墨晶体的层间距为________cm。
 。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com