
【题目】某烷烃的结构简式为CH3CH(CH3)CH(C2H5)2。
(1)该烷烃的名称是____________________。
(2)该烷烃可用不饱和烃与足量氢气反应得到。若不饱和烃为烯烃A,则烯烃的结构简式可能有________种。
(3)有一种烷烃C与上述烷烃是同分异构体,它却不能由任何烯烃催化加氢得到。则C的结构简式为______________。与氯气发生取代反应所得一氯代物有________种。
【答案】2-甲基-3-乙基戊烷4 1
1
【解析】
(1)依据烷烃的命名原则:“长、多、近、小、简”命名即可;
(2)若A是单烯烃与氢气加成后的产物,则烷烃中相邻两个C上需有H;
(3)若A的一种同分异构体不能由任何烯烃催化加氢得到,则烷烃中相邻两个C上至少有一个C原子没有H;以此解答。
CH3CH(CH3)CH(C2H5)2为某烷烃的结构简式,该烷烃的主链上有5个碳原子,2号位含有一个甲基,3号位含有一个乙基,则其名称是2甲基3乙基戊烷;
故答案为:2-甲基-3-乙基戊烷;
(2)若A是单烯烃与氢气加成后的产物,则烷烃中相邻两个C上需有H,由结构CH3CH(CH3)CH(C2H5)2可知,分子中两个乙基对称,两个甲基也对称,主链上可以形成4中双键位置,共有4种单烯烃结构,故答案为:4;
(3)若A的一种同分异构体不能由任何烯烃催化加氢得到,则烷烃中相邻两个C上至少有一个C原子没有H,则A的该同分异构体C为:(CH3)3CC(CH3)3,该分子中只有一种等效氢原子,所以与氯气发生取代反应所得一氯代物有1种;
故答案为:(CH3)3CC(CH3)3;1。


 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源: 题型:
【题目】某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+3B2(g)2AB3(g)化学平衡状态的影响,得到如图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是
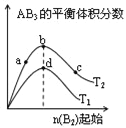
A. 图中T2一定大于T1
B. 图中b点速率一定大于d点速率
C. 达到平衡时,A2的转化率大小为:c>b>a
D. 加入催化剂可以使状态d变为状态b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了研究化学反应A+B![]() C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。试回答下列问题:
C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。试回答下列问题:
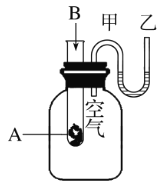
(1)该反应为________(填“放热”或“吸热”)反应。
(2)A和B的总能量比C和D的总能量_______(填“高”或“低”)。
(3)物质中的______能转化成______能释放出来。
(4)反应物化学键断裂吸收的能量__________(填“高”或“低”)于生成物化学键形成放出的能量。
(5)写出一个符合题中条件的化学方程式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子团SCN化合价为-1价,在很多方面跟卤素原子相似,因此称为“拟卤素”。拟卤素离子与卤离子还原性强弱顺序为Cl-<Br-<SCN-<I-,又知氧化性I2>S,下列反应不正确的是( )
A. (SCN)2+2Br-=Br2+2SCN-
B. (SCN)2+H2S=2H++2SCN-+S↓
C. 4H++2SCN-+MnO2![]() Mn2++(SCN)2↑+2H2O
Mn2++(SCN)2↑+2H2O
D. (SCN)2+2I-=2SCN-+I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,0.1 mol Na2CO3与盐酸混合所得的一组体积为1 L的溶液,溶液中部分微粒与pH 的关系如下图所示。下列有关叙述正确的是
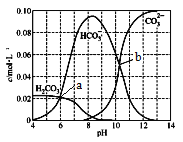
A. b点所示的溶液中:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(Cl-)
B. 随pH增大,![]() 数值先减小后增大
数值先减小后增大
C. 25℃时,碳酸的第一步电离常数Ka1=10-6
D. 溶液呈中性时:c(HCO3- )>c(Cl-)>c(CO32-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为镁--次氯酸盐燃料电池的工作原理图,下列有关说法不正确的是

A. 该燃料电池中镁为负极,发生还原反应
B. 电池的总反应式为Mg+ClO-+H2O===Mg(OH)2↓+Cl-
C. 放电过程中OH-移向负极
D. 酸性电解质的镁--过氧化氢燃料电池正极反应为:H2O2+2H++2e-===2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | ⑩ |
(1)用电子式表示元素④与⑥的化合物的形成过程________________________________,该化合物属于___________(填“共价”或“离子”)化合物.
(2)在这些元素中,化学性质最不活泼的是__________(填具体元素符号,下同),原子结构示意图为____________.元素⑩在周期表中的位置_____________.
(3)在最高价氧化物的水化物中,酸性最强的化合物的分子式是_______________.
(4)元素①与⑦的化合物是由__________(填“极性”、“非极性”)键形成的.
(5)③与⑥的气态氢化物稳定性强的是________、沸点低的是______________(填分子式)
(6)③⑥⑦三种元素形成的离子半径由大到小的顺序是__________________(填离子符号)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01 mol·L–1 r溶液的H+的浓度也是0.01 mol·L–1,s通常是难溶于水的有机混合物。上述物质的转化关系如图所示。下列说法正确的是( )
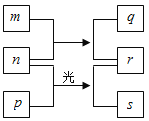
A. 原子半径的大小W<X<YB. 元素的非金属性Z>X>Y
C. Z的氧化物的水化物为强酸D. Y的氢化物常温常压下为液态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然气的主要成分为CH4,可将CH4设计成燃料电池,来解决能源问题,装置如图所示。在标准状况下,持续通入甲烷,消耗甲烷VL。下列说法错误的是

A. 当0<V≤33.6 L时,负极反应式为CH4+10OH--8e-== CO32-+7H2O
B. 正极反应式为O2 +4H+ +4e-==2H2O
C. 当V=67.2 L时,电池总反应方程式可写为CH4+2O2+NaOH== NaHCO3+2H2O
D. 电解质溶液中的Na+向正极移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com