
| 5 |
| 3 |
| 5 |
| 3 |


科目:高中化学 来源: 题型:
| A、1 mol Cl2参加反应转移的电子数为NA |
| B、在0℃,101kPa时,22.4L氢气中含有2NA个氢原子 |
| C、1molO2的质量为32g/mol |
| D、2molHCl溶解在1L水中得到盐酸溶液的物质的量浓度为2mol/l |
查看答案和解析>>
科目:高中化学 来源: 题型:
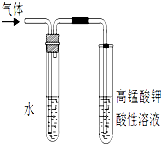 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.查看答案和解析>>
科目:高中化学 来源: 题型:
| 甲 | 乙 | 丙 | ||
| 起始物质的量 | n(SO2)/mol | 0.4 | 0.8 | 0.8 |
| n(O2)/mol | 0.24 | 0.24 | 0.48 | |
| SO2的平衡转化率/% | 80 | α1 | α2 | |
| A、甲中反应的平衡常数小于乙 |
| B、该温度下,平衡常数值为400 |
| C、平衡时,丙中c(SO3)是甲中的2倍 |
| D、平衡时,甲中O2的转化率大于乙中O2的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2Na+2H2O=H2↑+2NaOH |
| B、Cl2+NaOH=NaCl+NaClO+H2O |
| C、SO2+Cl2+2H2O=2HCl+H2SO4 |
| D、2F2+2H2O=4HF+O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、所有主族非金属元素,都有最高正价且等于其最外层电子数 |
| B、单原子形成的离子,一定具有稀有气体原子的核外电子排布 |
| C、某元素原子最外层电子数有2个,则该元素一定是第ⅡA族的元素 |
| D、两种单原子,若核外电子排布完全相同,则一定属于同种元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等物质的量的硫蒸汽和硫固体分别完全燃烧,前者放出热量比后者少 |
| B、由C(石墨)=C(金刚石);△H=+1.90 kJ?mol-1可知,金刚石比石墨稳定 |
| C、在101kPa时,2g H2完全燃烧生成液态水,放出285.8kJ热量,则表示氢气燃烧热的热化学方程式为:2H2(g)+O2(g)═2H2O(l);△H=-571.6 kJ?mol-1 |
| D、在稀溶液中,H+(aq)+OH-(aq)═H2O(1);△H=一57.3 kJ?mol-1,若将含0.5mol H2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于57.3 kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com