
【题目】用电石(CaC2)制备的乙炔气体中常混有少量H2S气体。请用图中仪器和药品组成一套制备、净化乙炔的装置,并可通过测定乙炔的量, 从而计算电石(CaC2)的纯度。
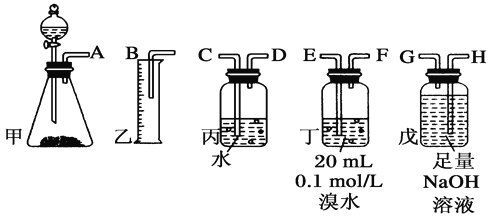
(1)完成甲装置发生的化学反应方程式______________。
(2)进行实验时,所制气体从左向右流,仪器的正确连接顺序是____________________(填接口字母);
(3)为了使实验中气流平稳,甲中分液漏斗里的液体X通常用____________________;
(4)若在标准状况下溴水与乙炔完全反应生成C2H2Br4,已知称取电石m g,测得量筒内液体体积V mL,则电石纯度可表示为____________________;
(5)若没有除H2S的装置,测定结果将会________(填“偏高”、“偏低”或“不变”),理由是_________________________________ (用化学方程式表示)。
【答案】 ![]() AHGEFDCB 饱和食盐水
AHGEFDCB 饱和食盐水 ![]() % 偏高 H2S+Br2===S↓+2HBr
% 偏高 H2S+Br2===S↓+2HBr
【解析】(1). 甲是制取乙炔的实验装置,电石与水反应生成乙炔和氢氧化钙,化学方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑,故答案为:CaC2+2H2O→Ca(OH)2+C2H2↑;
(2). 电石与足量水反应生成乙炔,其中混有的H2S气体可用NaOH溶液吸收,乙炔气体被溴水吸收后余下的部分通过排水法测量其体积,所以正确的连接顺序为:AHGEFDCB,故答案为:AHGEFDCB;
(3). 实验室一般用饱和食盐水代替水进行实验,以获得平稳的乙炔气流,故答案为:饱和食盐水;
(4). 在标准状况下溴水与乙炔完全反应生成C2H2Br4,化学方程式为:C2H2+2Br2= C2H2Br4,溴单质的物质的量为n(Br2)=0.1mol/L×0.02L=0.002mol,消耗乙炔的物质的量为:0.002mol÷2=0.001mol,测得量筒内液体体积为VmL,则与溴水反应后剩余乙炔的体积为VmL,物质的量为V×10-3L÷22.4L/mol=![]() mol,由CaC2+2H2O→Ca(OH)2+C2H2↑可知,CaC2的物质的量为(0.001+
mol,由CaC2+2H2O→Ca(OH)2+C2H2↑可知,CaC2的物质的量为(0.001+![]() )mol,质量为(0.001+
)mol,质量为(0.001+![]() )×64g,则电石纯度可表示为
)×64g,则电石纯度可表示为 ×100%=
×100%=![]() %,故答案为:
%,故答案为:![]() %;
%;
(5). 硫化氢具有还原性,能与溴发生氧化还原反应,导致测得乙炔的物质的量偏多,最终测得电石的纯度偏高,硫化氢和溴反应生成溴化氢和单质硫,化学方程式为:H2S+Br2=S↓+2HBr,故答案为:偏高;H2S+Br2=S↓+2HBr。


科目:高中化学 来源: 题型:
【题目】已知CO是工业上重要的原料,可作燃料、冶炼金属、合成液体酒精等。
(1)研究表明:反应CO(g)+H2O(g) ![]() H2(g)+CO2(g) ⊿H = ?
H2(g)+CO2(g) ⊿H = ?
平衡常数随温度的变化如下表所示:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
Ⅰ.通过平衡常数随温度的变化情况,推断反应热⊿H________ 0 (填>、<、﹦ )
Ⅱ.若反应在500℃时进行,设起始的CO和H2O的浓度均为0.020 mol·L-1,在该条件下CO的平衡转化率为________。
(2)用CO做燃料电池电解CuSO4溶液、FeCl3和FeCl2混合液的示意图如图1所示,其中A、B、D 均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。

①甲中通入CO的电极为______(填“正”、“负”、“阴”、“阳”)极,该电极反应方程式为__________。
②若乙中A极析出的气体在标准状况下的体积为2.24L,此时要使乙中CuSO4溶液恢复到原来的浓度,需要加入的物质及其物质的量是(___________)。
A.0.1molCuO B.0.1molCu(OH)2 C.0.1molCu2(OH)2CO3
③丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图2所示。完成丙装置C、D电极反应式:C:____________________________;D:________________________________;丙装置溶液中 c(Cl-)= _______________ mol/L 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列问题:
(1)甲基的电子式___________。
(2)写出由丙烯制备聚丙烯的化学反应方程式_______________________。
(3)反式2 -丁烯的结构简式______________________________
(4)与H2加成生成2,5 - 二甲基己烷的炔烃的系统命名___________________________
(5)![]() 的系统命名_____________________________________。
的系统命名_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由乙烯和丙二酸等物质合成I,合成路线如下:
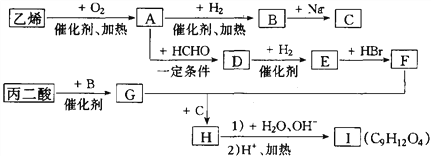
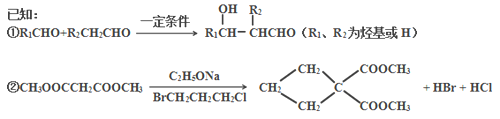
请回答下列问题:
(1)丙二酸的结构简式是_________。
(2)有机物D的分子式为C5H10O4,其官能团的名称是__________。
(3)写出A→B的化学反应方程式______________________________________。
(4)E→F的反应类型是______________。
(5)在一定条件下,丙二酸与乙二醇通过发生缩聚反应生成高分子化合物。写出该高分子化合物的化学式______________。
(6)I的同分异构体中属于芳香族化合物且满足下列条件的有_____种。
①苯环上有4个取代基;②与FeCl3溶液发生显色反应;③每种同分异构体1 mol能与1 mol碳酸钠发生反应,也能与足量金属钠反应生成2molH2;④一个碳原子连接2个或2个以上羟基不稳定。
其中苯环上的一氯代物只有一种的是___________________。(写出其中一种的结构简式)
(7)丙二酸可由乙烯、甲醛为原料制得(其它无机试剂任选)。请模仿并画出合成路线图。___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是由4个碳原子结合成的6种有机物(氢原子没有画出)
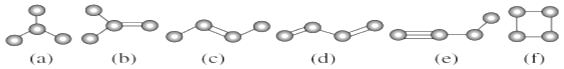
(1)有机物(a)有一种同分异构体,试写出其结构简式______.
(2)上述有机物中与(c)互为同分异构体的是______(填代号).
(3)任写一种与(e)互为同系物的最简单有机物的结构简式______.
(4)上述有机物中不能使酸性高锰酸钾溶液褪色的有______(填代号).
(5)(a)(b)(c)(d)四种物质中,4个碳原子一定处于同一平面的有______(填代号).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O![]() Cd(OH)2 + 2Ni(OH)2,有关该电池的说法正确的是
Cd(OH)2 + 2Ni(OH)2,有关该电池的说法正确的是
A. 充电时阳极反应:Ni(OH)2 -e— + OH- == NiOOH + H2O
B. 充电过程是化学能转化为电能的过程
C. 放电时负极附近溶液的碱性不变
D. 放电时电解质溶液中的OH-向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为元素在生物体内的含量分布情况,下列表述不正确的是( )
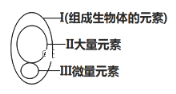
A. Ⅰ在非生物界中都能找到,体现了生物界与非生物界的统一性
B. Ⅲ含量虽少,却是生物体正常生命活动不可缺少的
C. Ⅱ和Ⅲ为生物体的必需元素,一旦缺乏就可能会导致相应的病症
D. P、S、K、Ca、Zn属于大量元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com